01
文献学习

今天分享的文献是由北京清华长庚医院李国新联合 云南省肿瘤医院放射科李振辉、南方医科大学南方医院、中山大学肿瘤防治中心等团队 于2025年8月在**《** Cell Reports Medicine**》(中科院1区top,IF=10.6)** 上发表的研究"TME-guided deep learning predicts chemotherapy and immunotherapy response in gastric cancer with attention-enhanced residual Swin Transformer"即基于注意力增强残差Swin Transformer的TME引导深度学习模型预测胃癌化疗与免疫治疗反应,该研究开发了一个名为"注意力增强残差Swin Transformer(AER-SwinT)"的多任务深度学习模型,利用术前CT图像和临床数据,同时预测胃癌患者术后辅助化疗反应、肿瘤微环境(ImmunoScore 和 POSTN 表达),并进一步评估其对免疫治疗反应的预测能力。模型在3095例患者的多中心队列中验证,表现出良好的预测性能和临床潜力。
创新点:①多任务深度学习框架 :首次将化疗反应预测与TME评估结合,提升模型性能与泛化能力。②注意力增强残差Swin Transformer :创新性地引入分层注意力机制,实现CT图像多粒度特征提取。③免疫治疗获益预测:通过TME biomarkers间接预测免疫治疗反应,拓展影像组学应用边界。
临床价值:①非侵入性化疗决策支持 :精准识别化疗敏感/耐药患者,避免无效治疗与副作用。②免疫治疗获益分层 :通过TME预测免疫反应,助力晚期胃癌个体化免疫治疗。③动态监测TME状态:替代活检实现肿瘤微环境无创评估,降低成本与操作复杂性。
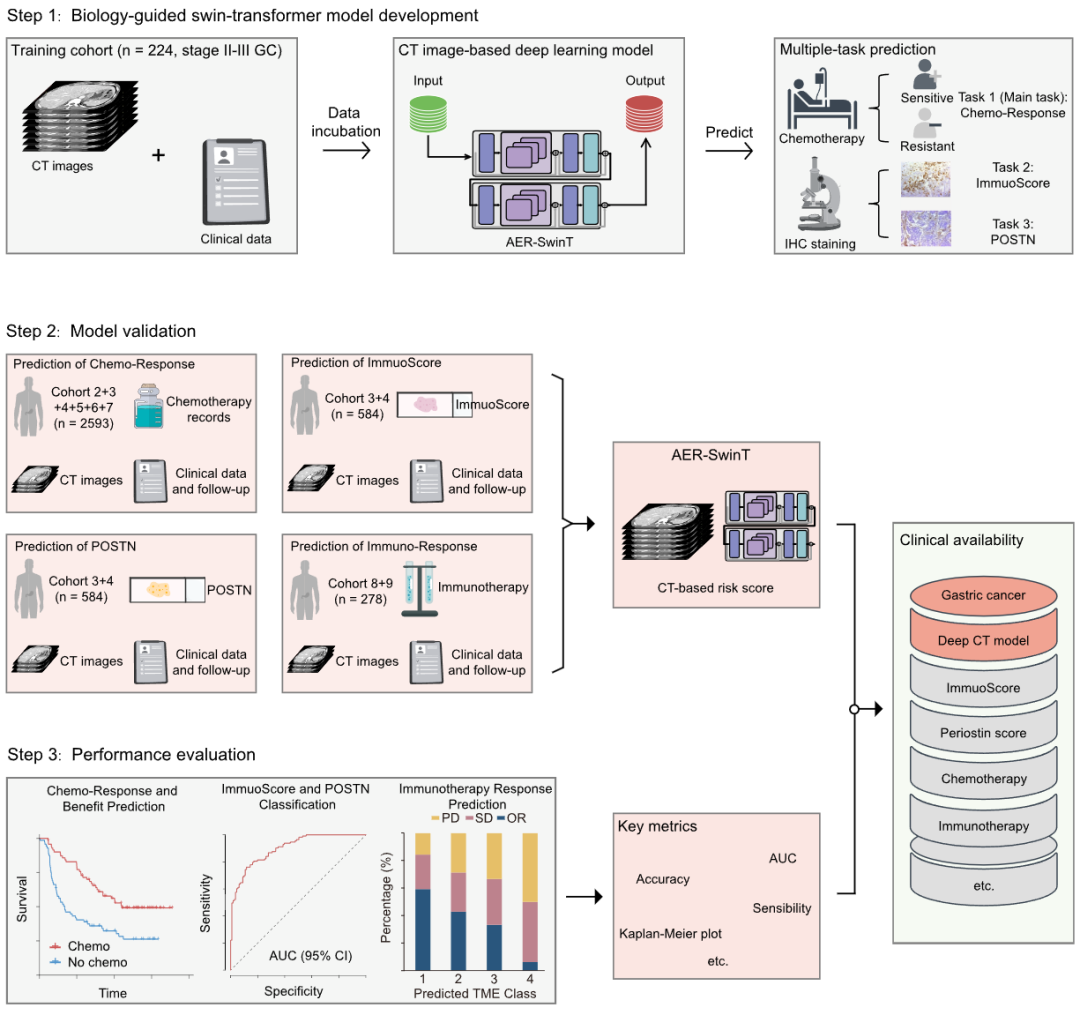
图 1:研究工作流程图
步骤1:生物学引导的Swin Transformer模型开发
输入数据:训练队列(224例II-III期胃癌患者)的术前CT图像、临床数据;
模型任务:多任务预测(主任务:化疗反应;两个子任务:ImmunoScore、POSTN表达);
参考标准:化疗反应以无病生存期(DFS)为依据,ImmunoScore和POSTN以免疫组化(IHC)染色结果为金标准。
步骤2:模型验证
验证数据:涵盖9个独立队列(共3095例患者),包括南方医科大学南方医院(SMU)、中山大学肿瘤防治中心(SYSUCC)、云南省肿瘤医院(YNCH)等5个中心的化疗队列(2593例),以及278例晚期胃癌免疫治疗队列(SMU+广东省中医院GPHCM);
验证任务:化疗反应预测、TME标志物(ImmunoScore/POSTN)预测、免疫治疗反应预测。
步骤3:性能评估
评估指标:化疗/免疫治疗反应预测采用AUC、灵敏度、特异度等;生存分析采用Kaplan-Meier曲线;
核心产出:基于CT的风险评分、TME分型,最终用于指导个性化治疗决策。
02
研究背景和目的
研究背景
胃癌是全球高发的恶性肿瘤,其治疗决策的精准化面临严峻挑战。在局部进展期胃癌的术后管理中,以5-氟尿嘧啶为基础的辅助化疗是标准方案,但临床实践显示,晚期患者的5年总生存率仍低于40% ,这表明大量患者可能接受了无效甚至有害的化疗,其根本原因在于缺乏能够有效预测化疗获益的可靠生物标志物 。与此同时,以免疫检查点抑制剂为代表的免疫治疗虽已成为晚期胃癌的一线方案,却同样面临整体响应率低、获益人群难以甄别的困境 。尽管PD-L1表达、微卫星不稳定性等标志物被用于指导免疫治疗,但其预测效能并不完美。近年来,研究证实肿瘤微环境(TME)在调控肿瘤进展和治疗反应中扮演核心角色 ,评估TME状态对于优化化疗和免疫治疗决策至关重要。然而,当前TME的评估主要依赖侵入性的组织活检和免疫组化染色,存在成本高昂、耗时长、技术复杂且无法动态监测等局限性。因此,临床上迫切需要开发一种非侵入性、高效且经济的全新工具,能够同时评估化疗响应和TME特征,从而为胃癌患者提供真正个性化的治疗策略。
研究目的
本研究旨在开发并验证一种名为注意力增强残差Swin Transformer(AER-SwinT)的创新性多任务深度学习模型 ,以期通过常规术前CT影像,解决胃癌治疗中的关键预测难题。研究的核心目标是利用该模型非侵入性地精准预测局部进展期胃癌患者术后辅助化疗的响应 ,旨在早期识别出能够从5-氟尿嘧啶化疗中真正获益的敏感人群,并使不敏感者免于无效治疗。为增强主任务的预测效能并赋予模型生物学可解释性,研究引入了免疫评分(ImmunoScore)和骨膜蛋白(POSTN)表达作为两个中间预测子任务 ,通过多任务学习策略让模型在预测化疗响应的同时,能够自主学习并量化关键的TME生物学特征。基于这些TME特征与免疫应答的已知关联,研究的最终目标是进一步评估该模型在晚期胃癌队列中预测抗PD-1免疫治疗疗效的潜在价值。综上所述,本研究旨在构建一个基于影像的综合性预测框架,通过将深度学习技术与肿瘤生物学知识深度融合,为实现胃癌化疗与免疫治疗的精准化、个性化决策提供科学依据和可靠工具。
03
数据和方法
研究数据
总样本量:3095例胃癌患者,来自中国5家医疗中心,时间跨度2005--2022年。
训练与验证队列:9个独立队列,包括内部验证和外部验证。
免疫治疗队列:278例晚期胃癌患者接受抗PD-1治疗。
数据类型:术前CT图像、临床病理数据、IHC染色的TME标志物(ImmunoScore、POSTN)。
技术方法
模型构建:
基于Swin Transformer构建AER-SwinT模型,提取CT图像的多层次特征。
引入通道平均注意力图和残差连接,增强模型对关键区域的关注。
多任务学习:主任务为化疗反应预测,辅助任务为ImmunoScore和POSTN预测。
模型训练与验证:
使用PyTorch实现,SGD优化器,交叉熵损失函数。
评估指标:AUC、敏感性、特异性、准确率、混淆矩阵等。
临床关联分析:
使用倾向性评分匹配(PSM)评估化疗获益。
分析模型预测的TME状态与免疫治疗反应、生存预后的关系。
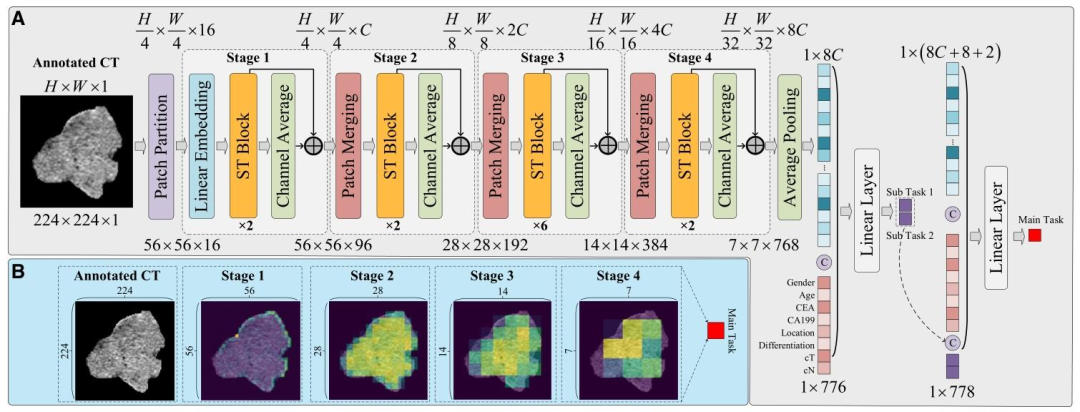
图 2:AER-SwinT模型架构及中间注意力
A:模型架构
输入层:224×224×1的CT图像块(以肿瘤为中心裁剪);
核心模块:
补丁划分(Patch Partition):将CT图像分割为4×4非重叠补丁,转化为16维特征向量;
线性嵌入(Linear Embedding):将补丁向量投影至指定维度(C);
四层Swin Transformer块:逐步提取从细到粗的分层特征,通过补丁合并(Patch Merging)降低分辨率、增加通道数(最终输出7×7×768特征图);
通道平均注意力(Channel Average Attention):结合挤压-激励(SENet)机制,通过点积和残差连接动态聚焦肿瘤关键区域;
输出层:融合CT图像特征、8项临床特征及两个子任务输出,最终完成主任务(化疗反应预测),总特征维度为778(768+8+2)。
B:中间注意力图
展示模型在不同阶段对CT图像的注意力分布:初始阶段聚焦肿瘤边缘信息,随模型深度增加,逐渐关注肿瘤内部区域;
04
实验结果
化疗反应预测:
AUC在各验证队列中为0.871--0.900,准确性>80%,敏感性74--91%,特异性67--93%。
TME预测:
ImmunoScore预测AUC为0.838--0.844,POSTN预测AUC为0.817--0.848。
化疗获益分析:
预测为化疗敏感的患者,辅助化疗显著改善DFS和OS;预测为耐药的患者无获益。
免疫治疗反应:
预测为高ImmunoScore或低POSTN的患者,免疫治疗响应率更高。
整合TME模型后,PD-L1的预测能力提升。
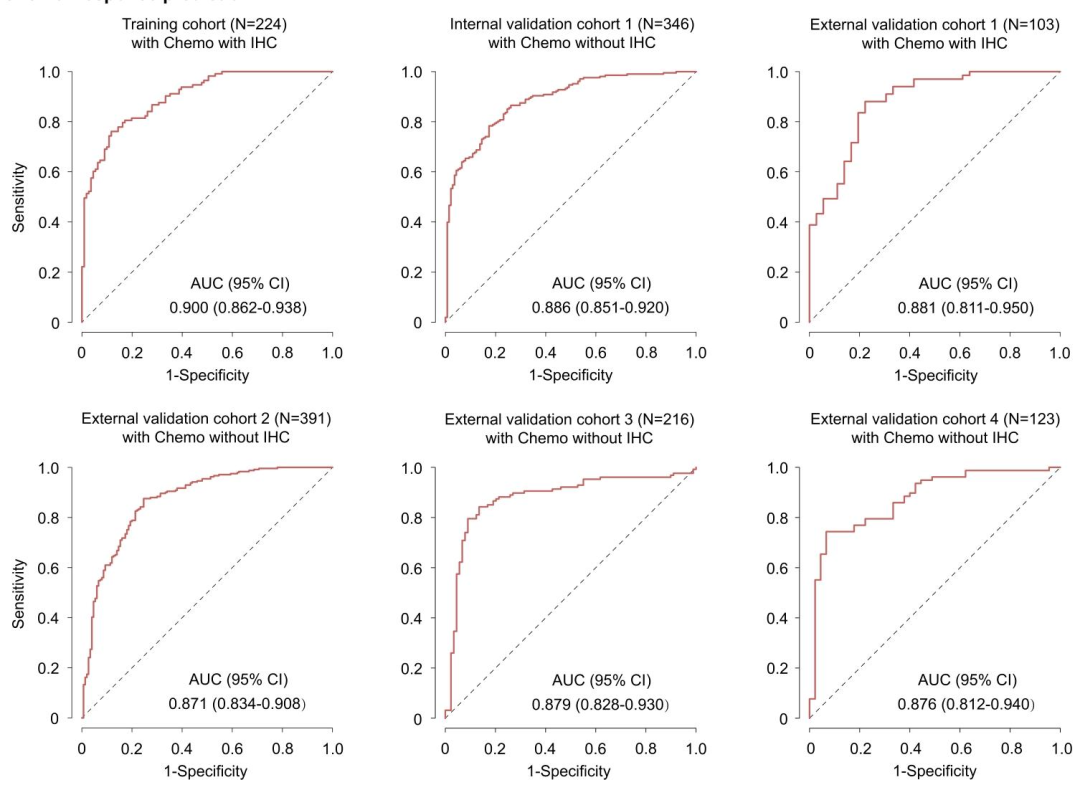
图 3:化疗反应预测的诊断准确性
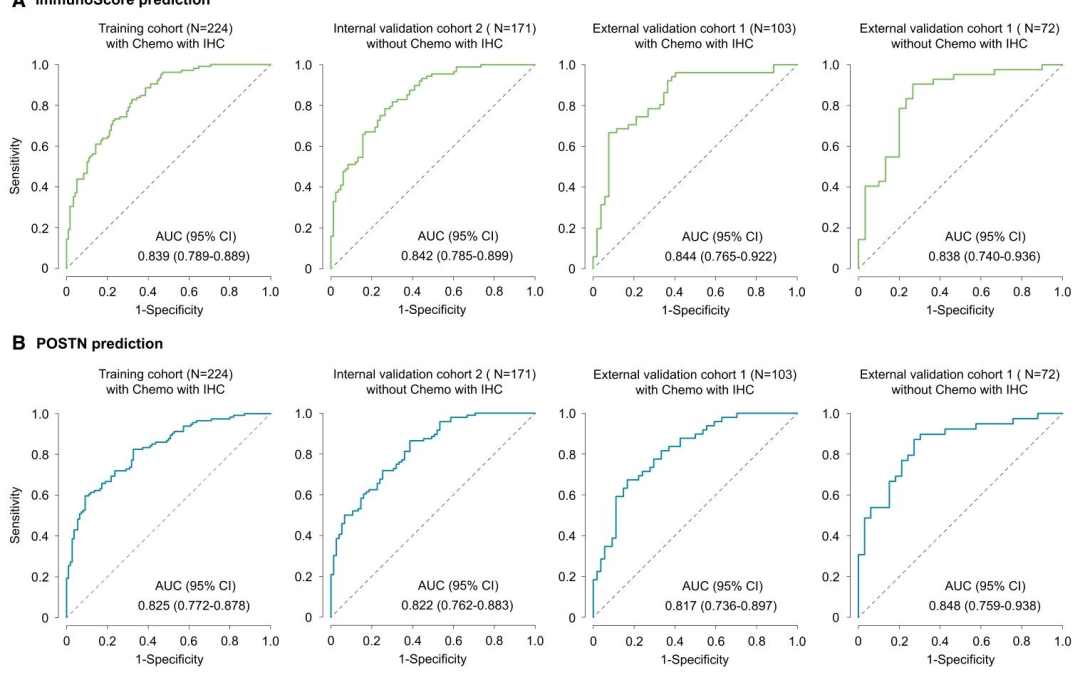
图 4:TME标志物(ImmunoScore/POSTN)预测的诊断准确性
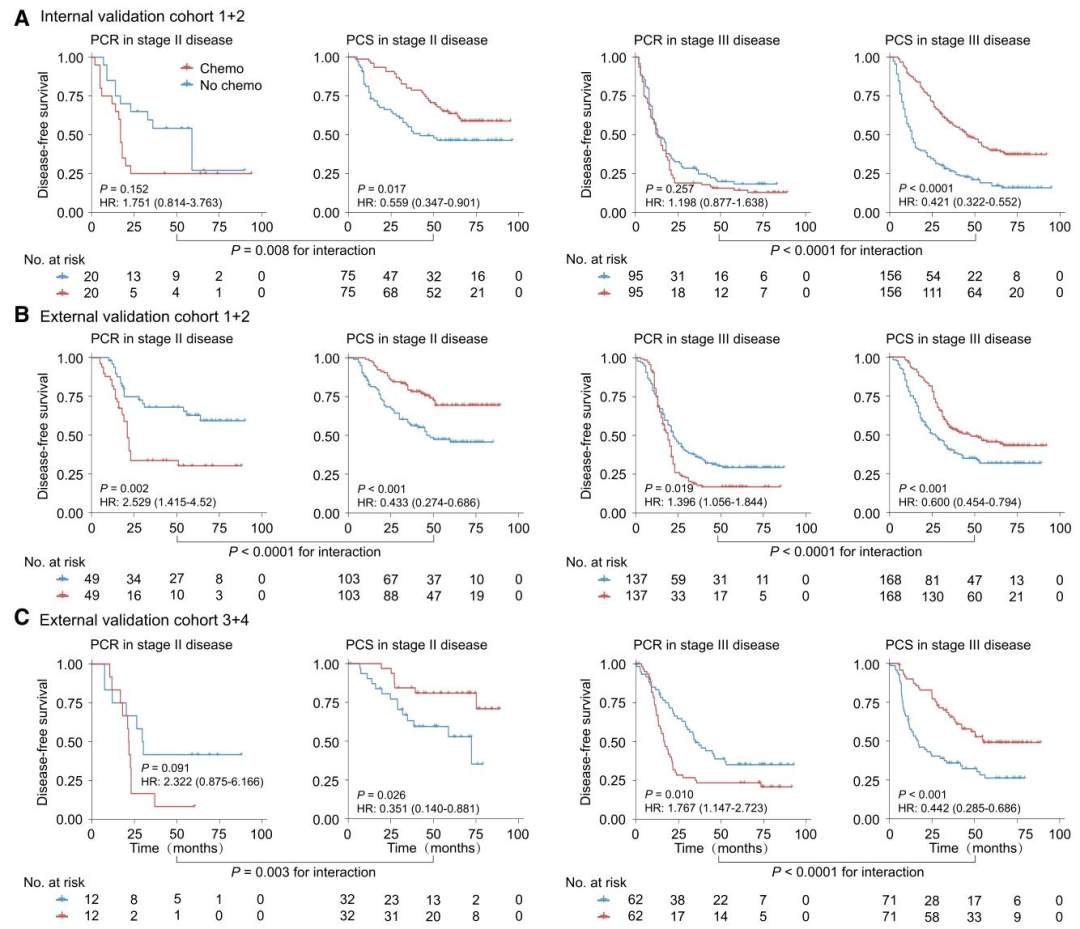
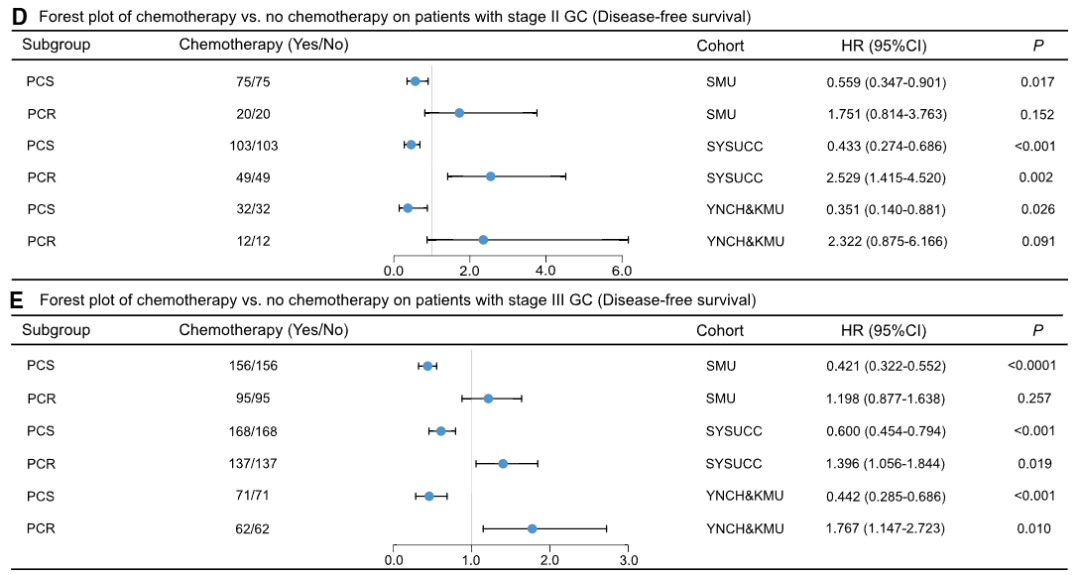
图 5:模型对化疗无病生存期(DFS)获益的预测价值
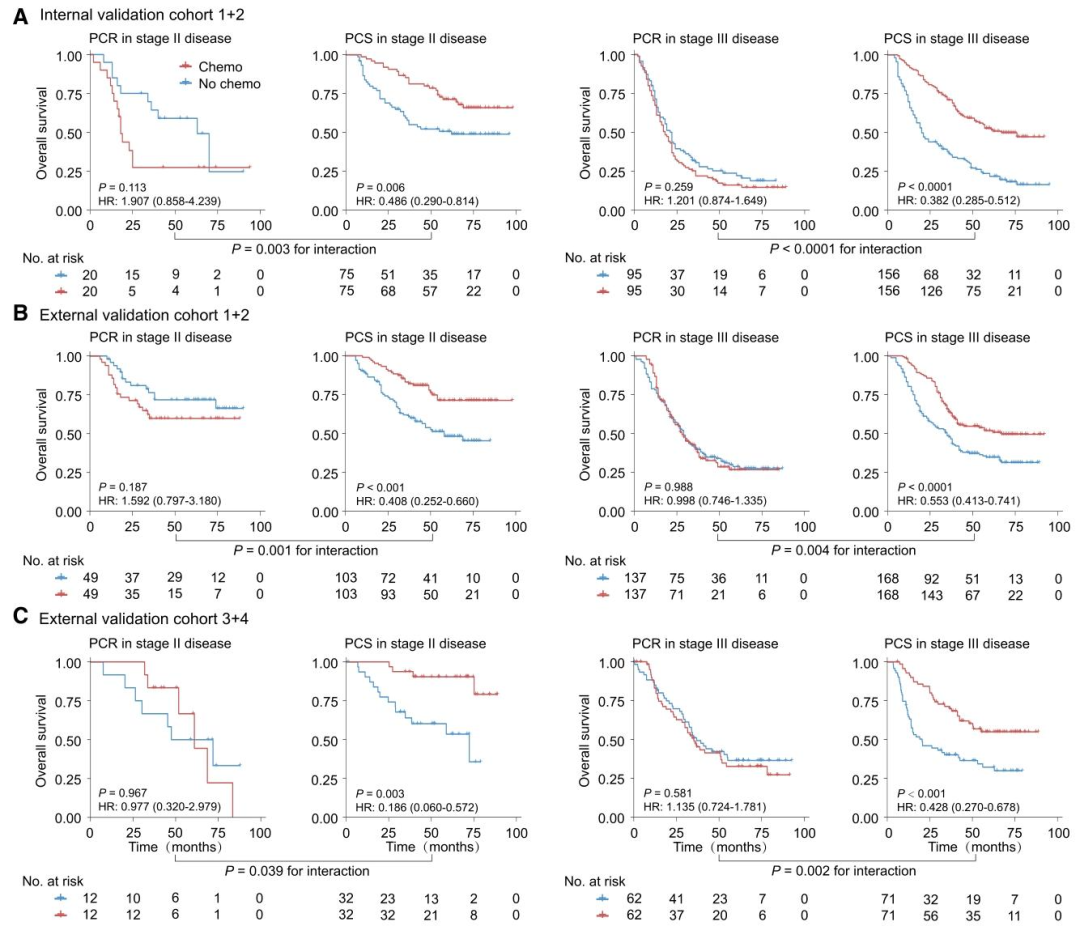
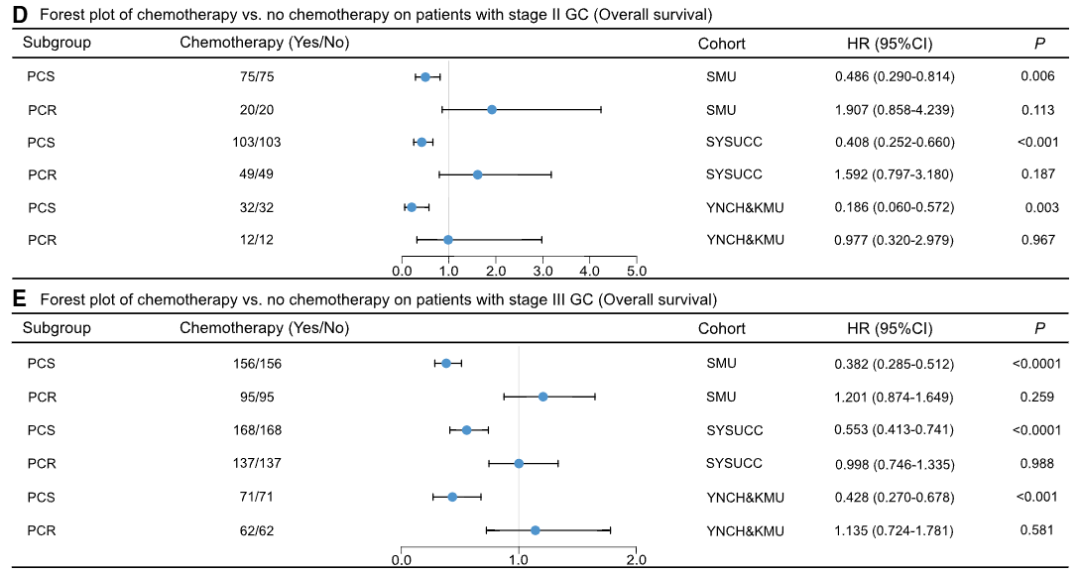
图 6:模型对化疗总生存期(OS)获益的预测价值
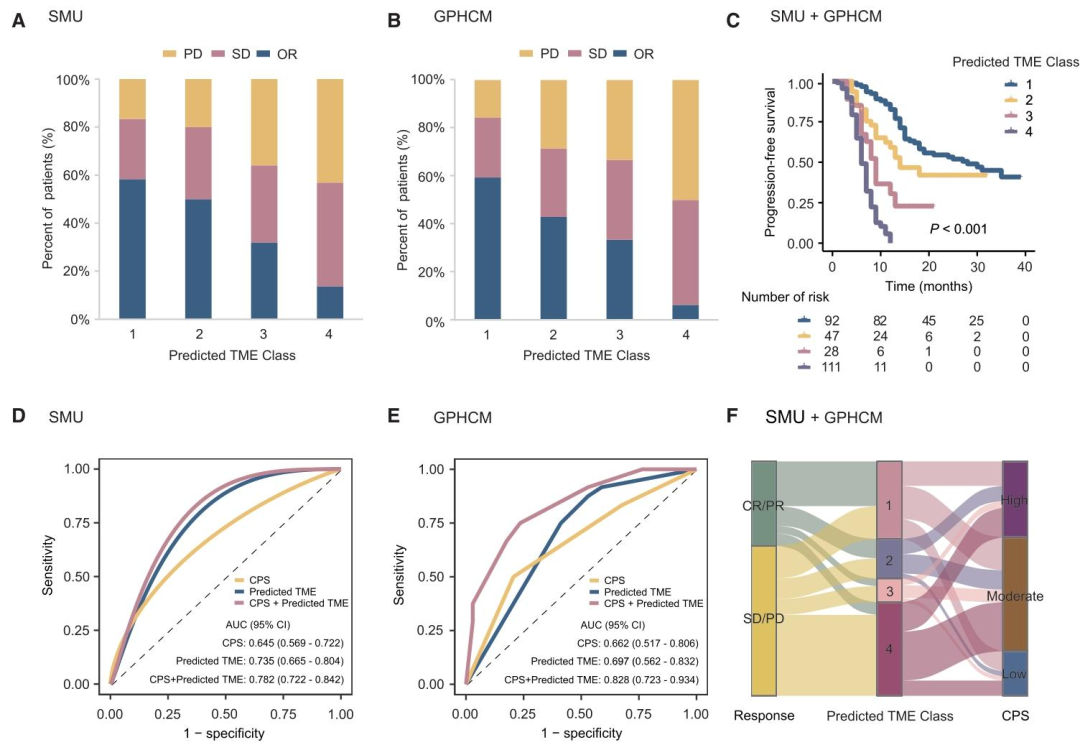
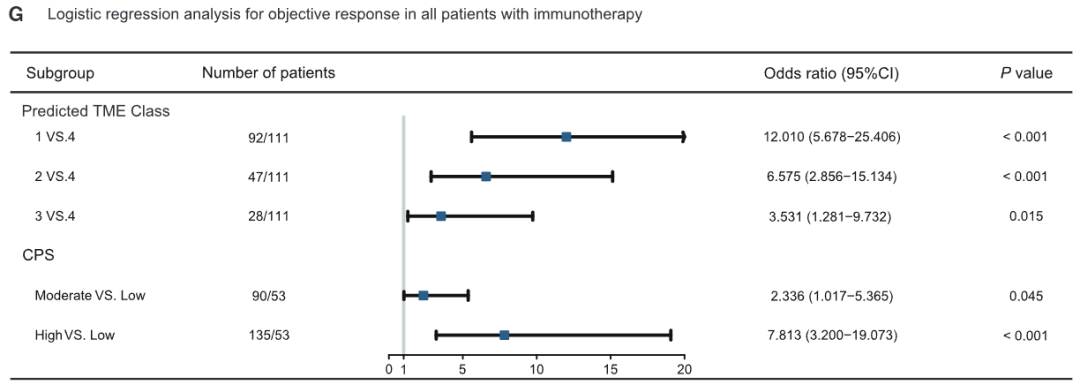
图 7:模型对免疫治疗反应及临床结局的预测价值
05
研究结论
该研究提出并验证了一种基于注意力增强的残差Swin Transformer(AER-SwinT)的多任务深度学习模型 ,利用来自3,095名胃癌患者的术前CT影像和临床数据,实现了对辅助化疗反应及肿瘤微环境(TME)关键标志物(ImmunoScore和POSTN)的无创、同步预测 。研究发现,该模型在多个内部和外部验证队列中均表现出高准确性,预测化疗反应的AUC值高达0.87-0.90。更重要的是,模型预测的化疗敏感患者能够从辅助化疗中获得显著的生存获益,而耐药患者则无此获益 。此外,基于模型预测的TME状态,研究进一步证实其能有效区分抗PD-1免疫治疗的获益人群 :预测为高ImmunoScore或低POSTN的患者,其客观缓解率显著更高(分别达55.0%-56.4% vs. 17.5%-10.5%)。该研究首次将多任务深度学习与生物学引导的TME标志物相结合,不仅提高了化疗疗效预测的准确性,还为个性化免疫治疗决策提供了新的无创工具,为胃癌的精准治疗开辟了新路径。
参考文献:Sang S, Sun Z, Zheng W, Wang W, Islam MT, Chen Y, Yuan Q, Cheng C, Xi S, Han Z, Zhang T, Wu L, Li W, Xie J, Feng W, Chen Y, Xiong W, Yu J, Li G, Li Z, Jiang Y. TME-guided deep learning predicts chemotherapy and immunotherapy response in gastric cancer with attention-enhanced residual Swin Transformer. Cell Rep Med. 2025 Aug 19;6(8):102242. doi: 10.1016/j.xcrm.2025.102242.