01
文献学习

今天分享的文献是由河北医科大学第四医院赵群等团队于2026年1月在《npj Digital Medicine》(中科院1区top,IF=15.1)上发表的研究"Multimodal digital biopsy for preoperative prediction of occult peritoneal metastasis in gastric cancer"即多模态数字活检用于胃癌隐匿性腹膜转移的术前预测,该研究开发并验证了一个多模态预测模型(Multimodal Model),整合了CT原发肿瘤的放射组学特征与临床变量,用于术前无创预测局部晚期胃癌患者的隐匿性腹膜转移。模型在多个大规模、多中心、跨国队列中表现出稳定的高预测性能(AUC 0.83--0.86),显著优于单模态模型。通过前瞻性临床试验和放射科医生交叉验证,AI辅助显著提高了诊断准确性。转录组分析进一步揭示了低风险组患者具有更强的抗肿瘤免疫微环境。
创新点:①大规模多中心前瞻性验证 :纳入1726例患者,多队列外部+前瞻性验证,AUC稳定0.83-0.86 。②首次关联转录组免疫机制 :揭示低风险组CD8+T细胞、TNFa信号富集 ,提供生物学解释。③AI辅助提升诊断效能 :前瞻交叉实验显示,放射科医生AUC从0.735升至0.872。
临床价值:①无创替代腹腔镜筛查 :减少侵入性手术,优化OPM高危患者筛选 ,降低医疗负担。②指导个体化治疗决策 :低风险直接手术,高风险优先新辅助或CRS/HIPEC ,改善预后。③高阴性预测值(0.955) :可靠排除隐匿转移,避免延误根治性手术,提升诊疗效率。
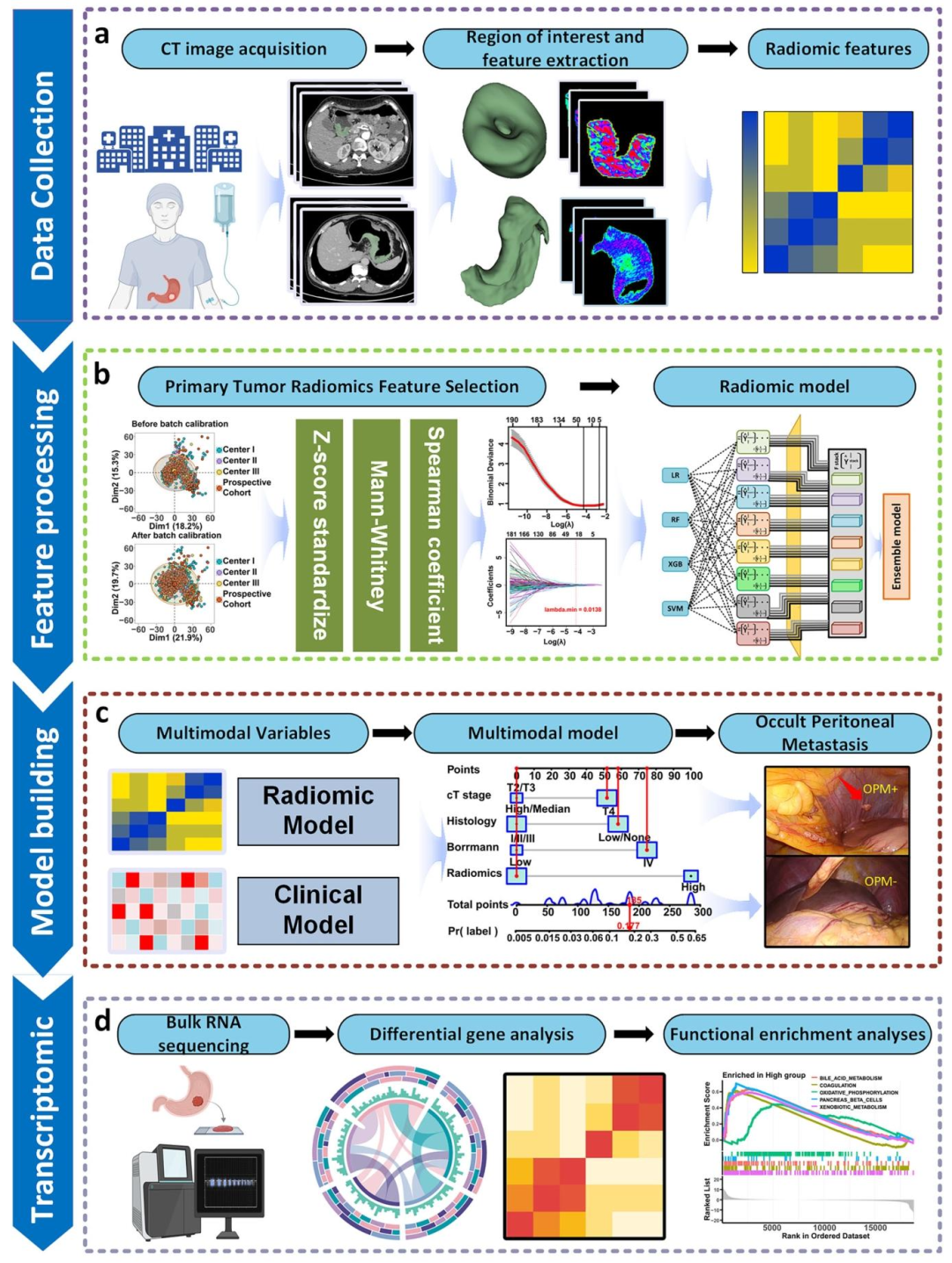
图 7:局部进展期胃癌OPM多模态模型开发与验证的研究流程总览
数据收集:术前门脉期CT→nnU-Net全自动分割原发肿瘤→3D ROI→提取1130个放射组学特征
特征处理:ComBat批次校正→Z-score标准化→特征筛选→集成学习构建放射组学模型
模型构建:临床因子+放射组学特征→多模态列线图→术中病理验证
转录组分析:倾向得分匹配18例样本→RNA测序→差异基因→功能富集
02
研究背景和目的
研究背景
胃癌是全球范围内癌症相关死亡的主要原因之一,尤其在东亚地区发病率极高。多数患者确诊时已处于进展期,腹膜转移是最常见且最致命的播散方式 。其中,隐匿性腹膜转移(OPM) 由于病灶微小或缺乏典型影像学特征,常规增强CT的敏感性极低(仅23%-76%),PET-CT和MRI虽有一定提升,但存在阴性预测值低、成本高、易受运动伪影干扰等局限。目前,分期腹腔镜仍是检测OPM的金标准 ,但其具有侵入性、需全身麻醉、费用高昂且资源有限,无法普遍开展。因此,临床上亟需一种可靠、无创的术前预测工具 以精准识别OPM高危患者。近年来,基于CT的放射组学和人工智能方法显示出潜力,但现有研究多受限于单中心设计、样本量小、依赖手动标注、缺乏外部及前瞻性验证,且缺乏生物学机制解释,难以支撑临床决策。综上,开发一种可泛化、可解释且非侵入性的OPM预测模型具有重要的临床意义。
研究目的
本研究旨在开发并验证一种多模态"数字活检"模型 ,用于术前无创预测局部进展期胃癌患者的隐匿性腹膜转移。该模型整合了基于CT原发灶的放射组学特征 与关键临床变量 ,通过自动化流程实现全自动分割与预测。研究团队利用一个大规模单中心队列进行模型训练和内部验证,并在两个独立的多中心外部验证队列 、一个评估腹膜细胞学阳性的增量队列以及一个前瞻性临床试验队列中系统评估其泛化能力。此外,通过倾向评分匹配的高低风险患者转录组分析,揭示模型风险分层背后的免疫生物学基础 (如CD8+ T细胞、TNFα信号通路等)。最终目标是提供一种准确、可解释、临床实用的非侵入性工具,用于OPM风险分层,优化个体化治疗决策,减少不必要的诊断性腹腔镜手术,并为高危患者精准选择新辅助治疗或强化局部区域治疗(如CRS/HIPEC)。
03
数据和方法
研究数据
总样本量: 1726例
**数据来源:**中国10个中心和德国1个中心
队列划分:
训练队列(n=658)
内部验证(n=282)
外部验证I(n=164)、II(n=145)
增量队列(n=477,用于细胞学阳性预测)
前瞻性队列(n=168,NCT06478368)
技术方法
**图像分割:**基于nnU-Net的深度学习自动分割原发肿瘤
放射组学特征提取: PyRadiomics提取1130个特征
特征选择与建模:
Combat协调、Z-score标准化
LASSO回归 + 集成学习(LR、XGBoost、RF、SVM)
**多模态模型构建:**整合临床独立预测因子(cT分期、组织类型、Borrmann分型等)
模型评估: AUC、校准曲线、决策曲线、NRI、IDI、Delong检验
生物学分析: RNA测序、GSEA、CIBERSORT、ssGSEA等
04
实验结果
模型性能:
训练队列AUC=0.853,内部验证AUC=0.849
外部验证I AUC=0.857,II AUC=0.850
增量队列AUC=0.834,前瞻性队列AUC=0.839
**优于单模态模型:**显著提升NRI和IDI
**AI辅助效果:**放射科医生平均AUC从0.735提升至0.872
**生存分析:**高风险组5年OS显著低于低风险组
**生物学机制:**低风险组富集CD8 T细胞、TNFα信号通路等免疫激活特征
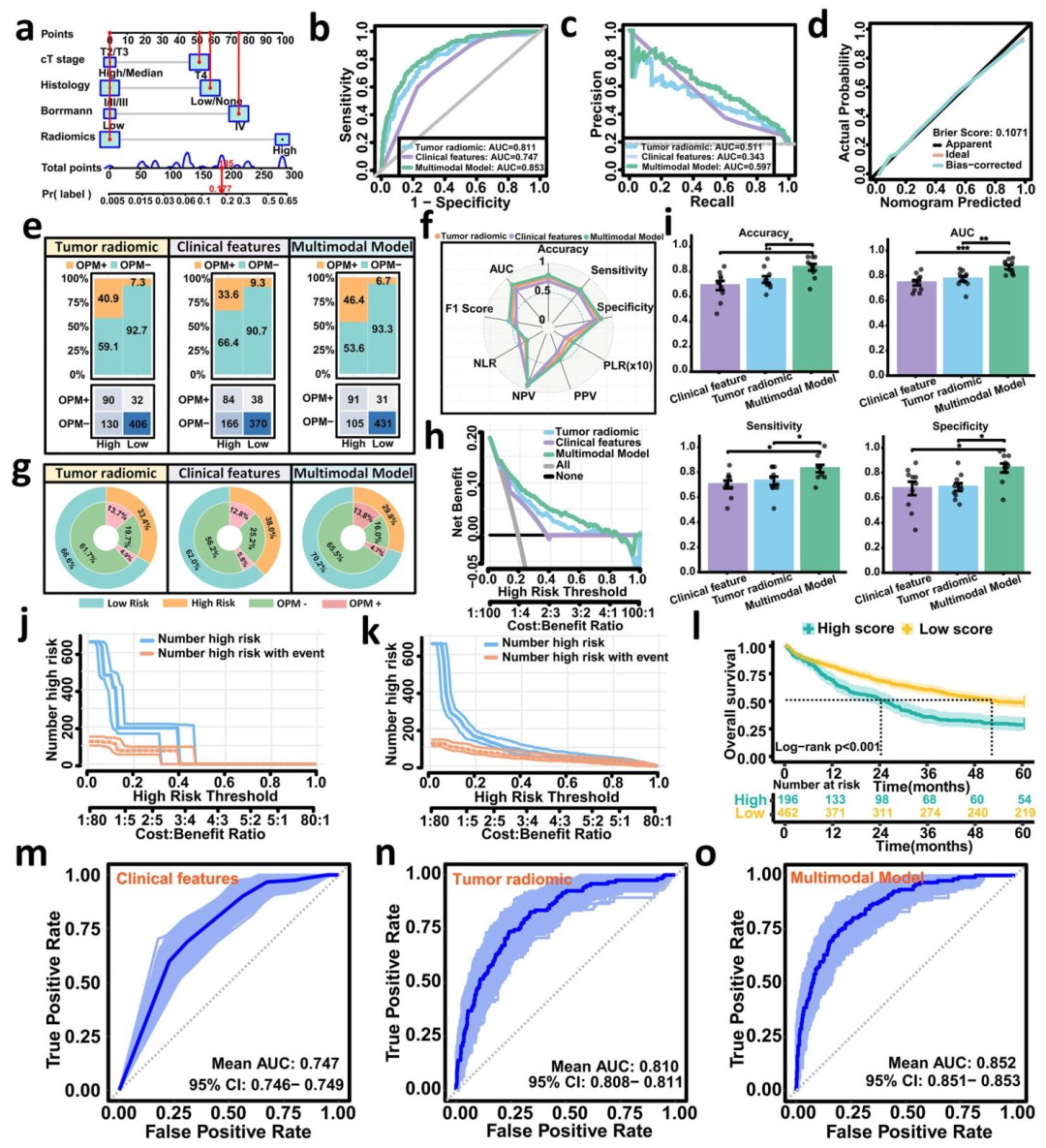
图 1:训练集中多模态模型预测胃癌隐匿性腹膜转移(OPM)的开发与性能
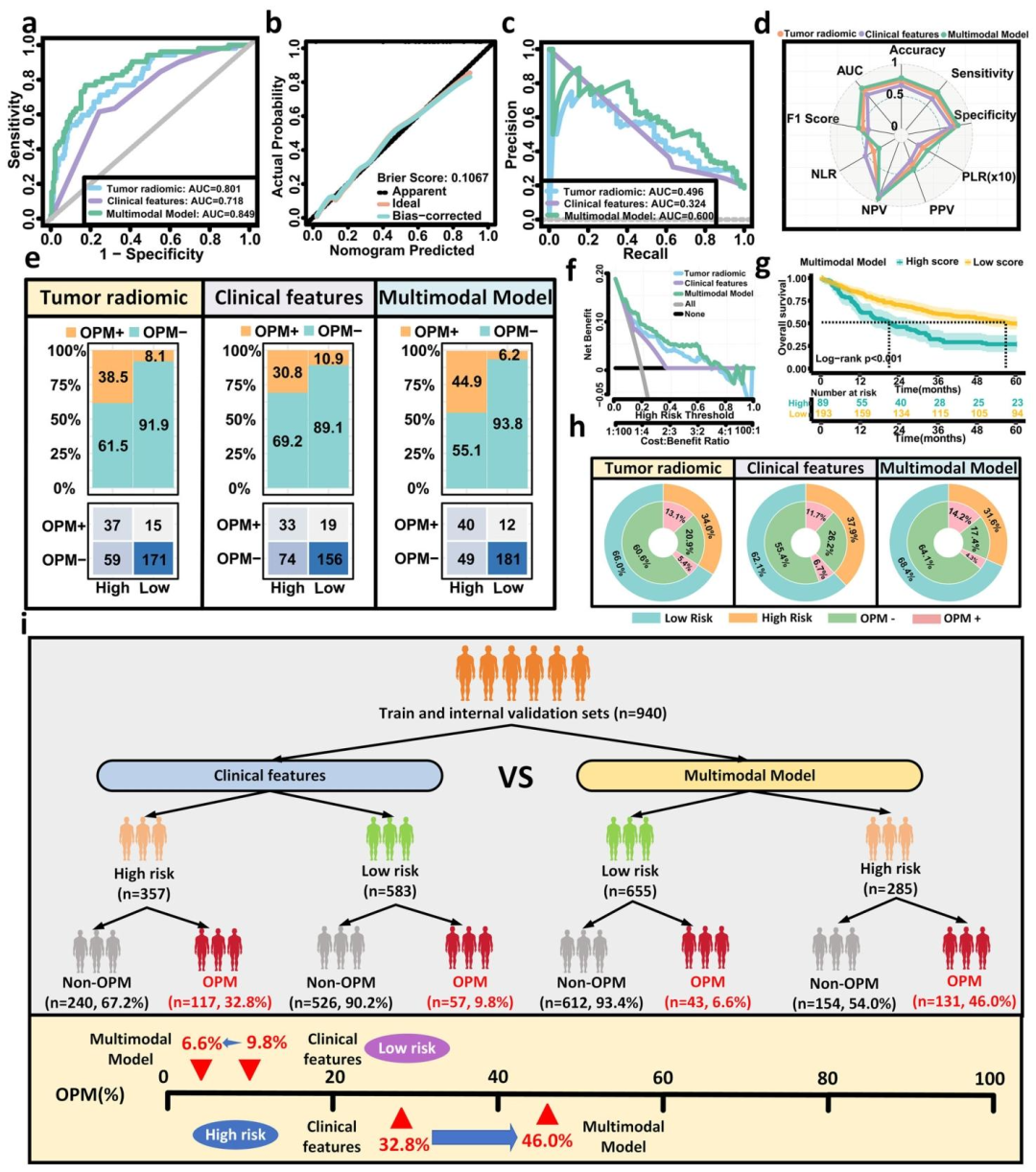
图 2:多模态模型在内部验证集的预测性能
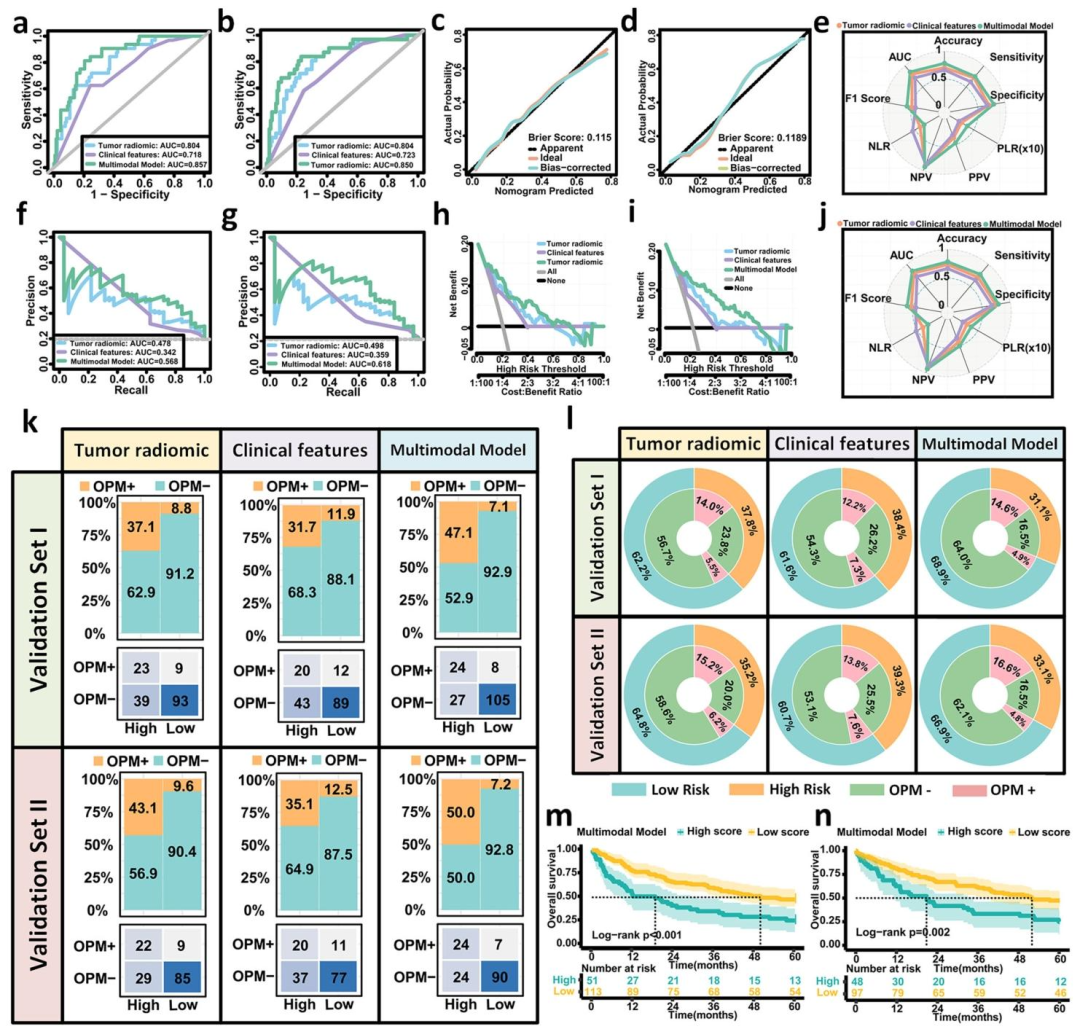
图 3:多模态模型在多中心外部验证集的预测性能
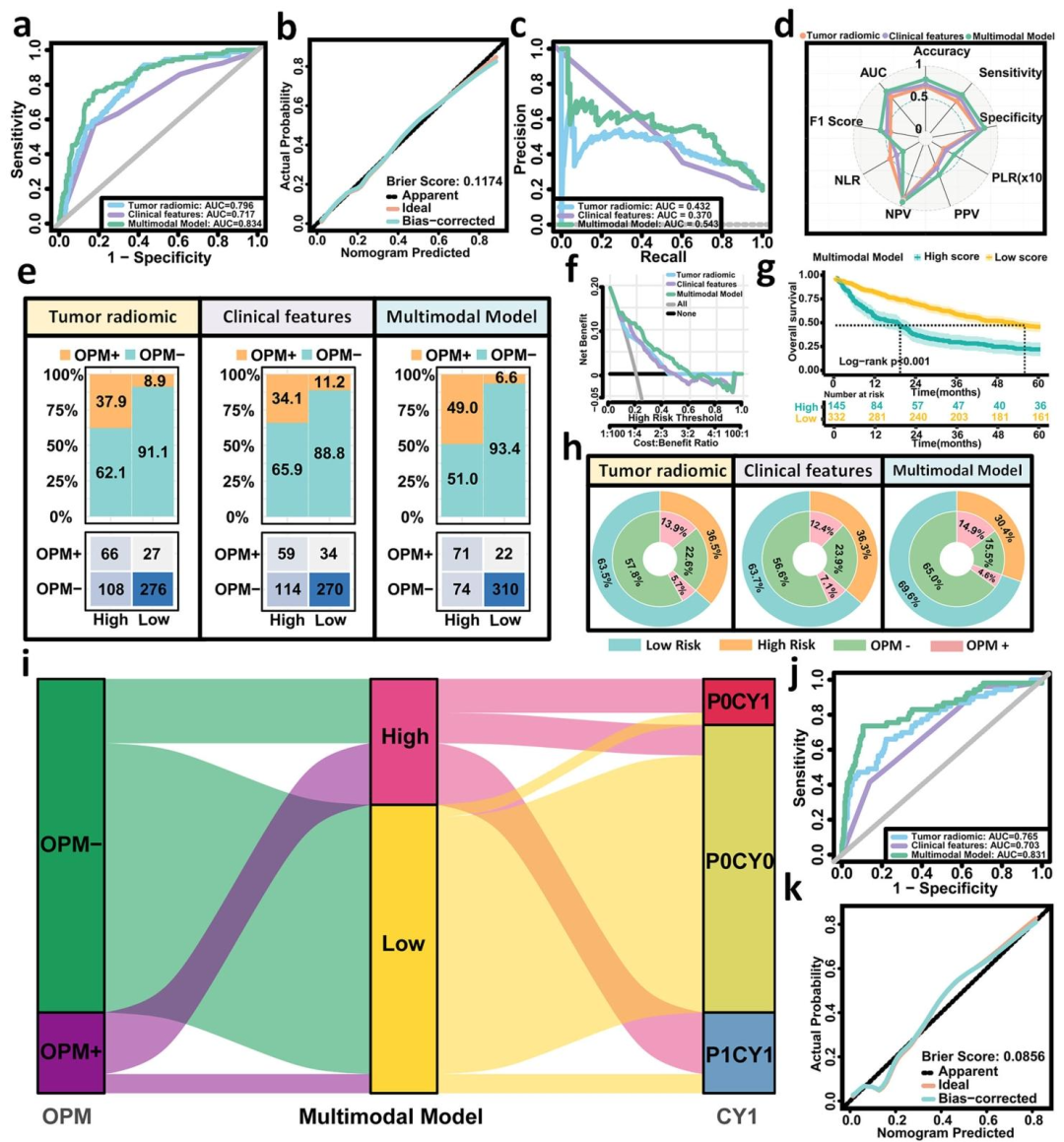
图 4:增量队列验证:多模态模型预测OPM与腹腔灌洗细胞学状态
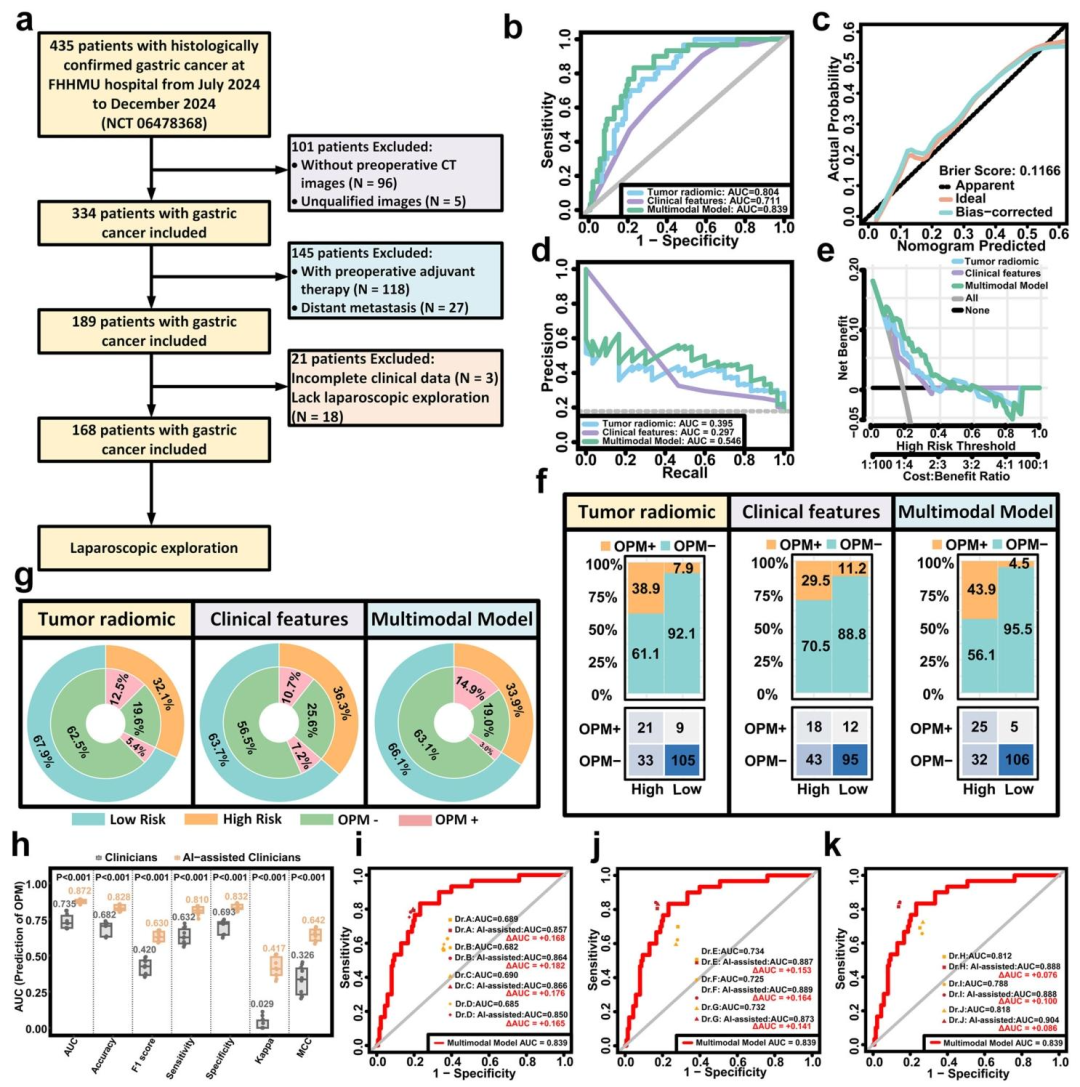
图 5:前瞻性队列验证与医生辅助效能评估
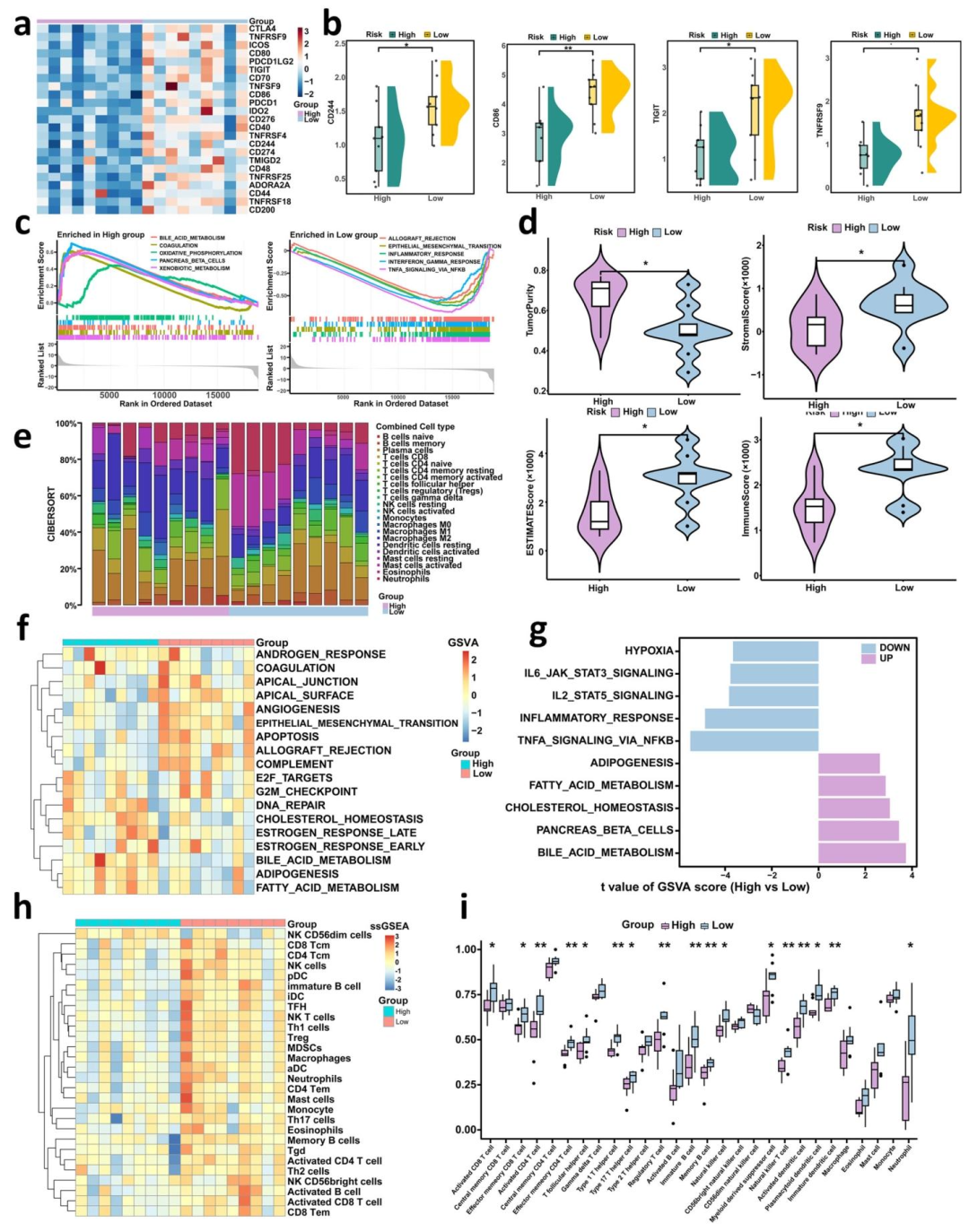
图 6:多模态模型高低风险组的转录组与免疫微环境差异
05
研究结论
该研究成功开发并验证了一种多模态数字活检模型 ,通过整合CT原发肿瘤放射组学特征 与关键临床变量(如cT分期、组织学类型、Borrmann分型),可无创、精准地预测局部晚期胃癌患者的隐匿性腹膜转移 。模型在训练、内部验证、多中心外部验证、增量及前瞻性临床试验等多个队列中均表现稳健,AUC达0.834-0.857 ,显著优于单一模态模型。AI辅助可将放射科医生平均AUC从0.735提升至0.872 ,有效降低诊断差异。模型风险分层与患者预后显著相关:低风险组5年总生存率约47-48%,高风险组仅约25-27%。转录组分析进一步揭示,低风险组肿瘤呈现增强的抗肿瘤免疫微环境(如CD8+ T细胞富集、TNFα/NF-κB及IL2/STAT5信号通路上调),而高风险组则表现为免疫抑制特征。该模型作为可解释的"数字活检"工具,不仅可优化分期腹腔镜的患者选择,还能指导个体化治疗策略(低风险直接手术、高风险优先新辅助治疗或CRS/HIPEC),具有重要的临床转化价值。
参考文献:Chen S, Ding P, Yang Y, Ma S, Guo H, Han X, Yang J, Ma W, Meng N, Xia Z, Li X, Zhang L, Shi Y, Guo Z, Gao K, Gu R, Long H, Meng L, Zhao Q. Multimodal digital biopsy for preoperative prediction of occult peritoneal metastasis in gastric cancer. NPJ Digit Med. 2026 Jan 26;9(1):107. doi: 10.1038/s41746-025-02268-9.