01
文献学习

今天分享的文献是由复旦大学肿瘤医院顾雅佳、龚敬团队联合复旦大学附属中山医院叶晓丹等团队于2026年3月31日在肿瘤学领域顶刊《npj Precision Oncology 》(中科院1区top,IF=8)上发表的研究"Habitat-based CT radiomics profiling spatial-temporal heterogeneity in resectable NSCLC predict pathological response to neoadjuvant chemoimmunotherapy: a multi-center study "即基于生境CT放射组学剖析可切除非小细胞肺癌的时空异质性以预测新辅助化疗免疫治疗的病理缓解:一项多中心研究,该研究开发并验证了一种基于CT影像的"生境成像"框架,用于预测可切除非小细胞肺癌患者对新辅助化疗免疫治疗的病理响应。通过将肿瘤分割为多个生物学上不同的"生境"亚区,提取空间异质性特征、全肿瘤纹理特征及治疗前后动态变化特征,构建了三个预测模型(ITH、WTH、WITH)。WITH模型在多个独立验证队列中表现最佳,AUC最高达0.85,显示出良好的预测能力和临床实用性。
创新点:①提出"生境影像"框架 ,通过分割肿瘤内生物学亚区域,量化空间异质性 ,突破传统全局纹理分析局限。②构建MSI空间互作矩阵 ,显式编码不同生境间的拓扑关系 ,捕捉肿瘤宏观结构信息。③整合空间、全局与时间维度 ,建立WITH联合模型,预测性能优于单一模型(AUC达0.85)。
临床价值:①无创预测新辅助化疗免疫治疗的主要病理缓解 ,指导个体化新辅助治疗策略制定。②识别非响应者并建议早期手术 ,避免无效治疗导致的纤维化与手术风险增加。③多中心外部验证泛化能力强 ,支持临床推广,实现精准患者分层与决策优化。
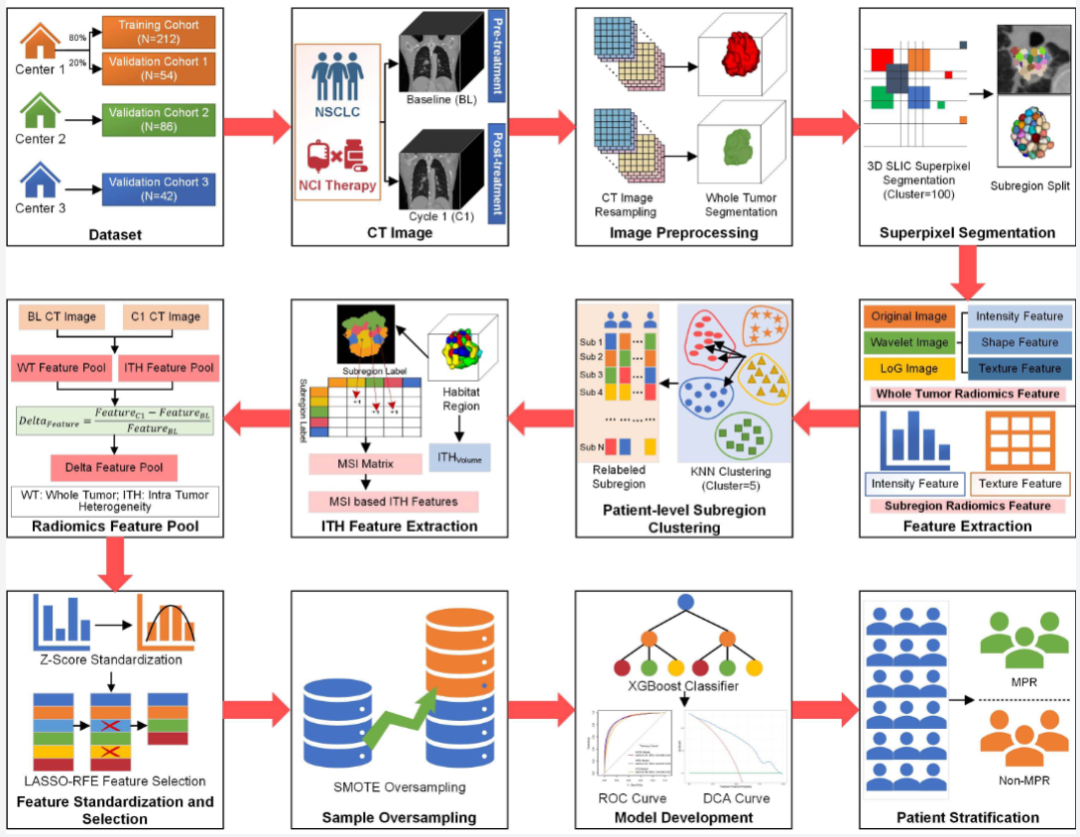
图 2:生境成像框架工作流程图
左侧:影像获取与肿瘤分割
输入:**治疗前(BL)+治疗后(C1)**胸部增强CT
处理:放射科医生用ITK-SNAP手动勾画全肿瘤体积(VOI)
标准化:体素重采样至1×1×1mm³,统一图像分辨率
中间:栖息地亚区分割与聚类
超像素分割:用SLIC算法将肿瘤拆分为100个亚区
无监督聚类:K-means聚类(k=5,轮廓系数最优),将亚区归为不同影像表型栖息地
右侧:特征提取→建模→预测输出
特征提取(三大类)
ITH特征:基于多区域空间交互(MSI)矩阵,量化栖息地空间拓扑与交互
WTH特征:全肿瘤全局纹理、强度、形态特征
Delta特征:治疗前后特征变化率,捕捉时空动态异质性
数据处理:Z-score标准化→LASSO-RFE特征筛选→SMOTE过采样平衡数据
模型构建:XGBoost分类器训练**ITH、WTH、WITH(整合)**三大模型
输出:MPR/非MPR预测概率→患者危险分层→临床决策
02
研究背景和目的
研究背景
尽管新辅助化疗免疫疗法(Neoadjuvant Chemoimmunotherapy, NCI)显著改善了可切除非小细胞肺癌(Non-Small Cell Lung Cancer, NSCLC)患者的病理缓解率(主要病理缓解率MPR可达86.0%),但不同患者对治疗的响应存在巨大的个体差异 ,其根本原因在于肿瘤内部存在深刻的时空异质性 。这种异质性不仅体现在基因水平,更表现为肿瘤微环境中不同区域在病理生理状态和微环境条件上的非均匀空间分布 。传统的影像组学方法(如全肿瘤纹理分析)往往将肿瘤视为一个统计整体,只能捕捉整体变异程度,而无法揭示肿瘤内部亚区域之间的空间拓扑关系 。此外,现有研究缺乏能够无创、动态监测治疗前后肿瘤异质性演变的可靠生物标志物,导致临床上难以精准筛选潜在获益人群,也难以及时识别耐药患者。因此,亟需开发一种能够解码肿瘤时空异质性的新型影像学方法,以填补当前NCI疗效预测领域的空白,并为个体化治疗决策提供依据。
研究目的
本研究旨在验证基于生境(Habitat)的CT影像组学方法 在预测可切除NSCLC患者新辅助化疗免疫治疗后的主要病理缓解(MPR) 方面的效能。具体目标包括:1)通过整合治疗前后的CT影像 ,构建一个融合全局纹理特征、空间异质性特征和纵向变化特征 的预测框架;2)比较全肿瘤异质性(WTH)模型 、瘤内空间异质性(ITH)模型 以及两者决策级融合(WITH)模型 的预测性能;3)评估该模型在不同临床亚组(如年龄、吸烟史、病理类型、肿瘤分期)中的稳健性,并探索其临床转化价值。研究通过多中心394例患者的数据验证,旨在证明空间拓扑信息是对全肿瘤纹理信息的补充 ,两者结合能更全面地刻画治疗敏感性,从而为临床提供一种无创、精准的患者分层工具,优化新辅助治疗策略(如继续治疗或早期手术)。
03
数据和方法
研究数据
总样本量:394例可切除NSCLC患者
数据来源:三家中国医疗机构
中心1(上海肺科医院):266例 → 训练集(212例)+ 内部验证集(54例)
中心2(复旦肿瘤医院):86例 → 外部验证集2
中心3(中山医院):42例 → 外部验证集3
数据内容:治疗前、后增强CT影像 + 病理缓解结果(MPR vs. non-MPR)
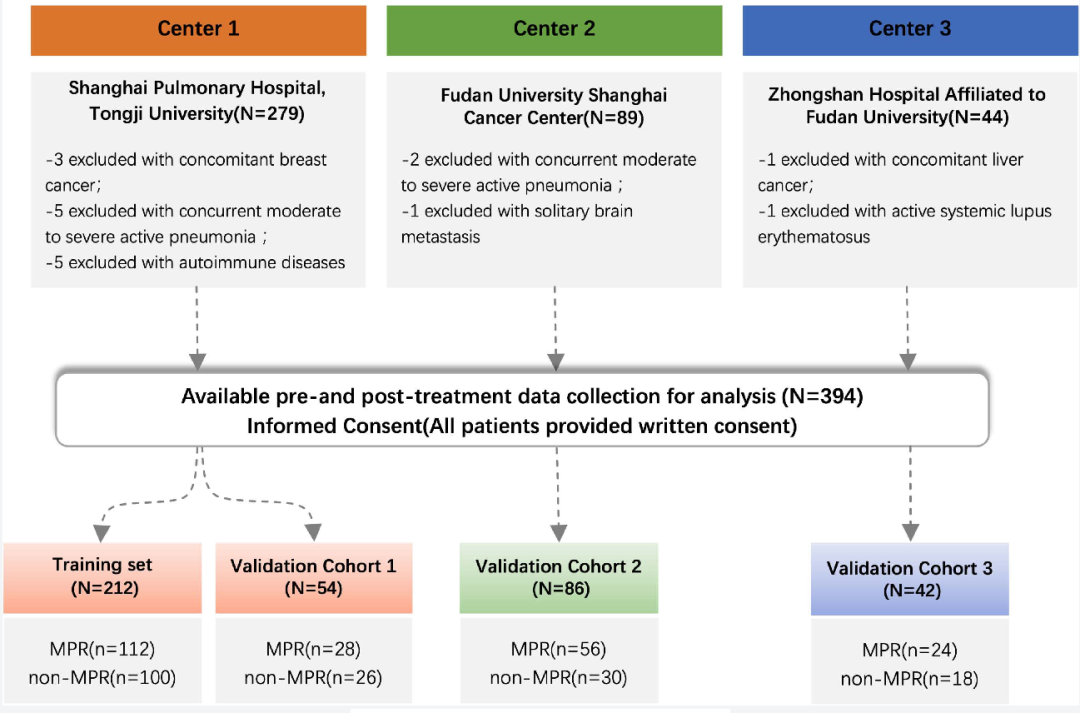
图 1:患者筛选流程图
技术方法
肿瘤分割:手工勾画肿瘤体积(VOI)
生境划分:SLIC超像素+ K-means聚类(k=5)
特征提取:
ITH特征:基于多区域空间交互矩阵(25个特征)
WTH特征:全肿瘤放射组学(1106个特征)
Delta特征:治疗前后变化
特征选择:RFE + LASSO
类别平衡:SMOTE
模型构建:XGBoost
模型融合:决策级融合 → WITH模型
评估指标:AUC、准确率、敏感度、特异度、决策曲线分析
04
实验结果
ITH模型:AUC在验证集中为 0.71--0.80
WTH模型:AUC在验证集中为 0.73--0.80
WITH模型(融合) :AUC在验证集中为 0.75--0.85,训练集AUC = 0.91
WITH模型在所有验证队列中均优于单一模型
DCA显示WITH模型具有更高的临床净收益
亚组分析显示:鳞癌、中央型、T3-4/N2-3患者预测效果更好
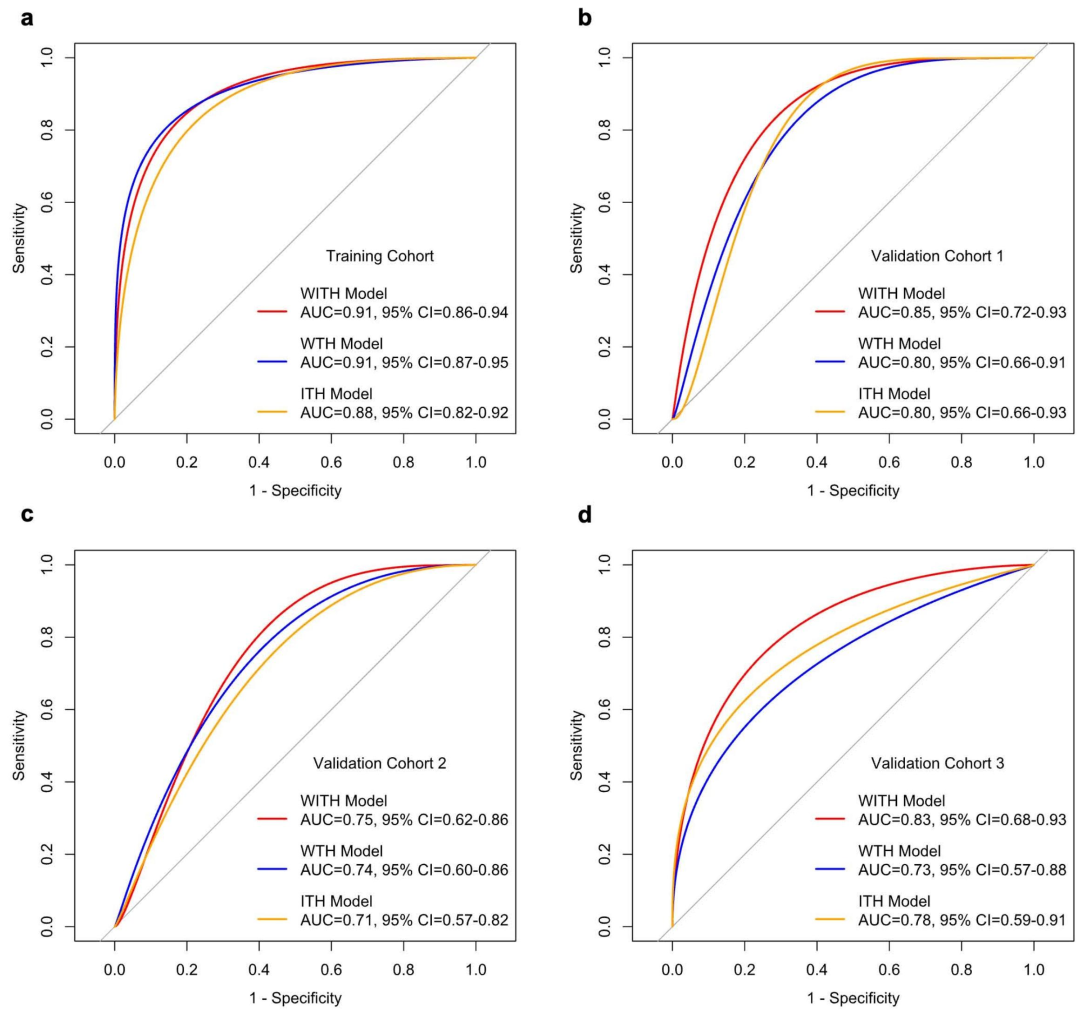
图 3:各队列模型效能对比(ROC曲线)
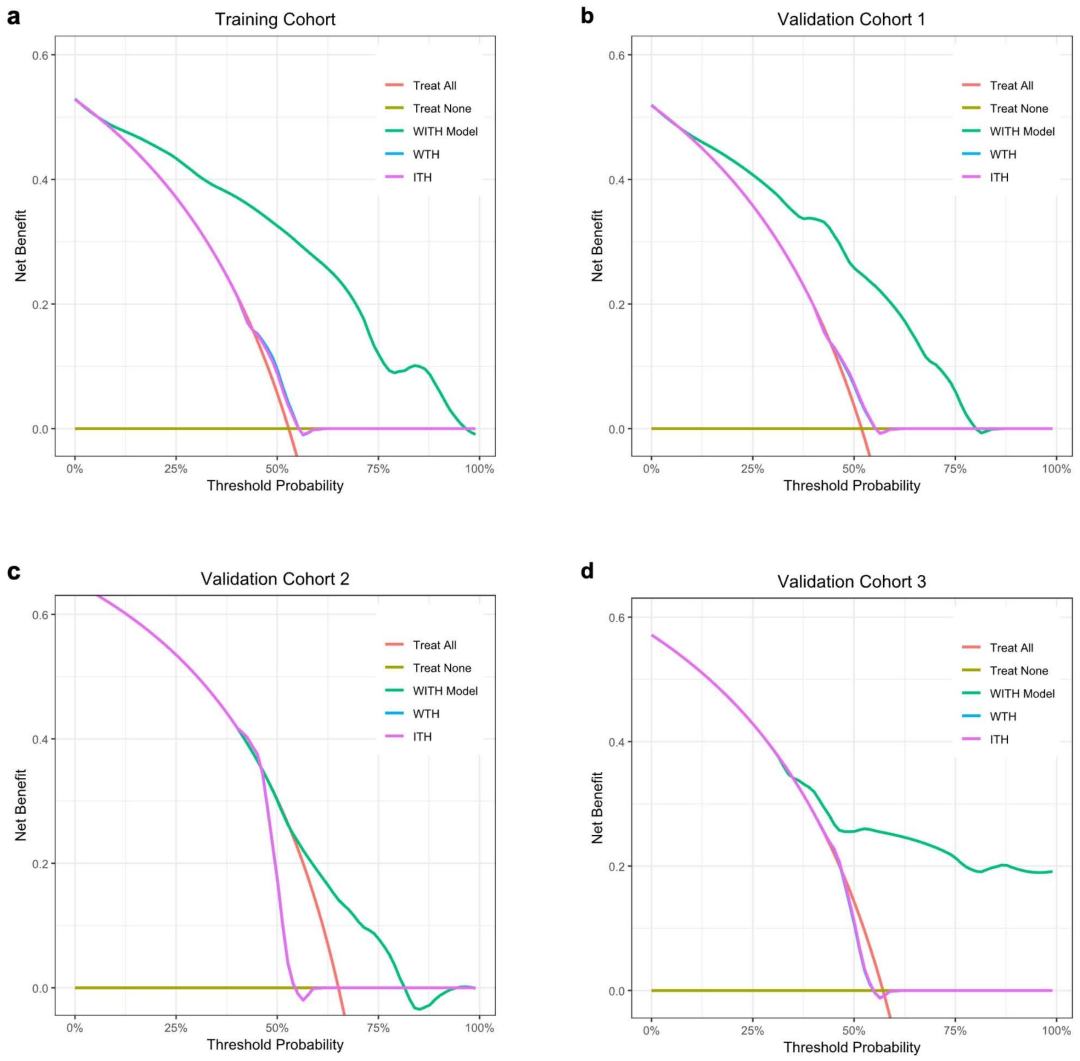
图 4:各队列决策曲线分析(DCA)
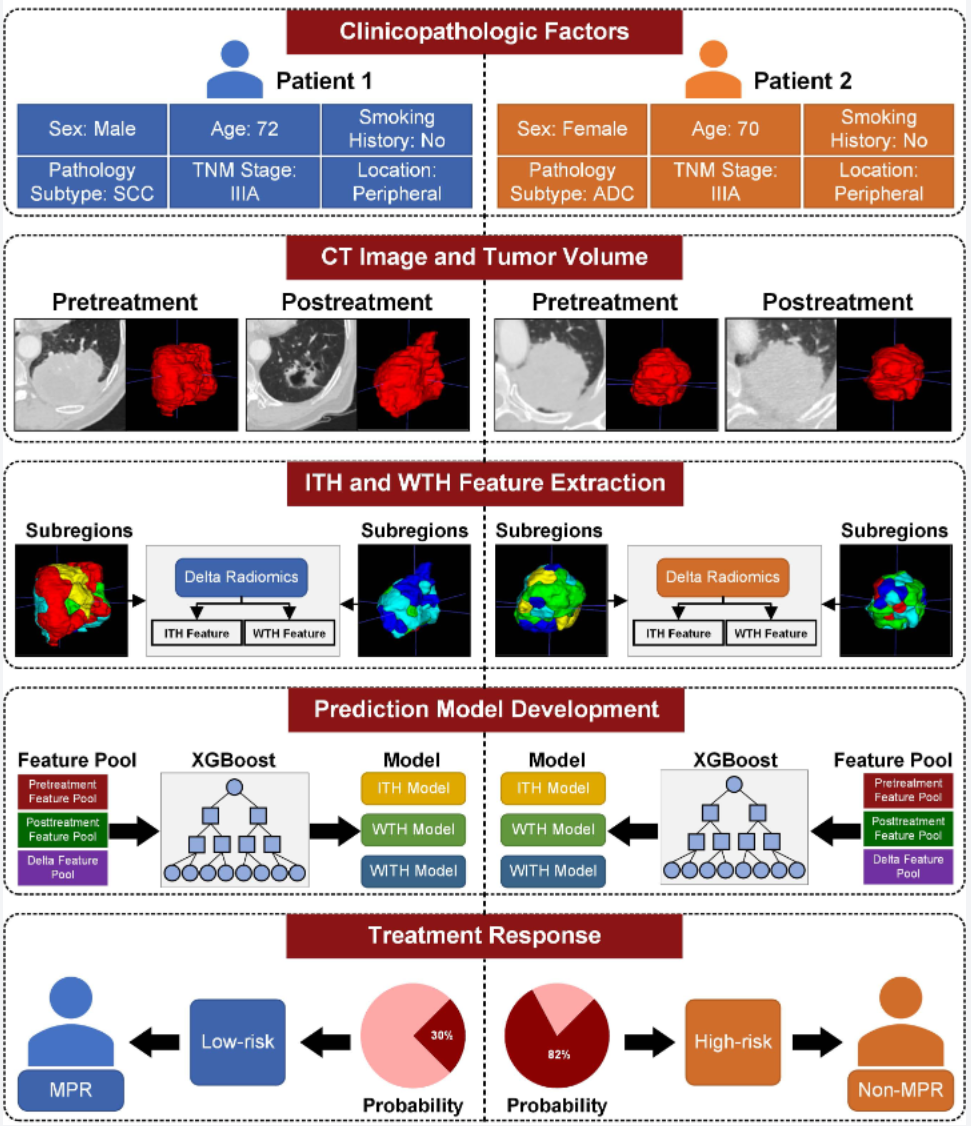
图 5:瘤内空间异质性代表性案例
05
研究结论
该多中心研究证实,基于生境成像 的CT放射组学框架能够有效解码可切除非小细胞肺癌(NSCLC)在新辅助化疗免疫治疗(NCI)中的时空异质性 ,从而精准预测主要病理缓解(MPR)。研究通过整合全局纹理特征 、瘤内空间拓扑特征 及纵向影像变化 ,构建了预测模型(WITH)。结果显示,单独使用全局纹理或空间异质性模型在验证队列中的AUC为0.71-0.80,而整合模型在外部验证中AUC提升至0.85 ,显著提高了鉴别能力。关键发现是:治疗敏感性不仅取决于肿瘤异质性的强度 ,更取决于其空间组织方式 ------即不同生物学"生境"的分布与相互作用。该框架通过多区域空间互作矩阵量化了宏观结构特征,弥补了传统整体纹理分析忽视空间拓扑的缺陷。尽管在伴有明显瘤周炎症、纤维化或磨玻璃成分的病变中存在一定局限性,但研究结论表明,生境成像可作为无创、可推广的生物标志物,助力患者分层、优化治疗决策(如预测响应者继续治疗、非响应者尽早手术),推动个体化精准医疗。
参考文献:Peng Q, Xu Y, Shen L, Bao X, Zhou S, Ye X, Gu Y, Gong J. Habitat-based CT radiomics profiling spatial-temporal heterogeneity in resectable NSCLC predict pathological response to neoadjuvant chemoimmunotherapy: a multi-center study. NPJ Precis Oncol. 2026 Mar 31. doi: 10.1038/s41698-026-01388-z.