在生物制药与免疫治疗的技术领域,靶点的选择与机制解析是药物研发的基石。CD37(TSPAN26)作为四跨膜蛋白超家族(TSPAN)的重要成员,凭借其在B细胞谱系中的特异性表达及独特的双向信号调控功能,已成为当前抗体药物研发的热点。本文将从生物信息学与分子生物学角度,深度剖析CD37的结构特征、信号通路机制及药物开发的技术挑战,为相关领域的技术人员提供参考。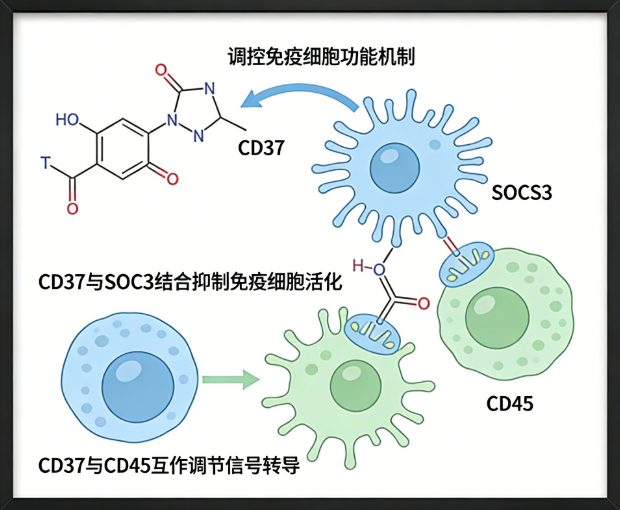
结构特征:四跨膜蛋白的拓扑学基础
CD37(TSPAN26)是由281个氨基酸组成的四跨膜糖蛋白,定位于人类染色体19q13.33。从结构生物学角度看,其核心特征包含4个跨膜结构域(TM1-TM4)、1个短胞内N端、1个长胞内C端,以及胞外保守的CCG基序(Cys-Cys-Gly)。
CCG基序是四跨膜蛋白家族的标志性结构,负责介导蛋白与蛋白、蛋白与脂质的相互作用,组装膜微结构域(TEM)。与CD9、CD81等广泛表达的家族成员不同,CD37具有高度的细胞谱系特异性,主要表达于成熟B细胞表面,在T细胞及髓系细胞中表达极低。这种独特的拓扑结构与表达模式,为靶向药物的设计提供了良好的安全窗口。
信号机制:ITIM与ITAM的双向博弈
CD37的核心生物学功能在于其双向信号调控能力,这种调控依赖于胞内不同酪氨酸基序的磷酸化状态。在技术实现上,CD37通过N端与C端的拮抗作用,介导细胞存活或凋亡信号:
- 抑制性信号(ITIM):胞内N端含有免疫酪氨酸抑制基序(ITIM)。当被Src家族激酶磷酸化后,会招募SHP1、SHP2等含SH2结构域的磷酸酶,进而诱导异常细胞凋亡,发挥负向调控作用。
- 激活性信号(ITAM):胞内C端含有免疫酪氨酸激活基序(ITAM)。当ITAM被激活时,会启动PI3K/Akt、MAPK等经典信号通路,促进正常B细胞与巨噬细胞的存活与增殖。
此外,CD37还参与调控免疫微环境,通过与SOCS3、CD45等分子相互作用,抑制IL-6/STAT3通路的异常激活,并作为巨噬细胞的"吞噬检查点",与CD47协同适度抑制吞噬功能,维持免疫稳态。
药物开发:单抗与ADC的技术路径
基于上述机制,靶向CD37的抗体药物开发已形成清晰的技术路径,主要分为单克隆抗体(mAb)与抗体偶联药物(ADC)两大类:
1. 单克隆抗体技术
目前的单抗药物主要分为激动型与拮抗型。
- 拮抗型:通过竞争性结合CD37胞外区,阻断其与配体的结合,解除异常的信号调控。
- 激动型 :旨在激活CD37的ITIM基序,诱导目标细胞凋亡。
两类药物均利用抗体的Fc段触发ADCC(抗体依赖性细胞介导的细胞毒作用)和ADCP(抗体依赖性细胞吞噬作用),招募NK细胞或巨噬细胞进行清除。
2. ADC药物技术
代表性药物如那妥昔单抗偶联物(Naratuximab emtansine),采用人源化抗CD37单抗与细胞毒性物质通过可切割连接子偶联。其技术难点在于连接子的稳定性设计:需确保在血液循环中稳定,而在进入胞内溶酶体的酸性环境下被精准切割,释放毒性载荷,从而在提升疗效的同时降低脱靶毒性。
未来趋势:技术迭代与精准化挑战
结合当前生物制药技术的发展,CD37靶点的研发正面临从"通用型"向"精准化"的技术迭代:
- 分子工程优化:利用抗体人源化改造与亲和力成熟技术,提升抗体对CD37的特异性与结合力,减少免疫原性。
- 联合治疗策略:探索CD37药物与其他免疫调节药物的协同机制,通过多靶点干预提升整体治疗效率。
- 诊断伴随技术:开发高灵敏度的CD37检测试剂,结合流式细胞术与免疫组化技术,实现患者的精准分层与疗效监测。