01
文献学习

今天分享的文献是由云南省肿瘤医院李振辉团队联合广东省人民医院、广州医科大学附属肿瘤医院等多家团队于2025年8月在肿瘤免疫领域顶刊《Journal for ImmunoTherapy of Cancer》(中科院1区top,IF14.1)上发表的研究"Immunophenotype-guided interpretable radiomics model for predicting neoadjuvant anti-PD-1 response in stage III--IV d-MMR/MSI-H colorectal cancer"即免疫表型引导的可解释放射组学模型预测III-IV期d-MMR/MSI-H结直肠癌新辅助抗PD-1治疗反应,该研究构建并验证了一个免疫表型(免疫热型 vs. 免疫冷型)引导的放射组学模型,用于预测III--IV期d-MMR/MSI-H结直肠癌患者对新辅助抗PD-1免疫治疗的反应。模型基于CT影像提取的放射组学特征,结合免疫表型信息,实现了高精度与高可解释性的预测。
创新点:①免疫表型指导特征筛选 :首次结合免疫热/冷表型与影像组学,通过RNA与IHC双重验证,实现生物学指导的影像特征选择。②可解释性决策树模型 :构建基于决策树与SHAP分析的预测模型,明确关键影像特征贡献,提升模型临床可信度。③多中心免疫影像关联验证:通过多中心数据验证免疫表型与CT特征的强关联,增强模型生物学基础与跨中心适用性。
临床价值:①非侵入性疗效预测工具 :提供基于术前CT的模型,无创预测免疫治疗疗效,辅助临床决策,避免无效治疗。②助力个体化治疗策略 :通过区分免疫表型与影像特征,为d-MMR/MSI-H结直肠癌患者提供分层治疗依据,提升治疗精准性。③推动影像组学临床转化:模型具有高准确性(AUC 0.904)与强解释性,为影像组学在免疫治疗中的应用提供可行框架。
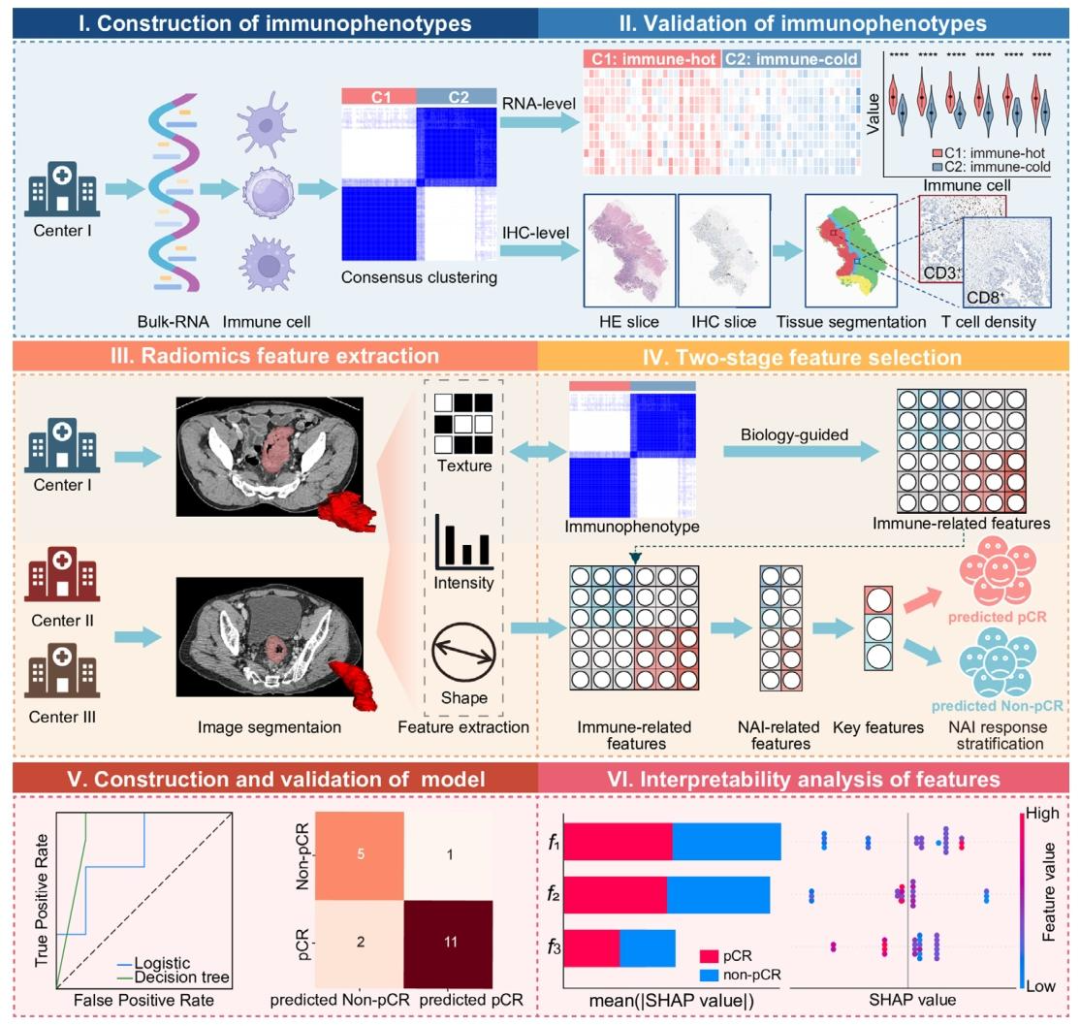
图 1:研究工作流程图
免疫表型构建(I):基于中心I患者的批量RNA测序数据,通过共识聚类分析肿瘤浸润免疫细胞,划分免疫表型。
免疫表型验证(II):从两个维度验证------RNA水平量化28种免疫细胞丰度;IHC水平通过HE切片、IHC切片的组织分割,检测CD3、CD8 T细胞密度。
放射组学特征提取(III):针对中心II(训练集)、中心III(验证集)患者的CT影像,进行图像分割后提取特征,涵盖纹理、强度、形状等类型。
两阶段特征选择(IV):先筛选与免疫表型相关的特征,再进一步筛选与新辅助免疫治疗(NAI)反应相关的关键特征。
模型构建与验证(V):基于关键特征构建预测模型,分别在训练集和验证集评估性能,区分pCR(病理完全缓解)和非pCR患者。
特征可解释性分析(VI):通过SHAP分析量化各特征对模型预测结果的贡献度。
02
研究背景及目的
研究背景
结直肠癌(CRC)是全球第三大常见恶性肿瘤,约70%的患者确诊时已处于晚期。传统术前治疗(如化疗、放疗等)虽能一定程度上控制疾病,但其病理完全缓解(pCR)率仍较低(6.5%--35%)。其中,错配修复缺陷/微卫星高度不稳定(d-MMR/MSI-H) 是CRC的一个重要分子亚型,约占全部病例的15%。该亚型虽在晚期预后较差,但对免疫检查点抑制剂(ICIs)反应良好 ,尤其是在新辅助治疗中,pCR率可达60%--100%。然而,由于肿瘤异质性和免疫微环境的复杂性,仍有一部分患者对ICIs治疗无反应。因此,亟需开发一种精准、高效的方法来预测术前免疫治疗的反应,以优化个体化治疗策略。
计算机断层扫描(CT)广泛用于CRC的诊疗,但其在评估免疫治疗反应时存在局限性,例如治疗反应延迟、假性进展等现象。放射组学 通过从常规医学影像中高通量提取定量特征(如纹理、形状、强度),能够表征肿瘤表型,提升诊断、预后及治疗反应预测的准确性。近年来,放射组学在预测新辅助治疗疗效方面取得进展,但现有模型大多缺乏与生物学信息的整合 ,导致其可解释性和临床相关性不足。研究表明,将放射组学与免疫特征等生物学信息结合,能显著增强模型的生物学意义和临床价值。因此,开发一种基于免疫表型指导的、可解释的放射组学模型,以非侵入性方式预测d-MMR/MSI-H CRC患者对新辅助免疫治疗的反应,具有重要的临床转化潜力。
研究目的
本研究旨在构建并验证一个由免疫表型指导的可解释放射组学模型 ,用于预测III--IV期d-MMR/MSI-H结直肠癌患者对新辅助抗PD-1免疫治疗的反应,以推动临床精准医疗的实现。具体目标包括:首先,通过RNA测序数据对肿瘤浸润免疫细胞进行无监督聚类,鉴定出具有不同免疫特征的亚型(如"免疫热"和"免疫冷"表型) ,并在免疫组织化学(IHC)水平通过CD3和CD8 T细胞的空间分布进行验证,以确立其生物学稳健性。其次,基于这些免疫表型,从治疗前CT影像中筛选出与免疫特征及治疗反应相关的关键放射组学特征 ,并采用两阶段特征选择方法(包括秩和检验与弹性网逻辑回归)进行优化。最终,利用决策树算法构建预测模型,并结合SHapley Additive exPlanations(SHAP)分析增强模型的可解释性,明确各特征对预测结果的贡献度。
该研究的目标不仅是实现高精度的预测(在独立验证队列中AUC目标≥0.85),更强调模型的临床可解释性与生物学意义 ,旨在揭示影像特征与肿瘤免疫微环境之间的关联。通过多中心数据验证,研究期望提供一个稳健、非侵入性且易于整合到临床工作流程中的决策支持工具,从而帮助临床医生在治疗前更准确地识别可能从新辅助免疫治疗中获益的患者,优化个体化治疗策略,减少不必要的治疗毒性,推动免疫治疗在结直肠癌中的精准应用。
03
数据和方法
研究数据
数据来源:3个多中心回顾性队列
中心I(2015.01-2017.11):108例接受术前增强CT扫描和批量RNA测序的CRC患者,用于免疫表型的构建与验证,其中87例有可用IHC切片(CD3、CD8染色)。
中心II(2019.12-2022.07):19例接受新辅助抗PD-1治疗前增强CT扫描的CRC患者,作为模型训练集(pCR13例,占68.42%)。
中心III(2019.12-2022.07):22例同类型患者,作为模型独立验证集(pCR14例,占63.63%)。
数据类型:临床病理数据(肿瘤分期、MSI状态等)、CT影像数据(腹盆腔增强扫描)、RNA测序数据(28种免疫细胞丰度量化)、IHC数据(CD3、CD8 T细胞密度)。
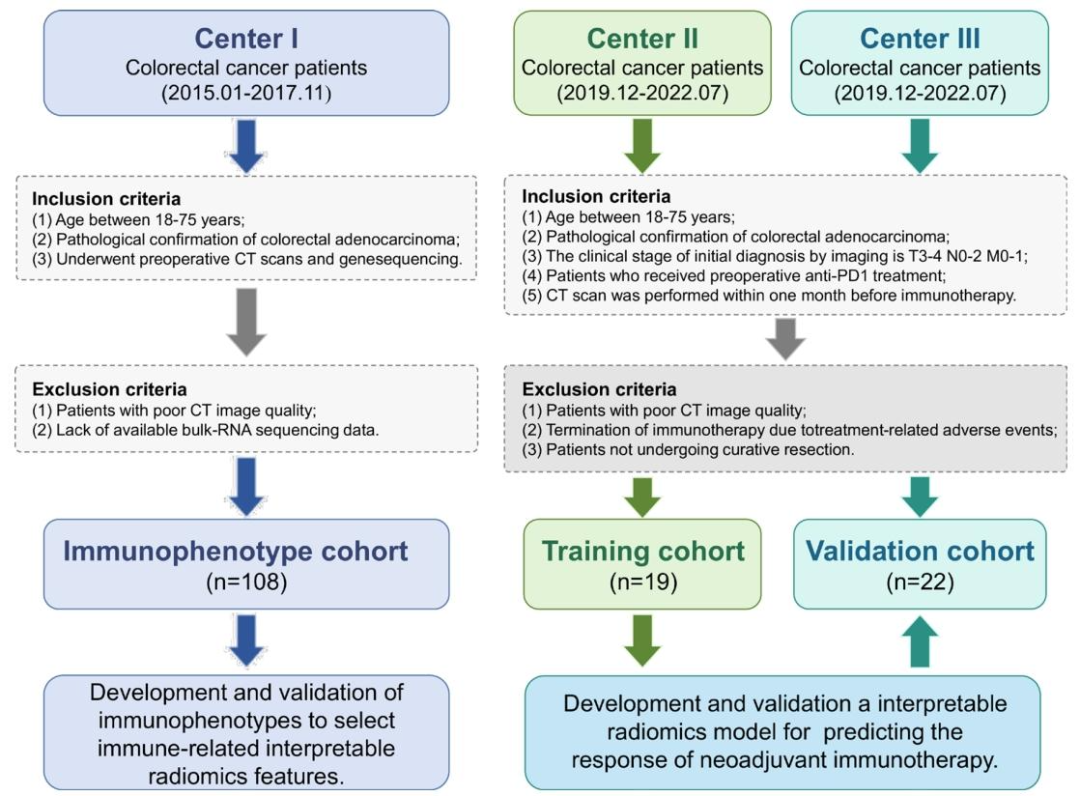
图 2:患者纳入与排除标准流程图
技术方法
(1)免疫表型构建与验证
采用单样本基因集富集分析(ssGSEA)量化28种免疫细胞的相对丰度;
通过共识聚类算法(k-means,k=2)进行无监督聚类,识别免疫表型;
利用IHC染色验证CD3、CD8 T细胞在肿瘤核心区和浸润边缘区的密度分布,确认免疫表型稳定性;
针对III-IV期亚组患者(n=52)重复聚类分析,验证表型泛化性。
(2)CT影像预处理与放射组学特征提取
由10年经验胃肠放射科医生使用ITK-SNAP软件手动勾勒肿瘤轮廓(仅保留原发肿瘤,排除转移灶);
采用PyRadiomics包提取944个放射组学特征(包括一阶特征、形状特征、强度特征、纹理特征);
通过组内相关系数(ICC)分析筛选稳定特征(ICC>0.75),最终保留693个特征。
(3)特征选择与数据预处理
第一阶段:秩和检验筛选与免疫表型相关的特征(p<0.05),得到100个免疫相关放射组学特征;
数据harmonization:采用ComBat校正批量效应,Z-score标准化;
第二阶段:Mann-Whitney U检验筛选与新辅助免疫治疗反应相关的特征(p<0.05),再通过弹性网逻辑回归(10折交叉验证优化参数)筛选关键特征,最终保留3个核心特征。
(4)模型构建与验证
构建两种预测模型:决策树模型和多变量逻辑回归模型;
以病理完全缓解(TRG 0级定义为pCR,TRG1-3级为非pCR)为结局指标;
采用ROC曲线、准确率、灵敏度、特异度、F1分数评估模型性能;
决策树模型参数优化:Gini指数为分裂准则,最大特征数=3,最大树深=3(平衡可解释性与泛化性)。
(5)模型可解释性分析
采用SHAP分析量化每个核心特征对模型预测结果的贡献度;
可视化特征与pCR的关联(如LargeDependenceEmphasis、方差特征的生物学意义)。
(6)统计分析
连续变量比较采用Mann-Whitney U检验,分类变量采用χ²检验;
统计软件为R4.3.2,p<0.05为差异有统计学意义。
04
实验结果
(1)免疫表型识别与验证
成功识别两种免疫表型:"免疫热型"(C1)和"免疫冷型"(C2);
免疫热型在RNA水平富集活化B细胞、活化CD8 T细胞等免疫效应细胞,IHC验证显示其肿瘤核心区和浸润边缘区的CD3、CD8T细胞密度显著高于免疫冷型(CD3CT:p=0.013;CD8CT:p=0.005);
III-IV期亚组患者的聚类模式与总队列一致,亚型分类完全吻合(免疫热型23例,免疫冷型29例),证明表型稳健性。
(2)放射组学特征筛选与模型性能
经两阶段筛选,最终确定3个关键特征:wavelet.LLH_gldm_LargeDependenceEmphasis、wavelet.HHH_firstorder_Variance、wavelet.LHH_firstorder_Variance;
决策树模型性能优于逻辑回归模型:
训练集(中心II):AUC=0.965(95% CI:0.900-1.000);
验证集(中心III):AUC=0.904(95% CI:0.679-1.000);
逻辑回归模型验证集AUC仅为0.782(95% CI:0.500-0.986)。
(3)模型可解释性(SHAP分析)
wavelet.LLH_gldm_LargeDependenceEmphasis对预测贡献最大(反映影像灰度值的大范围依赖关系,高值提示肿瘤纹理更均匀);
方差特征(wavelet.HHH_firstorder_Variance、wavelet.LHH_firstorder_Variance)高值提示肿瘤异质性增加,与较差的治疗反应相关;
高LargeDependenceEmphasis值+低方差值是pCR的潜在预测因子,量化了肿瘤同质性。
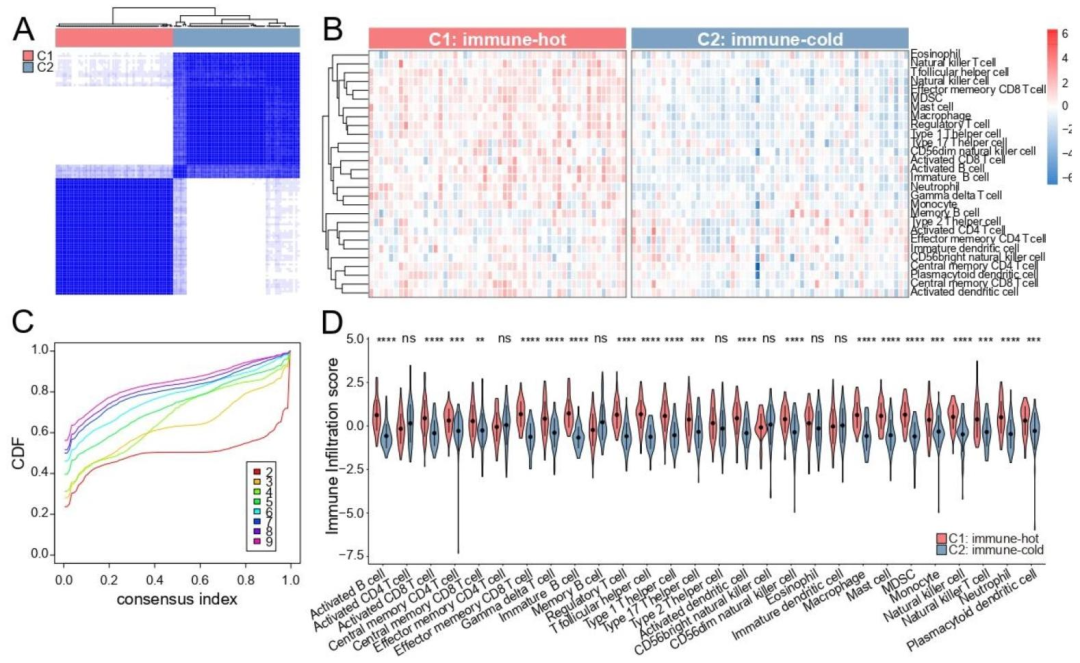
图 3:免疫表型的开发与评估
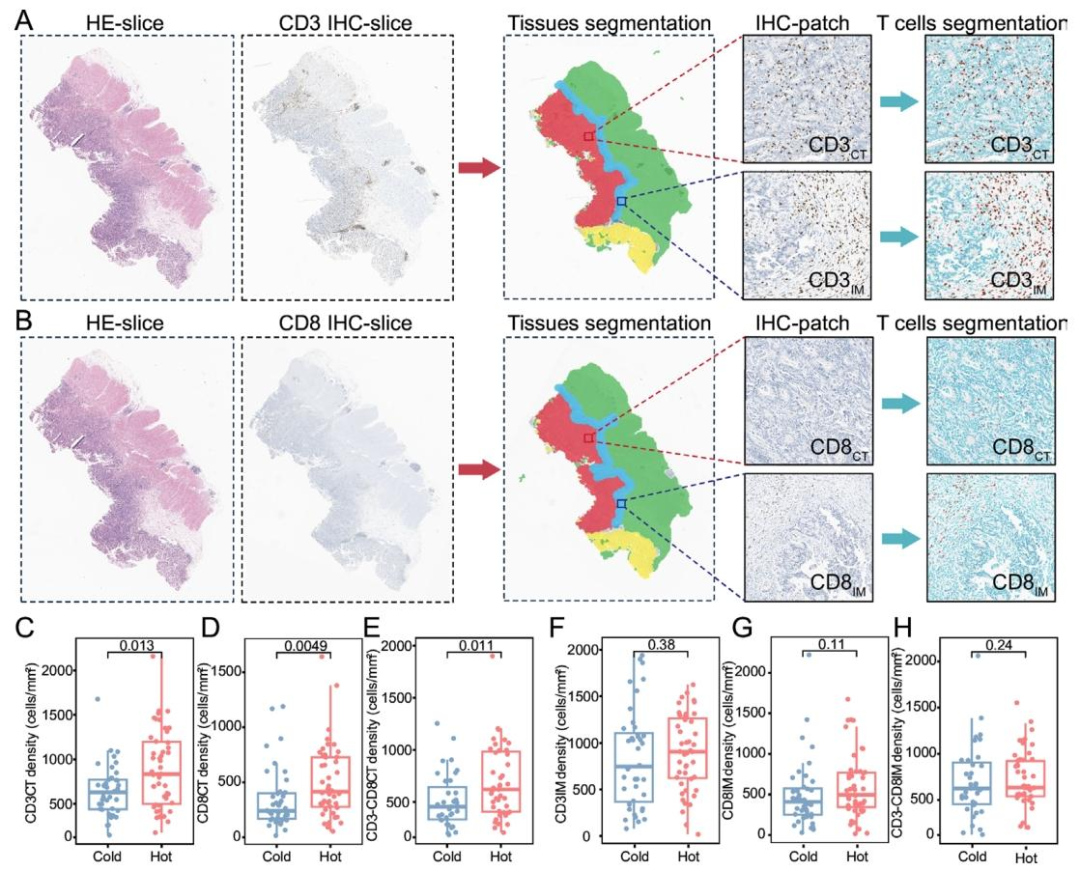
图 4:免疫表型在IHC水平的生物学验证
通过免疫组化(IHC)检测CD3、CD8T细胞密度,验证RNA水平划分的免疫表型的生物学相关性。
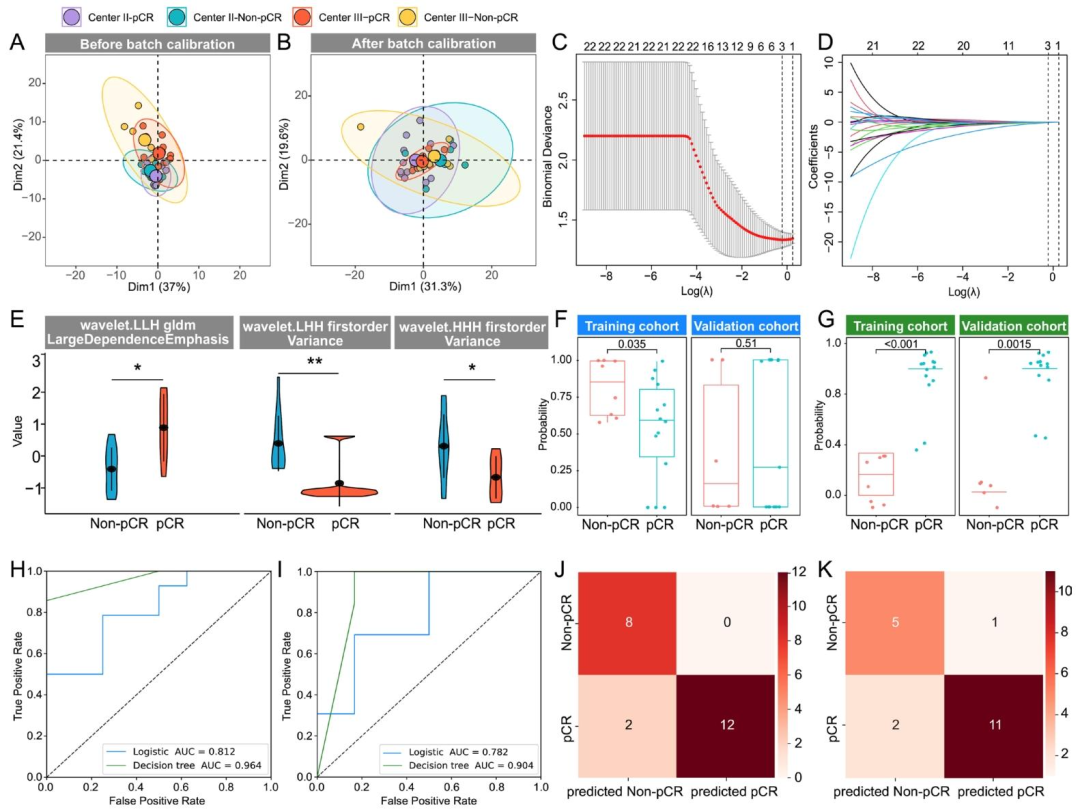
图 5:新辅助免疫治疗反应预测模型的构建与验证
展示放射组学特征筛选、模型构建过程及性能评估结果,对比两种模型(决策树vs逻辑回归)的预测效果。
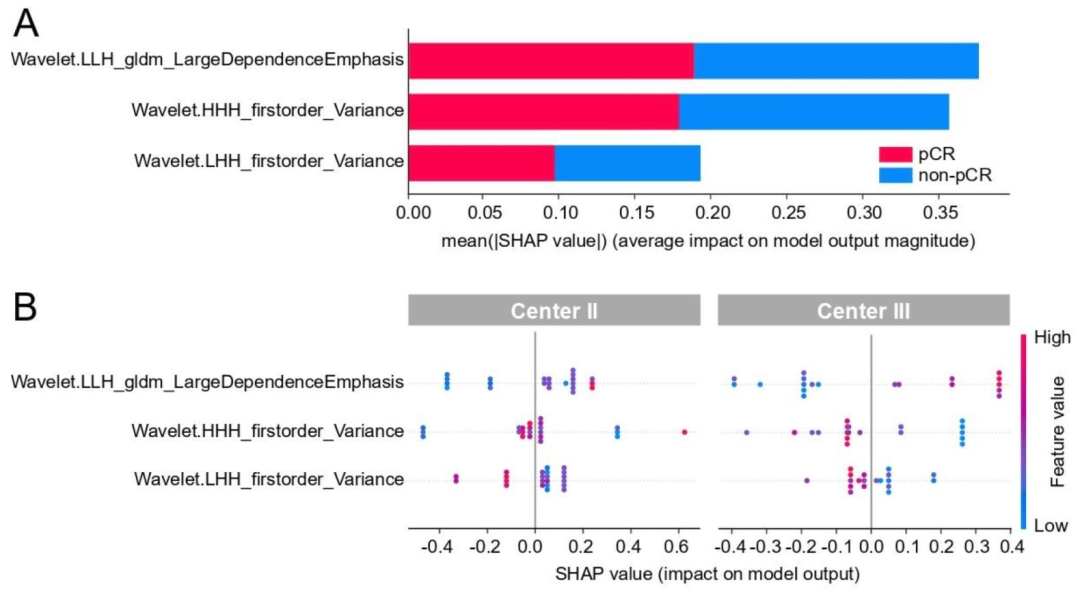
图 6:模型关键特征的SHAP可解释性分析
05
研究结论
本研究构建并验证了一个基于免疫表型引导的可解释放射组学模型 ,用于预测Ⅲ--Ⅳ期d-MMR/MSI-H结直肠癌患者对新辅助抗PD-1免疫治疗的反应。研究首先通过无监督聚类分析RNA测序数据,识别出两种免疫表型(免疫热型与免疫冷型) ,并在免疫组化层面证实热型肿瘤具有更高的CD3+与CD8+T细胞浸润。在此基础上,利用术前CT影像提取放射组学特征,经过两阶段特征筛选,最终纳入三个关键影像特征 构建预测模型。采用决策树算法 结合SHAP可解释性分析 ,该模型在独立验证队列中表现出优异性能,曲线下面积(AUC)达0.904 ,显著优于传统逻辑回归模型。SHAP分析进一步揭示,更高的"大依赖强调"(LargeDependenceEmphasis)和更低的"方差"(Variance) ------分别代表肿瘤纹理均匀性与异质性------是预测病理完全缓解(pCR)的重要影像标志。该研究不仅提供了一种非侵入性、高精度的预测工具 ,还通过免疫表型与影像特征的关联,增强了模型的生物学解释性与临床适用性,为个体化免疫治疗策略的制定提供了有力支持。
参考文献:Zhang Y, Zhang X, Zhong X, Huang L, Jiang W, Zhang C, Liu L, You R, Li Y, Yi X, Liu Z, Chen X, Li Z. Immunophenotype-guided interpretable radiomics model for predicting neoadjuvant anti-PD-1 response in stage III-IV d-MMR/MSI-H colorectal cancer. J Immunother Cancer. 2025 Aug 4;13(8):e011569. doi: 10.1136/jitc-2025-011569.