想象一下,如果你要修理一台精密的智能手机,却只能通过"换零件试错"来判断问题------换个屏幕看是否能开机,换个电池看是否能充电,每试一次就要拆开整机,耗时又费钱。
这正是传统药物研发的真实写照:为了找到一款有效的疗法,科学家往往要在实验室里反复测试成千上万种化合物,90%的候选药物会在临床试验阶段失败,平均每种成功药物的研发成本超过20亿美元,耗时长达10年。
问题的核心在于,我们一直缺乏一种能"提前看见细胞反应"的工具。
传统的细胞模型要么过于简单(比如只模拟单个分子的互动),要么复杂到无法实现(比如试图用计算机拼出真核细胞里100万亿个原子的运动)。
直到虚拟细胞(Virtual Cells)的出现------这种由AI、大数据和自动化实验结合而成的"细胞模拟器",终于让药物研发从"盲人试错"变成了"带导航的精准探索"。
交流群
罗小罗团队是一支以国内外硕博为主的科研团队,覆盖影像组学、病理组学以及基因组学等医学AI主流研究领域。
团队目前拥有7名副教授,60+硕博,多名成员以第一作者身份在Nature(2篇)、Nature Communications、Advanced Science以及Radiology等顶级期刊发表过论文。
如果想要加入我们团队,欢迎投递个人简历到团队邮箱:lxltx2025@163.com
目前小罗全平台关注量120,000+,交流群总成员3000+,大部分来自国内外顶尖院校/医院,期待您的加入!!
由于近期入群推销人员较多,已开启入群验证,扫码添加我的联系方式,备注姓名-单位-科室/专业,即可邀您入群。
虚拟细胞的"破局逻辑":不拼"乐高",改做"细胞翻译官"
传统的细胞模拟思路,本质是"全尺度还原"------就像用乐高积木拼出一整座城市,从每一块砖(分子)到每一栋楼(细胞结构)都要精准复刻。
但真核细胞的复杂度远超想象,这种方法要么拼到一半就卡住,要么拼出来的"城市"无法模拟真实的"人流车流"(分子互动)。
虚拟细胞的创新之处,在于放弃了"全还原"的执念,转而做"精准预测+机制解释"。
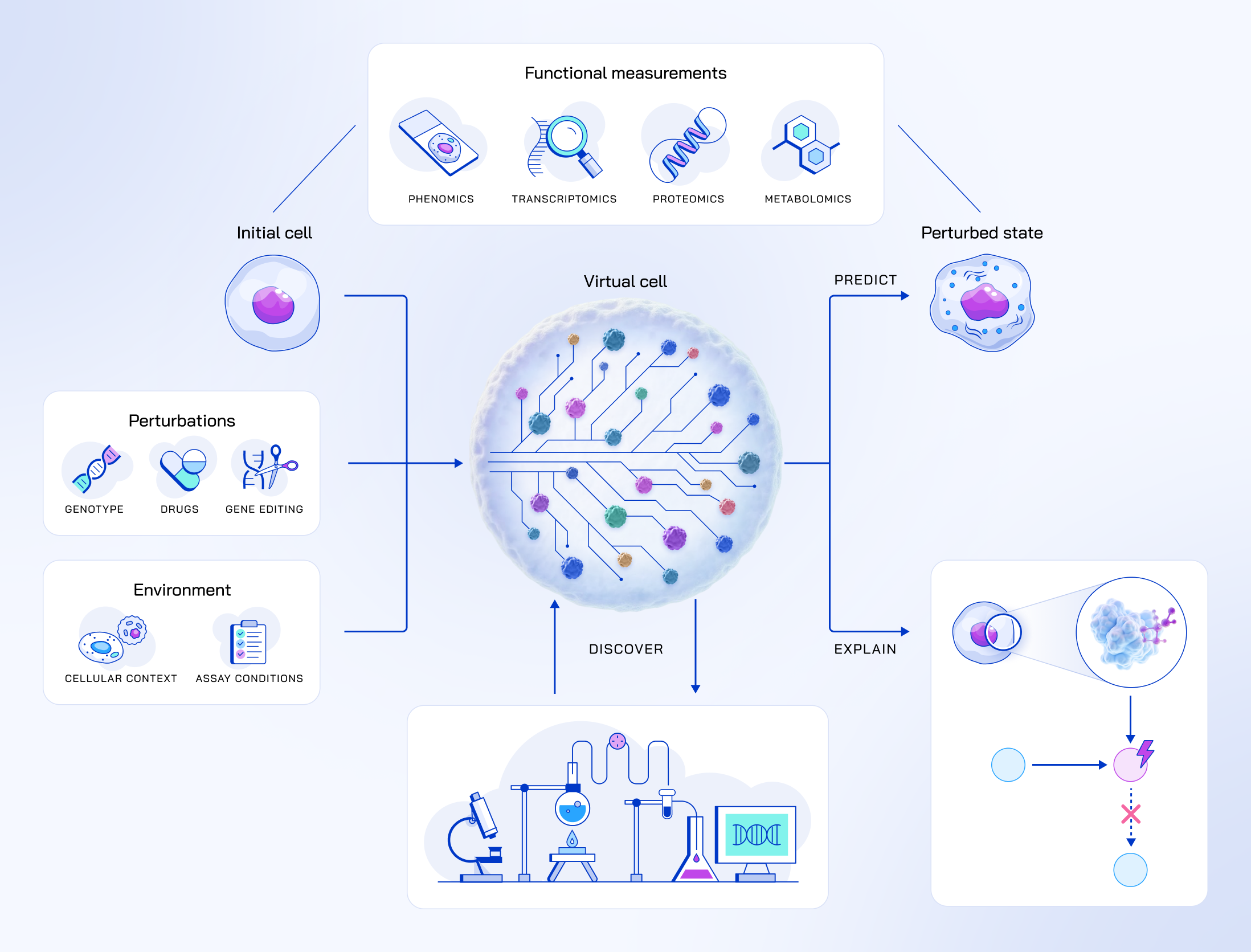
它就像一位懂"细胞语言"的翻译官:先收集细胞的各种"体检报告"(基因、蛋白质、代谢物等多组学数据),再用AI学习这些报告背后的规律,最终能做到三件事
- 预测(细胞遇到药物会有什么反应)
- 解释(为什么会有这个反应)
- 发现(还能尝试哪些新疗法)
这就是它的核心能力(Predict-Explain-Discover,P-E-D)。
要理解它的工作原理,我们可以拆解成三步,每一步都像日常生活中的场景。
第一步:预测(Predict)------像"天气预报"一样推断细胞反应
根据细胞的"初始状态",预测它在药物、基因编辑等"扰动"下的变化。比如,给肿瘤细胞加一种新药,虚拟细胞能提前算出基因表达、细胞形态会怎么变。
用AI模型(如TxPert、GEARS)分析多组学数据,重点学习"初始状态→扰动→变化"的关联,而且不是预测绝对数值,而是"相对变化"(比如对比未加药的正常细胞,加药后某基因活性上升20%)。
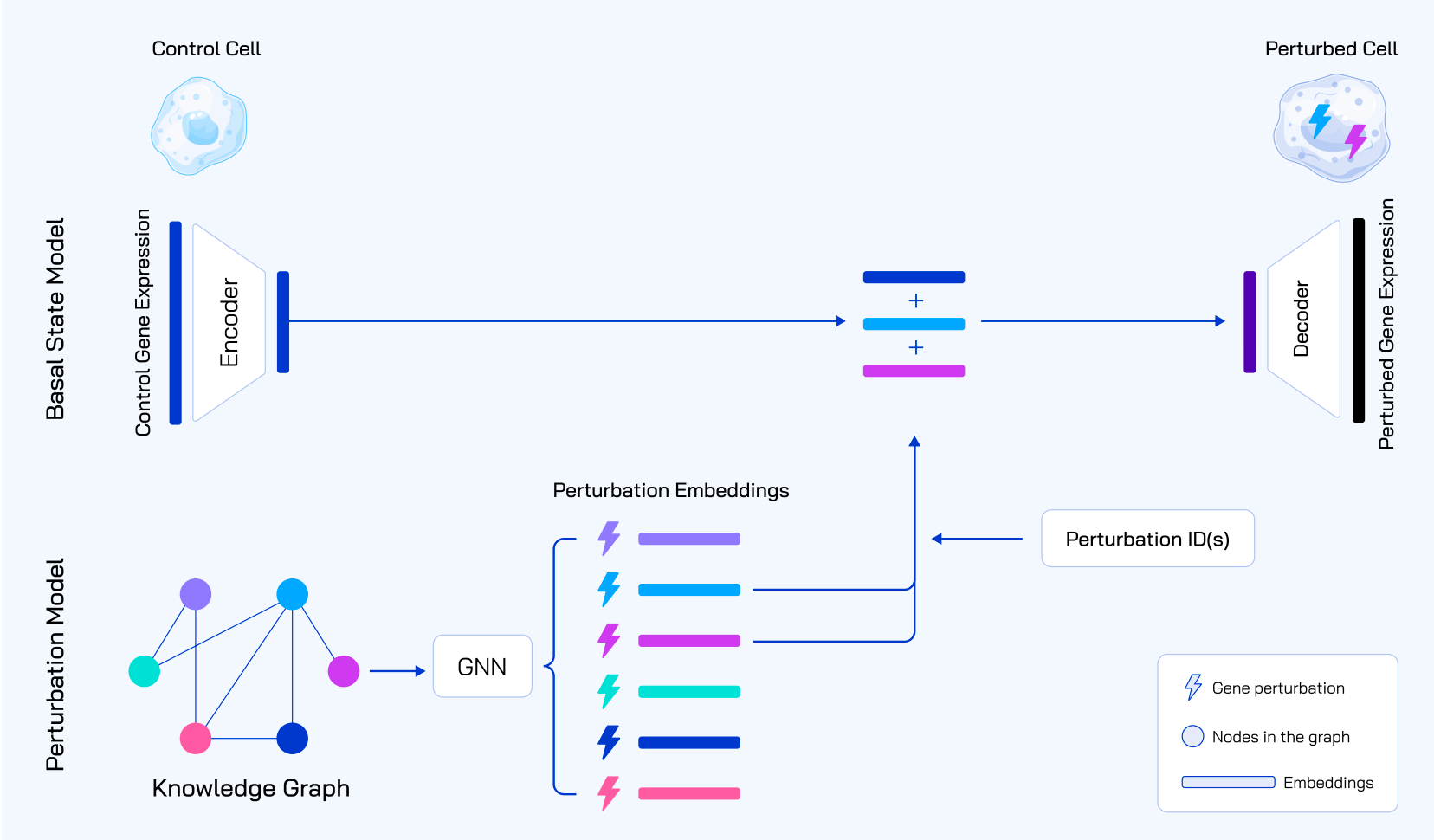
就像天气预报不会只说"明天会下雨",而是结合今天的温度、湿度(初始状态),预测"明天比今天多雨,气温下降5℃"(相对变化),这样更准确。
传统模型常忽略"细胞 context(语境)"------比如同样的药,对肝癌细胞和肺癌细胞的效果可能不同。
虚拟细胞会把细胞类型、实验环境这些"语境"纳入计算,比如预测某药物对"肝星状细胞(一种肝脏细胞)"的毒性时,会自动关联该细胞特有的代谢途径,避免"一刀切"的错误。
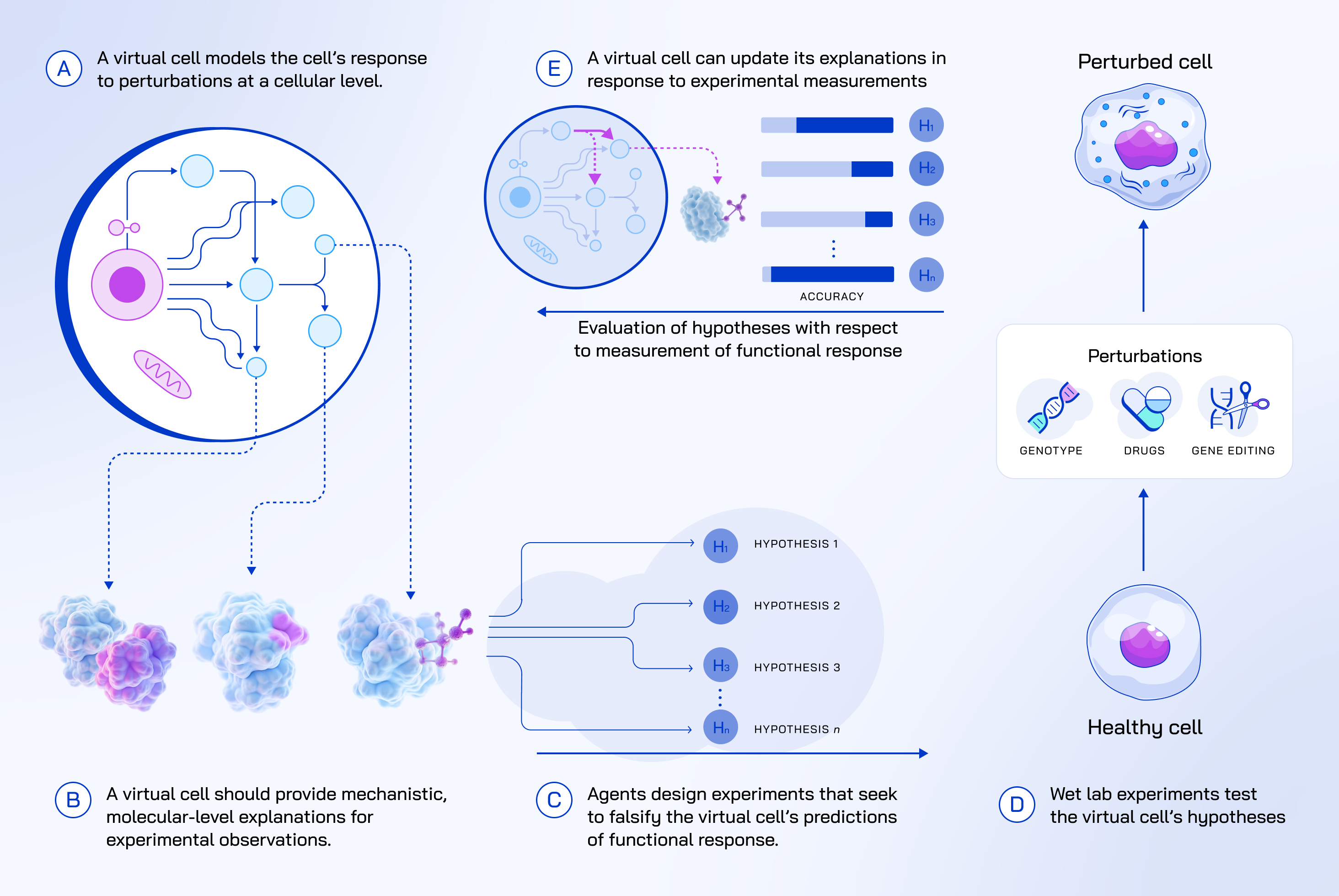
第二步:解释(Explain)------像"侦探查案"一样追溯分子机制
不只是说"会有什么反应",还要说清"为什么"。比如预测某药物能抑制肿瘤生长后,还要解释是"抑制了HDAC酶活性→让肿瘤抑制基因释放→阻止细胞分裂"这个链条。
结合AI驱动的分子模拟(如AlphaFold 3预测蛋白质结构、MLIPs加速原子动力学),从细胞的"宏观反应"反推"微观分子互动",甚至能模拟蛋白质的构象变化、分子结合过程。
就像侦探看到"窗户被撬、财物丢失"(宏观结果),不会只说"遭贼了",而是通过指纹、脚印(分子证据)还原"小偷从哪进、怎么偷"(机制),让结论更可信。
很多AI模型是"黑箱"------能预测但说不出原因,而虚拟细胞的解释是"可验证的"。
比如它说"药物通过抑制HDAC起效",研究人员可以在实验室里敲除HDAC基因,看药物效果是否消失,以此验证机制是否正确。
第三步:发现(Discover)------像"科学家做实验"一样迭代优化
通过"虚拟模拟→实验室验证→更新模型"的闭环,不断提出新假说。
比如虚拟细胞预测"药物A和药物B联用效果更好",实验室验证后,再用结果优化模型,让下一次预测更准。
结合自动化实验室(如Recursion的实验室每周能处理220万份样本)和主动学习算法,优先选择"最能推翻现有模型"的实验去做,快速排除错误方向。
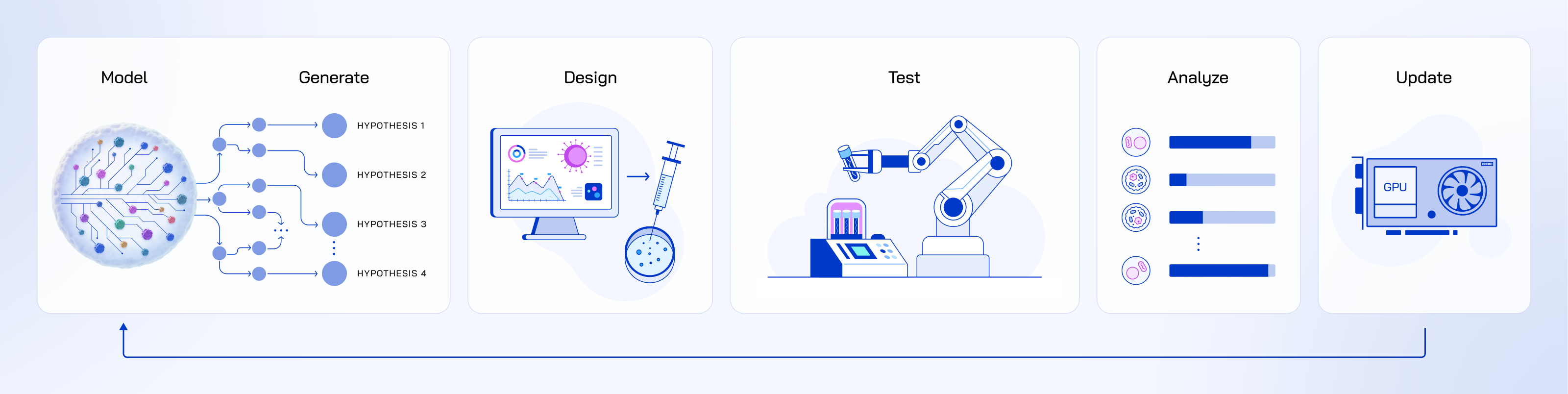
就像厨师试新菜------先在脑子里想"番茄和牛肉搭配可能好吃"(虚拟预测),实际做出来尝一尝(实验室验证),如果太咸就调整盐量(更新模型),反复几次就能找到最佳配方。
传统实验常"盲目试错",比如一次测试1000种化合物,可能990种都无效。
虚拟细胞能先"筛掉"90%不可能的选项,让实验室只聚焦10种最有潜力的,大幅节省时间和成本。
虚拟细胞的价值
基准测试------精准预测基因表达,打败"简单模型"
测试虚拟细胞对"基因扰动"的预测能力------比如敲除某个基因后,其他基因的表达会怎么变。这是判断模型是否可靠的基础,就像考试前先做模拟题。
研究人员用TxPert(一种虚拟细胞模型)和传统的"简单基线模型"(比如直接用平均值预测),分别预测500种不同基因敲除后的转录组变化,再对比真实实验结果。
结果呈现:
- 宏观表现:TxPert的预测准确率比简单模型高35%,尤其是对"细胞周期相关基因"的预测,误差率低于10%;
- 细节验证:当敲除"p53"(一种著名的肿瘤抑制基因)时,TxPert准确预测出"细胞凋亡相关基因表达下降"------这和真实实验中"p53缺失会导致细胞更难死亡"的结论完全一致;
- 深层发现:它还意外发现,p53敲除后,"糖酵解基因"的活性会上升------这为"肿瘤细胞代谢重编程"提供了新线索,而传统模型完全没捕捉到这一点。
传统模型像"死记硬背"------只会根据过去的数据套公式;而虚拟细胞像"理解原理",能捕捉到基因之间的隐藏关联,所以面对没见过的基因扰动,也能准确预测。
真实场景------破解抗癌药机制,发现联合用药方案
分析抗癌药"伏立诺他(Vorinostat)"的作用机制,并寻找能增强其疗效的联合用药。
伏立诺他是一种HDAC抑制剂,用于治疗皮肤T细胞淋巴瘤,但单独使用时效果有限,且机制未完全明确。
用虚拟细胞模拟伏立诺他处理淋巴瘤细胞的过程,预测药物对基因、蛋白质的影响,再设计真实实验验证;同时模拟"伏立诺他+其他药物"的组合,筛选协同作用的方案。
结果呈现:
- 机制验证:虚拟细胞预测"伏立诺他会抑制HDAC酶→让组蛋白乙酰化增加→打开肿瘤抑制基因(如p21)的表达",后续通过"免疫印迹实验"(检测蛋白质)和"染色质免疫沉淀"(检测基因开放状态),完全证实了这个链条;
- 联合用药发现:它还预测"伏立诺他+顺铂(一种DNA损伤药物)"会有协同作用------因为伏立诺他让染色质松散后,顺铂更容易进入细胞核破坏DNA。真实实验中,这种组合让肿瘤细胞死亡率比单独用药高40%;
- 临床价值:基于这个发现,研究人员已经启动小规模临床试验,探索该组合对晚期淋巴瘤患者的疗效,而整个从"虚拟预测"到"临床启动"的过程,只用了18个月------比传统方法快了近一半。
传统研究伏立诺他的机制,需要逐一敲除基因、检测蛋白质,耗时2-3年;而虚拟细胞能直接"锁定"核心通路,让实验目标更明确,同时还能快速筛选联合用药,避免了"大海捞针"式的尝试。
不止于"细胞模拟":虚拟细胞将如何改变医疗未来?
虚拟细胞的价值,远不止"加速药物筛选"------它正在重塑我们对生命科学的研究方式,甚至未来的精准医疗。
当下:解决"传统方法做不到"的难题
在肿瘤研究中,过去很难判断"为什么同一种药对有些患者有效,对另一些无效"。
现在,虚拟细胞可以模拟不同患者的肿瘤细胞(比如携带不同基因突变的肺癌细胞)对药物的反应,快速找到"疗效标志物"------比如发现"EGFR基因突变的患者,对伏立诺他更敏感",这样医生就能提前筛选适合用药的患者,避免无效治疗。
在神经科学领域,它能模拟神经细胞对"神经毒性药物"的反应。
比如研究阿尔茨海默病时,虚拟细胞可以预测某药物是否会影响tau蛋白的聚集,以及对正常神经细胞的毒性,这比直接在动物身上做实验更快速、更伦理。
未来:从"虚拟细胞"到"虚拟患者"
随着技术发展,虚拟细胞会逐步升级为"虚拟组织""虚拟器官",最终实现"虚拟患者"------用计算机模拟一个完整的人体对药物的反应。
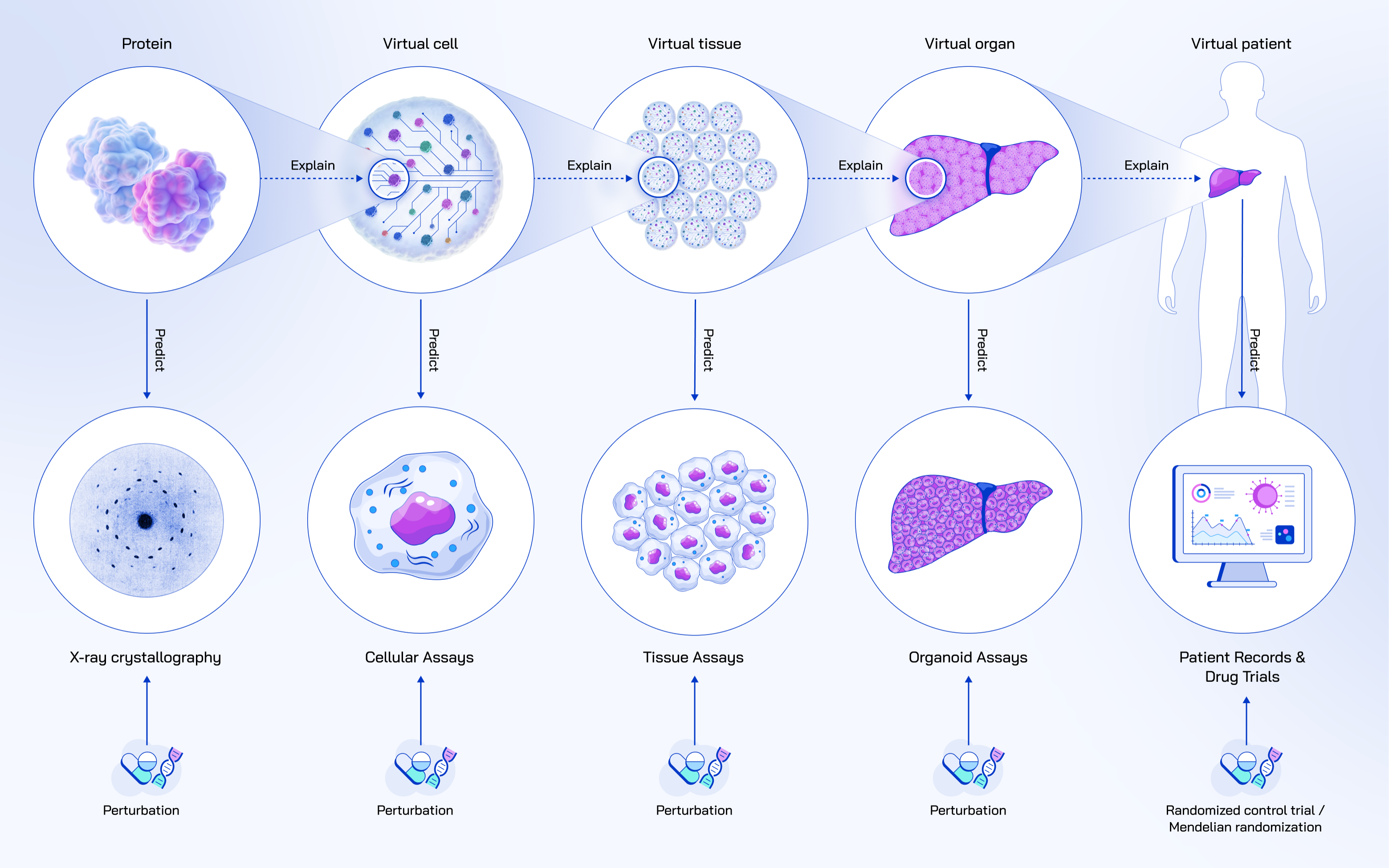
比如,给"虚拟糖尿病患者"用药后,可以同时预测药物对胰岛细胞(降血糖)、肝脏细胞(代谢药物)、肾脏细胞(排泄药物)的影响,提前发现可能的副作用,定制个性化用药方案。
更长远来看,它还能"解锁存量数据"。目前全球实验室积累了大量细胞实验数据,但很多因为"条件不匹配"(比如不同实验室的细胞培养环境不同)无法复用。
虚拟细胞可以学习这些数据的规律,建立"跨条件预测模型"------比如用A实验室的肝癌细胞数据,预测B实验室的肝癌细胞对某药物的反应,让旧数据焕发新价值。
从"试错"到"预测",一场药物研发的革命
回到开篇的"修手机"比喻:如果说传统药物研发是"拆手机试零件",那虚拟细胞就是"带电路图的维修手册"------它不仅告诉你"哪个零件有问题",还能提前模拟"换零件后的效果",甚至推荐"更好的零件组合"。
这场由AI和细胞生物学交叉带来的革命,本质上是让我们从"被动应对疾病"转向"主动预测疾病"。
当虚拟细胞能精准模拟每一个细胞的反应,当"虚拟患者"能为每个人定制用药方案,我们或许就能摆脱"研发10年、失败9次"的困境,让更多药物以更低成本、更快速度抵达需要的患者手中------这,就是虚拟细胞最动人的价值。
参考文献
本文核心技术细节来自Valence Labs与Recursion团队2025年发表于arXiv的研究《Virtual Cells: Predict, Explain, Discover》,论文编号:arXiv:2505.14613v3