一、聚类分群在单细胞数据分析中的核心地位
单细胞转录组测序(scRNA-seq)技术已彻底改变了我们研究细胞异质性的能力,其核心价值在于揭示组织或生物样本中不同类型的细胞状态、发育轨迹和功能亚群。聚类分析作为scRNA-seq数据处理流程中的关键环节,旨在将成千上万个具有相似转录谱的细胞归并为具有生物学意义的群体,是后续进行细胞类型注释、差异表达分析、轨迹推断等高级分析的基础。因此,聚类算法的准确性、稳健性和可解释性直接决定了研究结论的可靠性。
二、数据处理与降维:聚类分析的前置步骤
在进行聚类之前,原始测序数据需经过一系列严格的预处理和质量控制,包括基因表达矩阵构建、数据归一化、高变基因筛选、批次效应校正等。由于单细胞数据的高维稀疏性,直接在高维空间进行聚类通常是低效且易受噪声干扰的。因此,降维是必不可少的步骤,其目的是在保留数据主要结构的同时,将数据投射到低维空间。
目前主流的降维方法包括:
1.主成分分析:提取数据主要变异来源,是后续分析的通用起点。
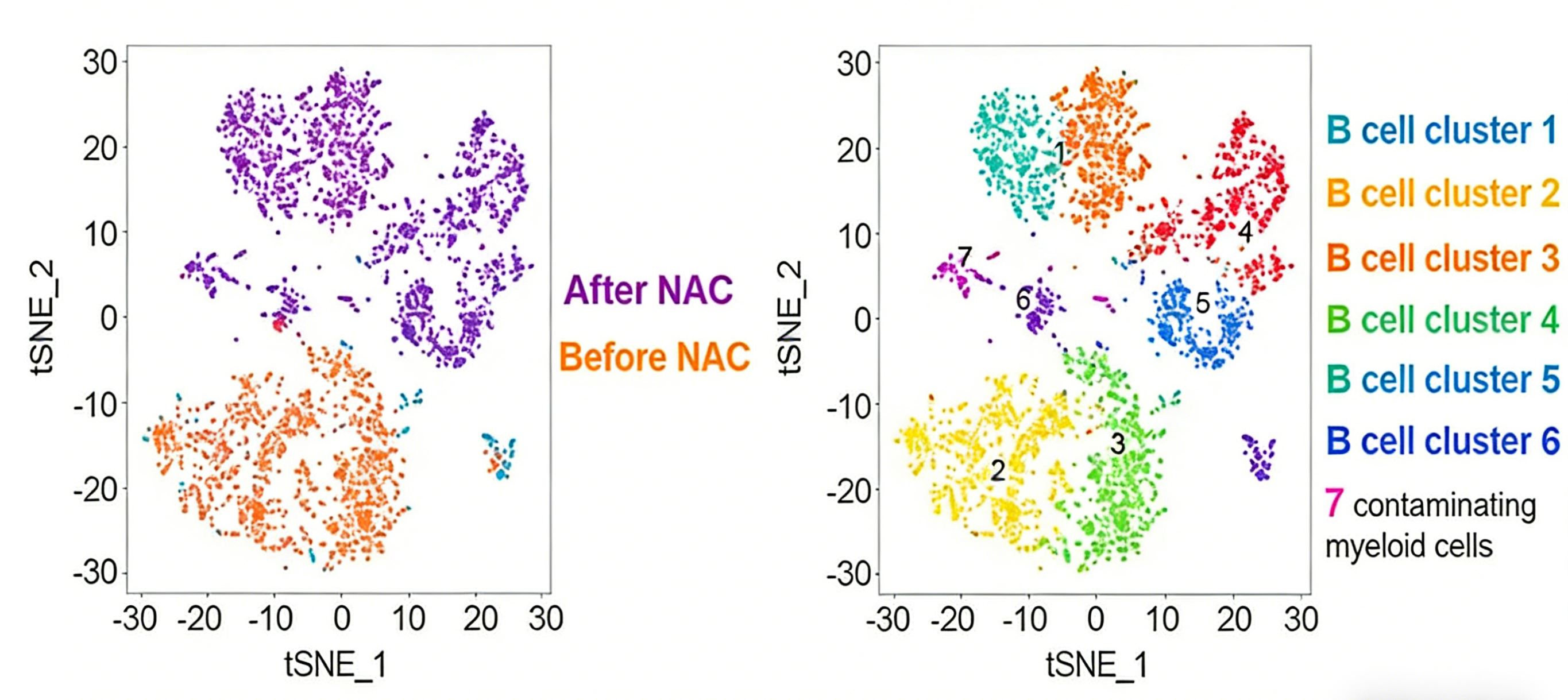
2.t-SNE:将高维数据映射到二维或三维空间,擅长可视化展示局部结构,但因其随机性,不同运行结果可能不一致。
3.UMAP:一种较新的流形学习方法,相比t-SNE能更好地保留数据的全局结构,且计算效率更高,已成为目前最流行的单细胞数据可视化工具之一。
三、主流聚类算法及其原理
根据算法原理,应用于单细胞数据的聚类方法大致可分为几类:
1. 基于图论的聚类方法
这类方法将细胞视为图中的节点,细胞间的相似性(距离)构建边的权重,通过对图进行划分来实现聚类。
Louvain算法与Leiden算法:通过优化模块度来识别网络中的社区结构。Leiden算法是对Louvain的改进,解决了其可能产生不连通社区的问题,是目前Seurat、Scanpy等主流分析工具包的默认或推荐算法。
谱聚类:利用数据相似度矩阵的特征向量进行降维,再对特征向量空间中的点进行聚类,对数据的形状假设较少。
2. 基于质心的聚类方法
K-means及其变种:通过迭代寻找K个质心,将每个细胞分配到最近的质心。该方法效率高,但需要预先指定聚类数K,且对非球形簇和噪声敏感。
模糊C均值:允许细胞以一定的隶属度属于多个簇,能更好地反映细胞状态的连续性。
3. 基于密度的聚类方法
DBSCAN:将簇定义为密度相连的点的最大集合,无需预先指定簇的数目,并能识别噪声点。但在单细胞数据中,细胞密度差异巨大时效果可能不佳。
4. 基于概率模型的聚类方法
高斯混合模型:假设数据由多个高斯分布混合生成,通过期望最大化算法求解。一些工具(如SC3)整合了此类方法,能提供聚类稳定性的评估。
四、聚类分群分析面临的挑战
尽管方法众多,但在实际应用中仍面临诸多挑战:
1.高维稀疏性与"维度灾难":基因表达矩阵极为稀疏,大量基因零表达,且技术噪音显著,给距离计算和邻域定义带来困难。
2.参数敏感性:几乎所有算法都涉及关键参数(如K值、分辨率参数、邻居数、距离阈值等),参数选择对结果影响巨大,缺乏普适性标准。
3.细胞连续性与模糊边界:许多生物学过程(如分化、激活)是连续的,细胞状态呈现连续谱,强行划分为离散的簇会损失信息或产生误导。
4.聚类数目的确定:如何客观确定数据中"自然"存在的类别数量,是聚类分析的基本难题。常用启发式方法(如肘部法则、轮廓系数、Gap统计量)在单细胞数据中常不稳定。
5.批次效应与生物变异的混淆:技术批次差异可能产生虚假的"聚类",需要在聚类前或聚类后进行有效校正。
五、前沿进展与集成策略
为应对上述挑战,研究领域正朝着更稳健、更智能的方向发展:
1.深度学习方法的应用:如scVI、scANVI等模型利用变分自编码器对单细胞数据进行建模,在隐空间进行聚类,能同时处理批次效应并学习细胞连续表示。
2.共识聚类与集成学习:通过组合多个不同算法或不同参数下的聚类结果,形成更稳健的共识聚类。工具如SC3和CACONOIA采用此策略,增强了结果的可靠性。
3.多模态数据整合:结合转录组、表观组(如scATAC-seq)、蛋白组等多组学数据进行联合聚类,获得更精确、信息更丰富的细胞分群。
4.空间信息整合:对于空间转录组数据,将基因表达相似性与物理空间邻近性共同纳入聚类考量,定义空间功能域。
5.自动化与可解释性:开发自动化工具(如PhenoGraph)以减少人工干预,并增强聚类结果的生物学可解释性,例如通过富集分析自动推断细胞类型。
六、最佳实践与展望
进行有效的聚类分群分析,建议遵循以下实践指南:
数据预处理是基础:重视质量控制、适当的归一化和高变基因选择。
多种方法结合验证:不依赖单一算法,结合可视化(如UMAP图)、已知标记基因表达和生物学先验知识进行综合判断。
参数的系统性探索:对关键参数进行网格搜索,评估聚类结果的稳定性(如使用聚类相似性指标)和生物学合理性。
重视下游分析验证:聚类结果需通过差异表达分析、拟时序分析等进行功能验证。
展望未来,单细胞聚类分析将更深入地与人工智能结合,发展出能够自适应数据复杂性、自动推断细胞状态连续变化、并整合多源信息的下一代智能聚类框架。随着数据量的指数级增长和计算能力的提升,聚类算法不仅需要更准确,也需要更高的可扩展性和计算效率,以应对百万乃至千万级细胞数据集的挑战。最终,更精准的聚类分群将为我们绘制更完备的细胞图谱、理解发育与疾病机制提供不可替代的支撑。