导读:2026年初,Nature Cancer 发表了一篇由美国国家癌症研究所(NCI)Lichun Ma团队和宾夕法尼亚大学/费城儿童医院Kai Tan团队联合撰写的Perspective文章------"Cellular neighborhoods in cancer"。这篇文章系统梳理了癌症研究中"细胞邻域"(Cellular Neighborhoods, CNs)这一核心概念的定义、分类、计算方法及其临床意义,为我们理解肿瘤微环境的空间架构提供了一份全景式的路线图。

一、为什么我们需要关注"细胞邻域"?
想象一下热带雨林------树木、灌木、苔藓、昆虫和微生物并非随机分布,而是形成了一个个功能各异的"生态小区"。每个小区中的物种相互依存、协同运作,共同塑造了整个生态系统的面貌。
肿瘤组织也是如此。 在传统的认知中,我们常常将肿瘤微环境(Tumor Microenvironment, TME)视为一个均质的"战场",关注的是整体的免疫细胞丰度、基因表达水平等"非空间"指标。然而,随着空间组学技术的飞速发展,科学家们逐渐认识到:细胞在组织中的空间排布方式,即"谁挨着谁",可能比"什么细胞存在"更加重要。
这正是"细胞邻域"概念的核心价值。细胞邻域,是指组织中反复出现的、具有特征性细胞组成和细胞间相互作用的空间结构单元。 它是介于单个细胞和整个组织之间的一个中间层次的组织形式,是驱动肿瘤生长、进展、免疫逃逸和转移等复杂过程的基本功能单元。
正如文章开篇所言,就像干细胞生态位(stem cell niche)支撑着骨髓和胃肠道的组织维持和再生一样,肿瘤中的细胞邻域也在持续地塑造着肿瘤的命运。传统的组织学方法虽然提供了基础的形态学洞见,但在解析分子复杂性和细胞间相互作用方面力不从心。空间组学技术的出现,才真正为深入探索组织微环境铺平了道路。
二、如何定义"细胞邻域"?------五大核心特征
尽管"细胞邻域"、"生态位(niche)"和"空间域(spatial domain)"这些术语在文献中常常被混用,但本文的一个重要贡献,是提出了统一的定义框架 。作者认为,所有细胞邻域应共享五个核心定义特征:
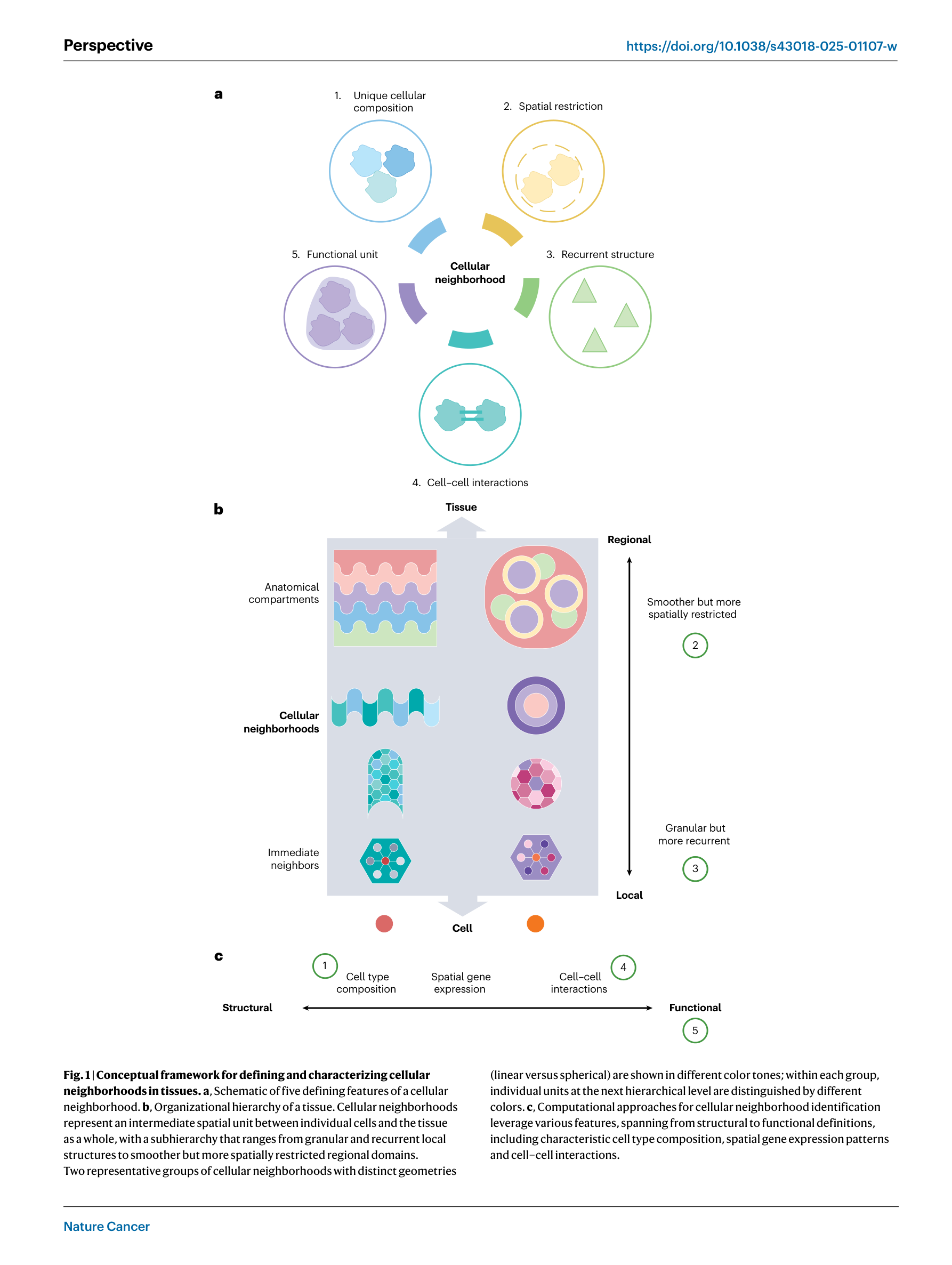
Figure1. (a) 细胞邻域的五大定义特征示意图;(b) 组织的空间层次结构------从单细胞到局部邻域再到区域性域,展示了不同尺度邻域的几何特征;(c) 计算方法在"结构---功能"轴上的分布,涵盖细胞类型组成、空间基因表达和细胞-细胞互作三类特征。
1. 独特的细胞组成(Unique cellular composition)
每个细胞邻域都有其标志性的细胞类型组合。例如,三级淋巴结构(TLS)以中央的CD20+ B细胞和周围的CD4+滤泡辅助性T细胞为特征;而CAF-肿瘤邻域则以癌症相关成纤维细胞和恶性细胞的密切接触为标志。
2. 空间限制性(Spatial restriction)
细胞邻域不是弥散的,而是在组织中占据特定的空间区域。它们在空间上是有边界的、可定位的------这正是区别于传统"细胞丰度"分析的关键。
3. 可重复性(Recurrent structure)
细胞邻域并非一次性的巧合,而是在不同组织区域甚至不同患者样本中反复出现的结构模式。这种可重复性暗示了其背后存在生物学上的"组织规则"。
4. 富集的细胞-细胞相互作用(Cell-cell interactions)
细胞邻域内的细胞之间存在密切的信号交流,通过配体-受体互作、旁分泌信号、代谢物质交换等方式相互影响,构成功能性的信号网络。
5. 功能单元(Functional unit)
细胞邻域不仅仅是一个结构概念,更是一个功能概念。每个邻域都承担着特定的生物学功能,如促进肿瘤增殖、抑制免疫应答、支持干细胞维持或驱动代谢重编程。
📐 空间尺度的层次性
作者特别强调了细胞邻域在空间尺度上的层次性。如 Figure 1b 所示:
-
局部尺度:细胞邻域可能仅包含单个细胞的直接微环境(几个到十几个邻近细胞),更加颗粒化但在不同区域中高度可重复。
-
区域尺度:涵盖更大的、具有特征性细胞类型组成或基因表达模式的空间区域(如解剖学区室),空间上更均一但空间限制性更强。
多种组织层次可以共存于同一组织中,不同的计算方法也侧重于不同的空间尺度和生物学特征。
三、癌症中细胞邻域的三维分类体系
本文另一个核心贡献是提出了一套系统化的细胞邻域分类体系 ,基于三个维度:组成、功能和空间位置。这种分类就像为肿瘤空间生物学建立了一套"分类学"(taxonomy)------正如组织学亚型为理解肿瘤生物学和指导临床决策提供了标准化框架一样,细胞邻域分类学有潜力将空间癌症生物学从描述性学科推向预测性和机制性学科。

Figure2. 细胞邻域按组成分为恶性细胞主导型、免疫细胞主导型和基质细胞富集型;按功能分为增殖性、缺氧重编程、免疫抑制性、干性支持型和代谢重编程;按空间位置分为肿瘤核心区、肿瘤边界区和邻近非肿瘤区域。三种分类互相关联。
🧩(一)基于细胞组成的分类
这是最基础、最直观的分类方式,根据邻域中占主导地位的细胞类型来定义。
🔬 恶性细胞主导型邻域
根据恶性细胞的丰度,细分为两大类:
-
纯恶性细胞邻域(Malignant-only CN):密集堆积的肿瘤区域,免疫活性低,是肿瘤的"核心堡垒"。
-
恶性-TME互作邻域(Malignant-TME interaction CN):恶性细胞与免疫细胞、成纤维细胞和内皮细胞等TME成分之间存在活跃的相互作用,参与免疫接触、基质重塑或血管生成,是理解肿瘤-宿主对话的关键窗口。
更精细的分类则基于恶性细胞的细胞状态,包括上皮-间充质转化(EMT)、细胞周期、干扰素应答、缺氧和应激反应等。举几个代表性例子:
-
肝癌 :基于恶性细胞状态的空间组织鉴定出了8种不同的恶性细胞邻域,每种与独特的TME组成相关。
-
肺癌:EMT相关邻域的特征是EMT样恶性细胞、肌成纤维细胞和巨噬细胞之间的空间互作。
-
卵巢癌等的干扰素应答相关邻域:标记为干扰素应答和抗原呈递相关基因高表达,优先与免疫细胞共定位。
-
多种癌症中的缺氧应激邻域:特征为VEGFA、HSPA1B和ADM等基因高表达,通常远离血管分布。
🛡️ 免疫细胞主导型邻域
根据主导的免疫细胞谱系,分为两个主要亚型:
-
淋巴细胞主导型 :最典型的代表是三级淋巴结构(TLS) ------由中央的CD20+ B细胞区和周围的CD4+ T滤泡辅助细胞区组成,还可能包含CD8+细胞毒性T细胞、调节性T细胞、CD68+巨噬细胞和树突状细胞等。此外,近年在肺腺癌中发现的"淋巴网络"(lymphonets)------特别是TCF1+PD-1+CD8+ T细胞和B细胞组成的空间网络------为TLS之外的淋巴邻域增添了新成员。
-
髓系细胞主导型 :包括巨噬细胞、单核细胞、树突状细胞和粒细胞的多种亚型。功能高度多样且上下文依赖------脑肿瘤中的M1型巨噬细胞富集邻域、胰腺导管腺癌中的基质相关CD68+巨噬细胞邻域与抗肿瘤免疫相关;而肝癌侵袭前沿的CSF1R+PD-L1+肿瘤相关巨噬细胞富集邻域、以及SPP1+/CCL20+巨噬细胞和SPP1+/CCL4+/IFIT1+中性粒细胞富集邻域则构成免疫抑制微环境。
🧬 基质细胞富集型邻域
以成纤维细胞和内皮细胞为主导,是TME的关键调节者。文章总结了四种CAF富集的细胞邻域亚型,每种参与不同的配体-受体互作网络:
| 邻域类型 | 主要特征 |
|---|---|
| CAF-肿瘤邻域 | FGF2-FGFR1、TGF-beta-TGFBR1和胶原信号驱动ECM重塑 |
| 基质富集邻域 | 成纤维细胞和内皮细胞为主 |
| CAF-髓系富集邻域 | CAF与髓系免疫细胞共定位 |
| CAF-淋巴聚集体邻域 | CAF与淋巴细胞聚集 |
⚙️(二)基于功能的分类
这一维度聚焦于细胞邻域的生物学功能,揭示了它们如何参与肿瘤的关键过程。
📈 增殖性细胞邻域
增殖细胞并非随机散布,而是组织成不同尺度的增殖邻域:
-
小邻域(~10-30微米):代表少数快速分裂的局部恶性克隆。
-
大邻域(~100-300微米):反映缺氧、营养分布等宏观环境因素的影响。
在胰腺导管腺癌(PDAC)中,Ki-67+和Ki-67-肿瘤/导管细胞形成截然不同的邻域,提示局部环境和邻近细胞可能决定癌细胞的增殖能力。
🫁 缺氧诱导的功能重编程邻域
缺氧是大多数实体瘤的共同特征,与肿瘤侵袭性、治疗耐药和不良预后密切相关。当恶性细胞远离富含氧气的血管时,氧气、营养物质和代谢废物的梯度驱动恶性细胞的功能重编程。在胶质母细胞瘤中,空间转录组分析揭示了层状组织的缺氧驱动细胞邻域 ,每层具有不同的肿瘤细胞状态和免疫-基质相互作用。缺氧还调控肿瘤细胞的"生长或逃逸"(growth or go)潜力------快速增殖的肿瘤可能从磷酸戊糖途径转向糖酵解以求生存,部分具有生存或迁移优势的肿瘤细胞则逃逸至含氧区域。
🚫 免疫抑制性细胞邻域
由调节性T细胞、M2极化巨噬细胞等免疫抑制细胞和多种机制共同构建。典型的免疫抑制邻域常位于肿瘤边界,通过三重机制发挥作用:
-
物理屏障:致密的纤维基质限制免疫细胞浸润。
-
化学招募:恶性和基质细胞产生趋化因子(如CXCL6)招募免疫抑制细胞并促进M2极化。
-
检查点抑制:恶性和非恶性细胞表达免疫检查点分子。
🧫 干性支持型细胞邻域
为癌症干细胞(CSC)提供支持性微环境。多种细胞类型参与其构建:
-
在胶质母细胞瘤中,分化的恶性细胞通过BDNF-NTRK2旁分泌信号促进干细胞生长,干细胞则分泌VGF神经肽支持自身和分化细胞的存活------形成正反馈环路。
-
CAF和肿瘤相关巨噬细胞通过IL-6和IL-8等细胞因子支持CSC存活。
⚡ 代谢重编程细胞邻域
肿瘤细胞不仅依赖自身代谢(沃伯格效应),还与邻近细胞进行代谢共生 ------含氧区域的恶性细胞以邻近糖酵解细胞产生的乳酸为主要能源。这种代谢共生还延伸到基质和免疫细胞("反沃伯格效应"):
-
PDAC中高度活化的代谢性CAF通过供给氧化磷酸化底物支持肿瘤代谢。
-
胶质母细胞瘤中富含脂质的巨噬细胞将髓鞘来源的脂质转移给癌细胞。
-
肿瘤细胞甚至可以向肿瘤浸润淋巴细胞转移线粒体,导致后者代谢功能障碍和抗肿瘤免疫受损。
📍(三)基于空间位置的分类
从解剖学角度,细胞邻域按其在肿瘤和周围组织中的位置分为三类:
-
肿瘤核心区:纯恶性邻域和缺氧相关邻域的主要分布区。
-
肿瘤边界区:恶性-TME互作邻域和免疫抑制邻域的重要分布区。值得注意的是,"肿瘤边界"(tumor border,肿瘤与邻近组织的整体边界)与"肿瘤侵袭前沿"(invasive front,主动入侵的恶性细胞前缘)是不同的概念。
-
邻近非肿瘤区域:以非恶性细胞为主。
一个值得深思的发现:同一类型的细胞邻域在不同位置的功能可能截然不同。 例如,TLS在肿瘤内部通常与抗肿瘤免疫相关,但在肝内胆管癌的瘤内和瘤周区域却与不同的临床结局相关联。这提醒我们,脱离空间上下文讨论邻域功能是不完整的。
四、识别细胞邻域:技术平台与计算方法
空间组学技术产生的海量数据,需要配套的技术平台和计算方法来解析。文章系统梳理了当前主流的技术平台和三大类计算方法。
🔬 空间组学技术平台一览
文章以 Table 1 详细列举了当前主流的空间组学技术平台,涵盖转录组、蛋白组和代谢组三大模态:
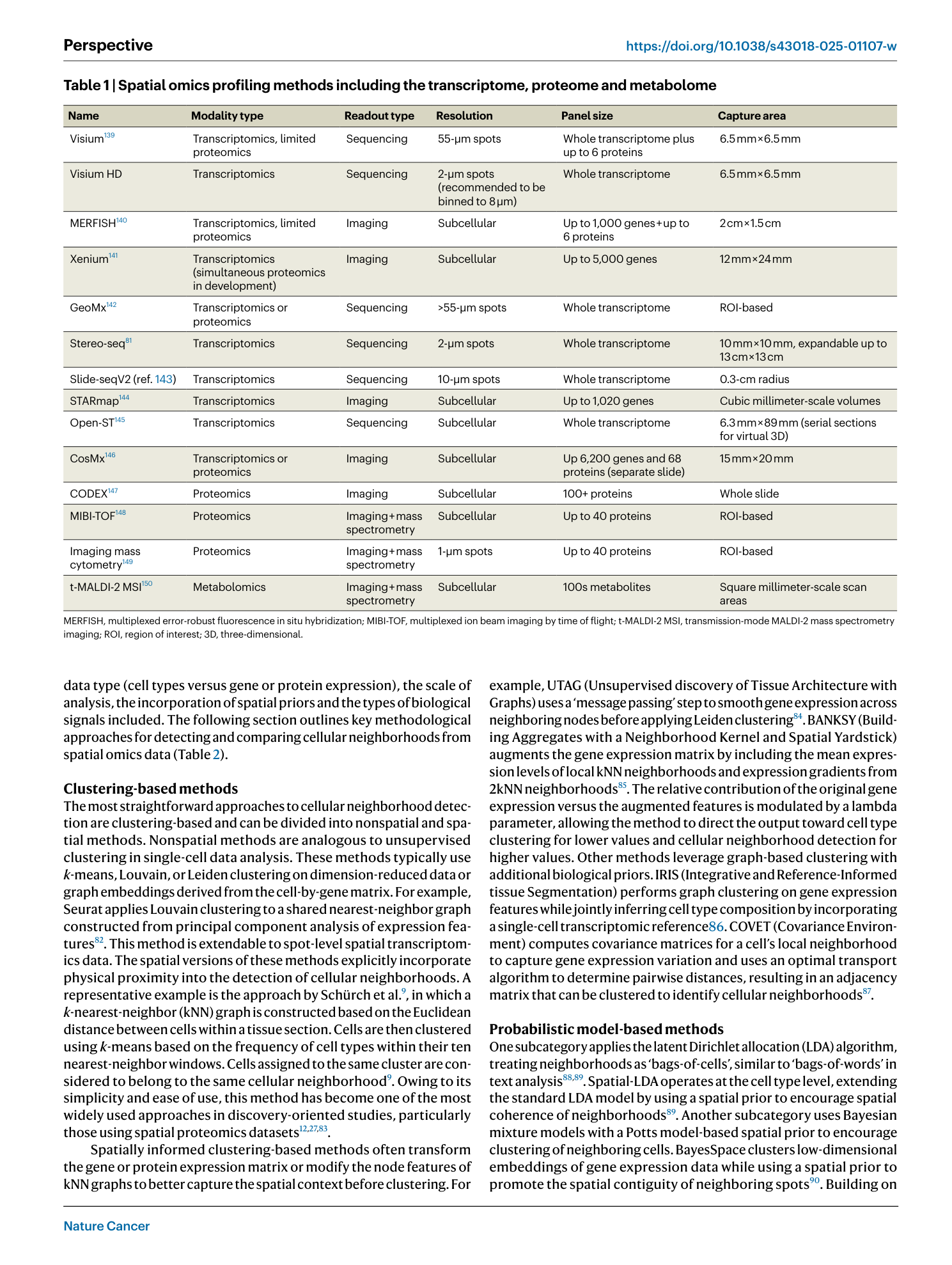
Table1. 列出了12种主流空间组学平台的模态类型、检测方式、分辨率、面板大小和捕获面积等核心参数。
关键平台包括:
-
测序类:10x Visium(55微米 spot)、Visium HD(2微米)、Stereo-seq(500纳米,最大可达13cm x 13cm)等
-
成像类:MERFISH(多达1000基因)、Xenium(多达5000基因,亚细胞分辨率)、CosMx(6200基因+68蛋白)、CODEX(100+蛋白)等
-
质谱成像类:MIBI-TOF、成像质谱流式(IMC)、t-MALDI-2 MSI(代谢组学)
🧮 三大类计算方法
文章以 Table 2 系统梳理了细胞邻域检测方法,可归纳为三大方法学范式:
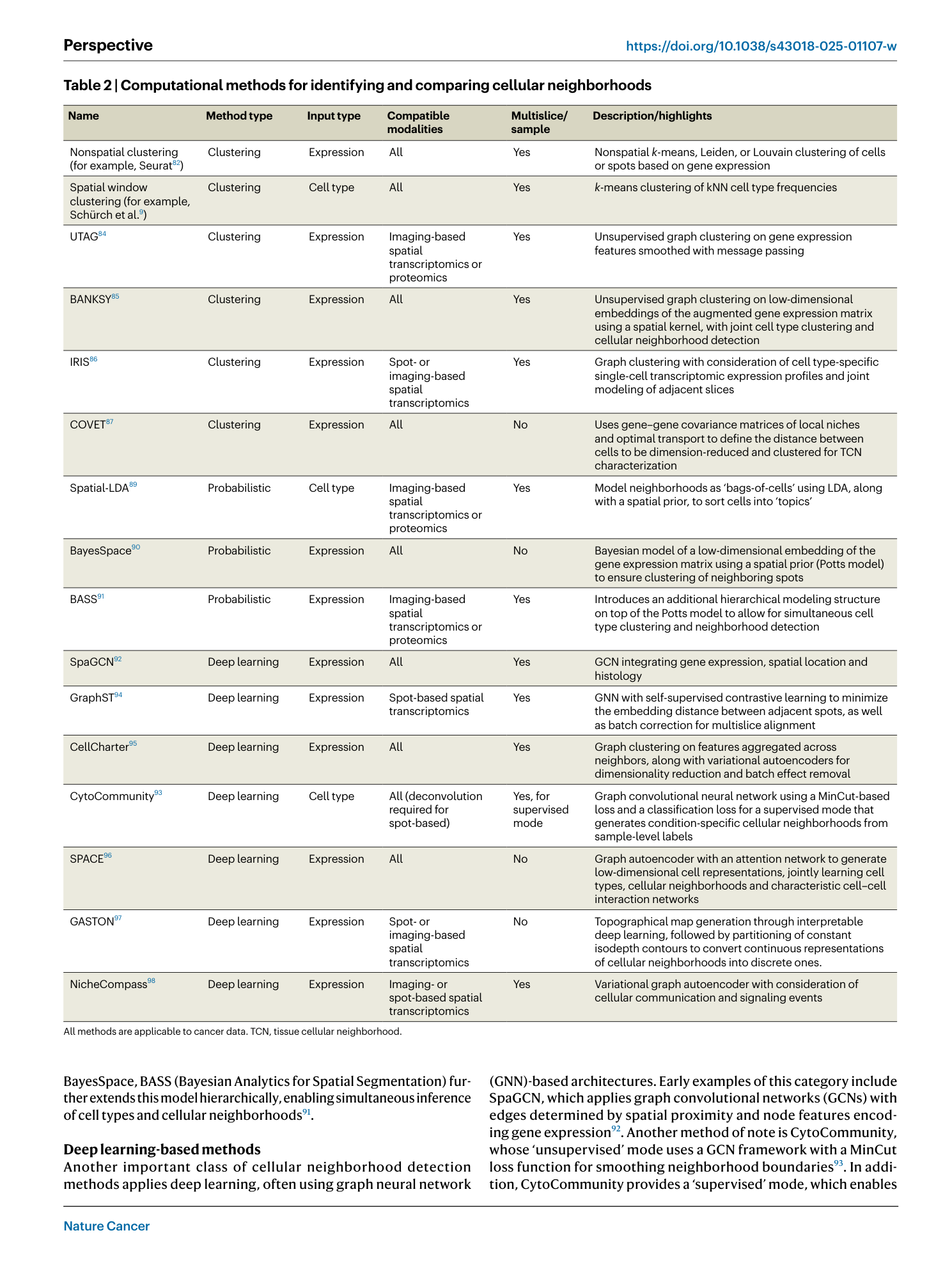
Table2. 系统列出了14种代表性的细胞邻域检测方法,包括方法类型、输入类型、兼容的空间组学模态、是否支持多切片/多样本分析等信息。
🔷 聚类方法(Clustering-based)
最直接的方法类别,又分为非空间聚类和空间聚类:
-
非空间聚类(如Seurat):在降维后的基因表达数据上进行Louvain/Leiden聚类,不考虑空间位置。
-
空间窗口聚类(如Schuerch等人的经典方法):构建基于细胞间欧氏距离的kNN图,基于最近邻窗口内的细胞类型频率进行k-means聚类------因简单易用而成为蛋白组学空间数据分析的首选。
-
高级空间聚类:UTAG(消息传递平滑表达)、BANKSY(局部邻域表达增强+lambda参数调控)、IRIS(整合单细胞参考)、COVET(协方差矩阵+最优传输)等。
🔷 概率模型方法(Probabilistic)
-
Spatial-LDA:将邻域建模为"细胞词袋",类似文本分析中的主题模型,结合空间先验鼓励空间一致性。
-
BayesSpace:贝叶斯混合模型+Potts模型空间先验,促进邻近spot的聚类一致性。
-
BASS :在BayesSpace基础上引入分层建模,实现细胞类型聚类和邻域检测的同时推断。
🔷 深度学习方法(Deep learning-based)
-
SpaGCN:图卷积网络,整合基因表达、空间位置和组织学信息。
-
CytoCommunity:提供无监督和有监督两种模式,有监督模式可从样本级标签识别条件特异性邻域。
-
GraphST:自监督对比学习+批次校正的图神经网络。
-
CellCharter:变分自编码器进行降维和批次效应去除。
-
GASTON:创新性的"地形学"方法,先学习连续的"等深度线",再离散化定义邻域。
-
NicheCompass:图变分自编码器+配体-受体数据库先验知识。
📊 基准测试的实用指导
一项对19种方法的综合基准测试给出了重要结论:
-
添加空间位置信息显著提升邻域识别准确性------最核心的启示。
-
没有单一方法在所有数据模态上都表现最优。
-
GraphST 在总体准确性、计算效率和内存使用方面取得最佳平衡,是推荐首选。
-
整合多种方法的结果通常能增强鲁棒性。
-
GCN类工具的默认参数并非总是最优的,建议有编程经验的用户进行调参。
🔄 邻域比较:尚待开拓的前沿
如何定量比较不同条件下的细胞邻域变化,是当前领域的关键挑战。目前大多研究依赖间接评估(如邻域内差异细胞类型富集),新兴方法如COVET和NicheCompass开始提供局部生态位映射策略,SMORE通过随机游走发现空间motif。邻域比较和对齐方法的进一步开发将是该领域下一个重要增长点。
五、从实验室到病床:细胞邻域的临床价值
也许对临床工作者和转化研究者而言最令人兴奋的部分------细胞邻域正在成为预测患者预后和治疗反应的新型生物标志物。
🏥 预后预测
两种主要策略将细胞邻域与临床结局关联起来:
策略一:基于邻域全景的亚型分类。 在肝细胞癌中,基于恶性细胞和免疫细胞的空间互作将患者分为四个预后显著不同的组,其中CD8+T细胞富集互作组预后最好。
策略二:聚焦特定邻域的预后价值。 在非小细胞肺癌中,CAF与恶性细胞共定位的患者预后最差;而CAF与T/B细胞在淋巴聚集体中共定位的患者预后最好。更振奋人心的是,在肝细胞癌中发现阻断PD-L1和TGF-beta能恢复活化的CD8+T细胞并消除残余肿瘤细胞------直接证明了靶向功能失调细胞邻域的治疗潜力。
💊 治疗反应预测
-
非小细胞肺癌:成熟TLS(含CD23+滤泡DC)与免疫治疗改善响应相关;不成熟TLS则无预测价值。
-
肝细胞癌:成熟免疫调节性DC、CXCL13+辅助T细胞和祖细胞样CD8+T细胞组成的邻域与PD-1阻断更好反应相关。
-
肺癌:富含干性TCF7+PD-1+CD8+T细胞、活化CCR7+LAMP3+DC和CCL19+成纤维细胞的"干性-免疫中心"与PD-1阻断获益相关。
-
三阴性乳腺癌 :恶性细胞与B细胞和GZMB+T细胞的空间互作预测化疗+抗PD-L1免疫治疗反应,但不能 预测单纯化疗反应------强调了临床相关性的情境依赖性。
⚖️ 空间信息 vs 非空间指标:决定性优势
文章通过三个有力案例论证了空间信息的不可替代性:
| 癌症类型 | 非空间指标 | 空间邻域指标 |
|---|---|---|
| 小细胞肺癌 | 免疫细胞丰度不能预测预后 | MT2邻域(抗肿瘤巨噬+CD8+T+NKT)预测更好结局和免疫治疗反应 |
| 胶质母细胞瘤 | 星形胶质样恶性细胞丰度与预后无关 | 其空间互作模式与预后密切相关 |
| 皮肤T细胞淋巴瘤 | 免疫/恶性细胞频率在应答者和非应答者间无差异 | PD-1+CD4+T细胞与恶性细胞的空间邻近性预测治疗反应 |
核心启示:细胞邻域提供的空间信息是传统非空间分析无法获取的,它为精准肿瘤学开辟了全新维度。
六、未来展望:迈向空间靶向治疗时代
展望未来,作者勾勒了三个令人期待的发展方向:
🤖 1. AI和基础模型的赋能
随着空间组学数据的爆炸式增长,AI基础模型将成为核心引擎。类似于scGPT在单细胞分析领域的变革性影响,Nicheformer、CellSAM和SpatialAgent等空间组学基础模型正在兴起,有望实现更精准的细胞分割、多模态空间数据整合,以及单细胞图谱与空间上下文的桥接。
🗺️ 2. 构建泛癌细胞邻域图谱
STOmicsDB、SODB等公共数据库已开始汇集空间组学数据集。将这些数据整合为泛组织、泛癌细胞邻域图谱,将使我们能系统性地鉴定保守的和癌种特异的邻域类型,并为计算方法提供"金标准"基准。
🧪 3. 实验验证:从关联到因果
-
空间基因扰动平台(Perturb-map、Perturb-FISH、CRISPRmap):在保留空间信息的情况下进行遗传扰动,直接验证邻域功能。
-
临床前模型(异种移植、基因工程小鼠):仍然重要但受限于物种差异。
-
生物工程策略(组织芯片,Tissue-on-a-chip):重建合成细胞邻域,模拟人类特异性TME,研究邻域特异性的细胞互作和治疗脆弱性。
七、小结
这篇Perspective文章为癌症空间生物学提供了一个极为重要的概念和方法学框架,其核心贡献可概括为:
| 维度 | 贡献 |
|---|---|
| 定义统一 | 五大核心特征为多样化的"邻域"概念建立共识基础 |
| 分类体系 | 组成-功能-位置三维分类为肿瘤空间架构标准化描述奠基 |
| 方法集成 | 从聚类、概率模型到深度学习的全景综述,附带实用选择指南 |
| 临床转化 | 大量证据证明空间信息在预后和疗效预测中超越传统非空间指标 |
细胞邻域的研究正将空间癌症生物学从"描述性"推向"预测性和机制性"。随着空间组学技术的持续革新、AI方法的深度赋能、以及实验验证手段的不断完善,我们有理由期待:以细胞邻域为靶点的"空间靶向治疗"将成为精准肿瘤学的下一个前沿阵地。
参考文献 Ma, L., Xiong, B., Liu, M. and Tan, K. Cellular neighborhoods in cancer. Nature Cancer (2026). https://doi.org/10.1038/s43018-025-01107-w IF: 28.5 Q1 B1