文章:SPEGC: Continual Test-Time Adaptation via Semantic-Prompt-Enhanced Graph Clustering for Medical Image Segmentation
代码:https://github.com/Jwei-Z/SPEGC-for-MIS
单位:陕西科技大学陕西省人工智能联合实验室
一、问题背景
医学图像分割是AI辅助诊断的核心技术,能精准勾勒出眼底视神经、肠道息肉、心脏组织等关键区域,但域偏移问题严重阻碍了模型的临床部署。简单来说,模型在A医院的设备、标注数据上训练,到B医院用不同扫描仪、不同采集协议的图像做检测,效果会显著下降。
更贴合临床的痛点是,测试数据并非批量输入,而是单张、连续的流数据,这就要求模型实现持续测试时自适应(CTTA) :一边处理新图像,一边自适应新数据分布,同时还要避免两个致命问题------错误累积 (越适配越出错)和灾难性遗忘(适配新数据后,忘了原本的核心分割能力)。
而现有CTTA方法要么依赖像素级的不可靠监督信号,要么冻结核心模型参数仅做轻量适配,适配能力弱、抗干扰性差,始终无法很好地平衡适配效果和模型稳定性。
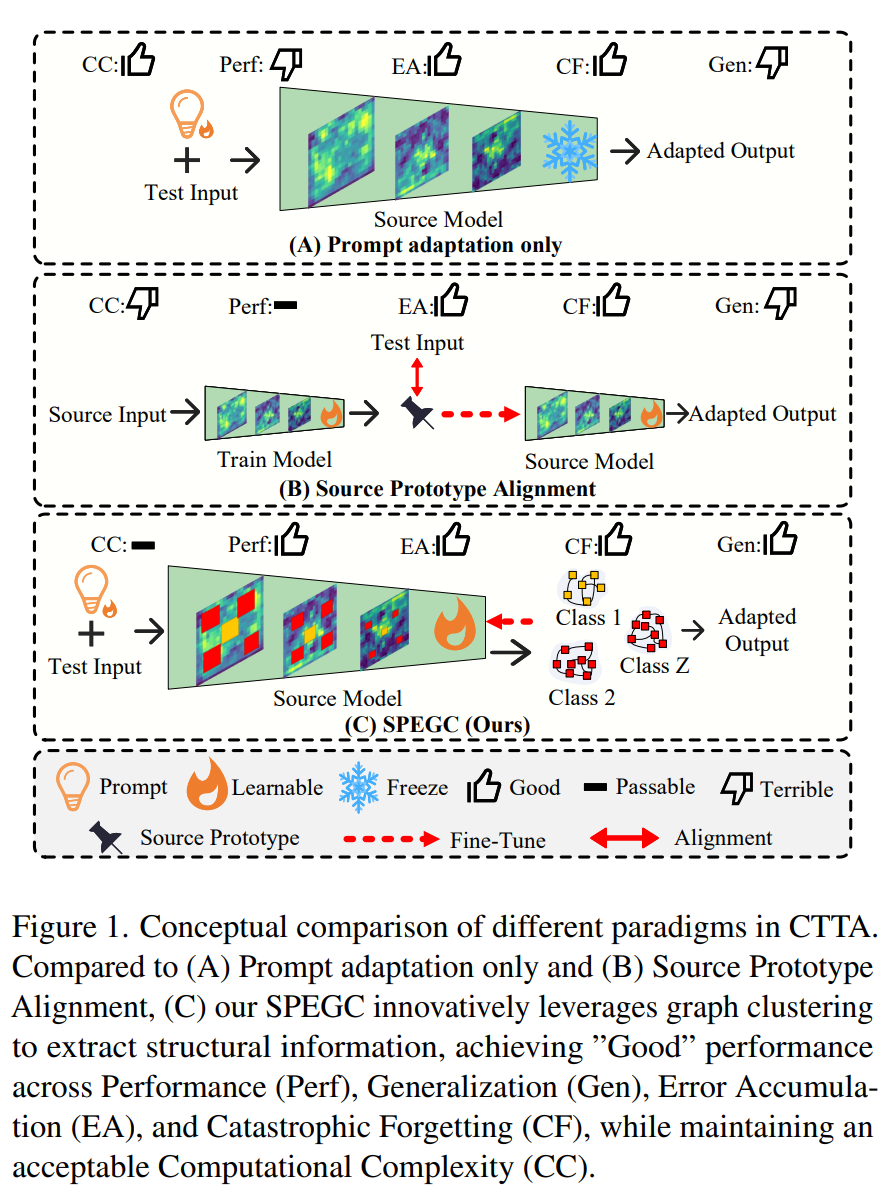
二、方法创新
为解决上述问题,研究团队提出了基于语义提示增强图聚类的持续测试时自适应框架(SPEGC),核心思路是"先增强特征抗干扰性,再用结构化特征指导模型自适应",设计了两大核心模块,配合联合优化策略实现端到端的模型适配,整体流程层层递进、环环相扣:
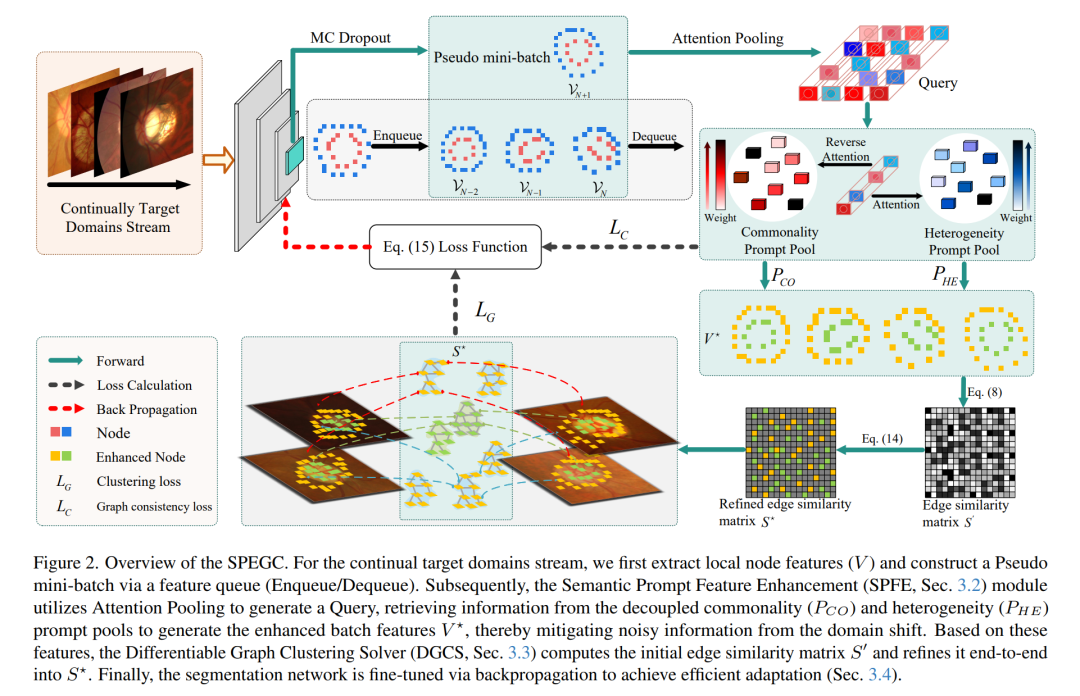
-
语义提示特征增强模块(SPFE) :先通过MC Dropout量化图像特征的不确定性,筛选出稳定的核心特征;再设计解耦的通用提示池和专属提示池,前者提取跨医院、跨设备的通用语义知识,后者捕捉特定数据的专属特征,通过注意力和反向注意力机制,将两类全局信息注入局部特征,有效缓解域偏移下的噪声干扰,让特征更稳定、更具代表性。
-
可微分图聚类求解器(DGCS) :将增强后的特征转化为图节点,先计算节点间的相似度矩阵,再把图聚类的离散问题转化为最优运输问题,通过Sinkhorn算法实现全局边稀疏化,蒸馏出精炼的高阶结构相似度矩阵,让特征形成清晰的语义聚类(比如视神经特征归为一类、息肉特征归为一类)。
-
联合优化策略:设计图一致性损失和聚类损失双目标函数,前者保证同一聚类内的特征分割预测一致,动态调整模型决策边界;后者约束通用提示池的语义稳定性,强制模型保留跨域核心知识,从结构和语义两层避免错误累积和灾难性遗忘。
三、实验结果
研究团队在眼底视盘/视杯分割 和肠道息肉分割两大经典医学图像分割任务上开展了全面实验,还拓展到3D心脏MRI分割任务,对比了6种当前主流的CTTA方法,结果亮眼:
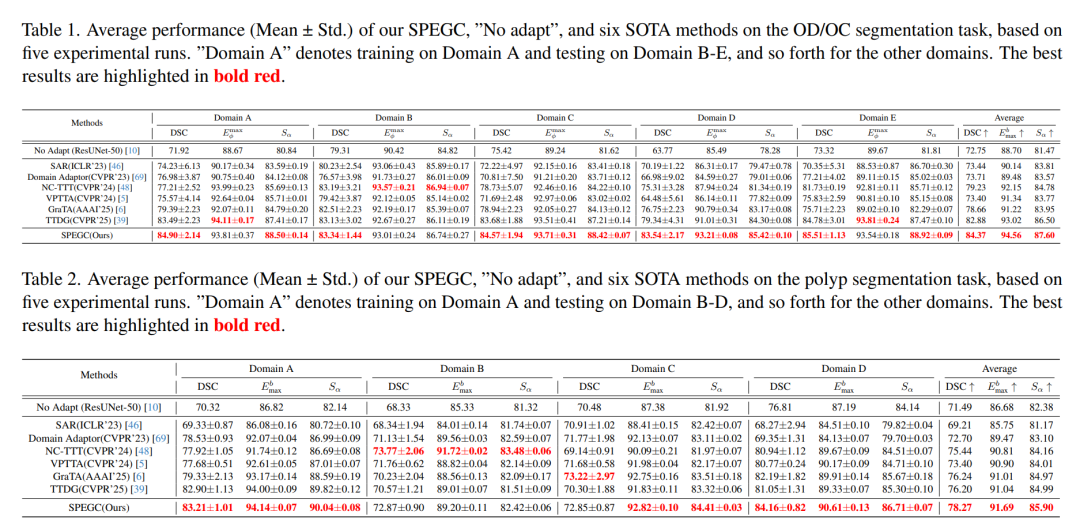
-
基础分割性能领先:在两个2D任务中,SPEGC的平均DICE相似度系数(分割核心指标)均大幅超越SOTA方法,其中眼底分割比次优方法提升1.49%;息肉分割中,部分依赖熵最小化的方法甚至不如无适配基线,而SPEGC凭借数据结构指导,始终保持高分割精度。
-
长期持续适配能力突出:在五轮长期持续适配测试中,SPEGC实现了83.10%的平均DSC,为所有方法最优,同时仅出现1.27%的性能衰减,有效缓解了错误累积和灾难性遗忘,远优于梯度对齐、熵最小化等方法。
-
模块有效性验证:消融实验证明,移除语义提示或图聚类模块后,模型性能会显著下降,而通用+专属的解耦提示池、低不确定性特征采样,是提升模型性能的关键。
-
泛化性强:在混合分布偏移的极端场景(打乱所有目标域数据顺序输入)中,SPEGC仍保持最高分割精度;拓展到3D心脏MRI分割时,相比无适配基线,各组织分割的DSC均有明显提升,边界分割的平均对称表面距离也显著降低。
-
超参数鲁棒性好:核心超参数(聚类数、提示数、损失平衡系数)在合理范围内调整时,模型性能稳定,最优配置下能平衡分割效果和计算效率。
四、优势与局限
核心优势
-
抗干扰性强:通过解耦的语义提示池注入全局信息,让局部特征摆脱域偏移和噪声的影响,特征表征更鲁棒;
-
语义保留能力好:聚类损失约束通用提示池,显式保留跨域核心知识,从根源上缓解灾难性遗忘;
-
监督信号更可靠:基于图聚类得到的高阶结构表征作为监督,替代传统的像素级/实例级信号,避免错误累积;
-
泛化性广:不仅在2D眼底、息肉分割中表现优异,还能拓展到3D医学图像分割,适配不同临床场景;
-
端到端可训练:将图聚类的离散问题转化为可微分的最优运输问题,实现全框架端到端训练,适配流程更高效。
现存局限
SPEGC的可微分图聚类求解器需要构建并精炼特征图的相似度矩阵,计算成本相比轻量型适配方法更高,特征池规模增大时,计算量和GPU显存占用会呈二次方增长,在算力有限的临床设备上部署会受到一定限制。
五、一句话总结
SPEGC通过语义提示增强特征鲁棒性、可微分图聚类挖掘数据结构信息,实现了医学图像分割模型在连续测试数据中的高效、稳定持续自适应,有效解决了域偏移下的错误累积和灾难性遗忘问题,为医疗AI的临床实际部署提供了新的有效方案。