01
文献学习

今天分享的文献是由南方医科大学南方医院、中山大学肿瘤防治中心等团队于2024年5月在肿瘤免疫学领域顶刊《Journal for ImmunoTherapy of Cancer》(中科院1区top,IF=10.6)上发表的研究"Development and interpretation of a pathomics-driven ensemble model for predicting the response to immunotherapy in gastric cancer"即基于病理组学的集成模型在胃癌免疫治疗反应预测中的开发与解读,该研究开发并验证了一种基于病理组学的集成学习模型(PDEM),用于预测胃癌患者对免疫检查点抑制剂(ICIs)的治疗反应。研究使用H&E染色的全切片图像(WSI)提取三类病理组学特征(细胞核、单细胞空间分布、微环境深度特征),并通过集成多个机器学习模型构建预测模型。模型在多个独立队列中表现出优异的预测性能,AUC达0.92以上。SHAP分析和病原组学分析进一步揭示了模型的决策机制和分子基础。
创新点:①直接预测免疫疗效 :区别于建立分子标志物(如MSI、PD-L1)的影像替代物,直接预测胃癌免疫治疗反应 ,避免间接局限性。②集成多维度病理特征 :融合细胞核、单细胞空间分布及微环境深度特征,全面刻画肿瘤微环境异质性 。③模型可解释与分子验证 :结合SHAP分析与病原基因组学,揭示免疫、代谢相关通路驱动机制,提升临床信任度。
临床价值:①低成本非侵入性工具 :基于常规H&E染色切片,无需额外分子检测 ,普适性强,降低医疗成本。②精准筛选获益人群 :优于PD-L1 CPS等传统标志物,识别低CPS仍有效及高CPS无效患者 ,优化治疗决策。③多中心稳健验证 :在多个外部验证集中AUC均>0.91,泛化能力优秀,助力个体化免疫治疗推广。
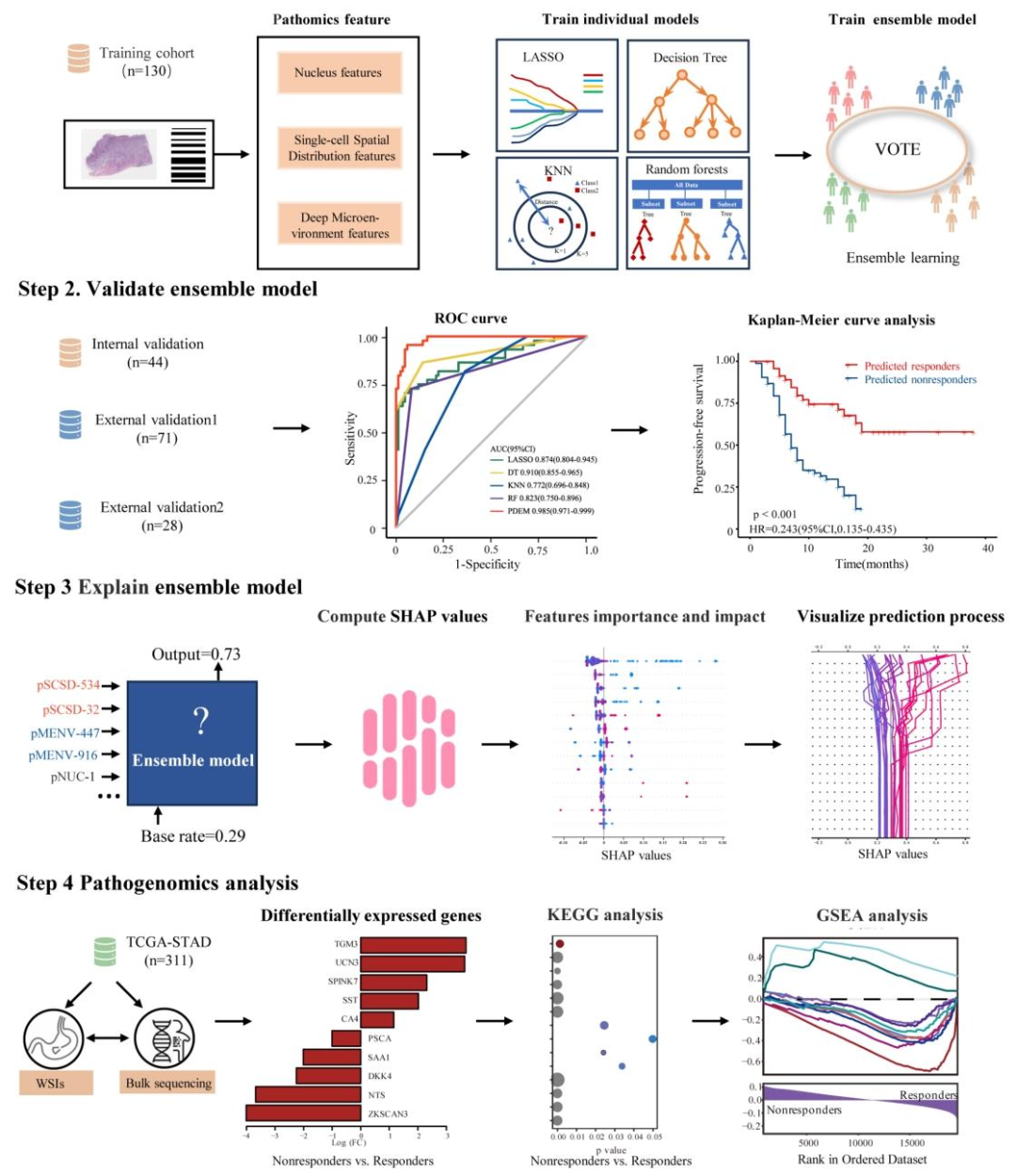
图 1:研究整体工作流程图
研究对象与数据入组
多中心回顾性纳入584例胃癌免疫治疗患者 ,来源:中山大学肿瘤防治中心、南方医科大学南方医院、广东省中医院;另纳入TCGA-STAD队列311例用于分子验证。
病理影像处理
H&E染色全切片影像(WSI)→40×扫描→CLAM算法自动组织分割→病理学家复核ROI(感兴趣区域)。
病理组学特征提取
提取三类互补特征:
pNUC:病理组学细胞核特征(强度、形态、纹理)
pMENV:病理组学深度微环境特征
pSCSD:病理组学单细胞空间分布特征
集成模型构建(Step1)
融合4种机器学习算法 :LASSO、KNN、决策树(DT)、随机森林(RF),通过投票回归器集成输出最终预测结果。
模型验证与解释
性能验证:训练集+内部验证集+2个外部验证集,用ROC/AUC、灵敏度、特异度评估;
可解释性:SHAP分析解析特征贡献;
分子机制:病原组学分析(GSEA/KEGG),关联免疫/肿瘤/代谢通路。
02
研究背景和目的
研究背景
胃癌是全球常见的恶性肿瘤之一,也是癌症相关死亡的第三大原因。免疫检查点抑制剂(ICIs)已成为缺乏靶向治疗选择的胃癌患者的重要治疗手段,然而仅有部分患者能从ICIs治疗中获得长期生存获益。目前临床常用的预测生物标志物如PD-L1表达 、微卫星不稳定性(MSI) 和肿瘤突变负荷(TMB) 存在明显局限性:PD-L1低表达或不表达的患者仍可能从抗PD-L1治疗中获益;MSI-H在晚期胃癌中仅占4%~7%;且这些检测存在样本要求高、标准化不足、成本昂贵等问题。ICIs的疗效受到肿瘤、微环境和宿主因素之间复杂相互作用 的复杂影响。H&E染色的全切片图像(WSI)蕴含丰富的肿瘤微环境信息,病理组学分析 可量化组织微环境、识别与预后和治疗反应相关的形态学特征。既往研究主要集中于建立针对MSI、EBV感染状态或PD-L1表达等特定分子指标的成像替代标志物 ,而非直接利用病理组学特征预测免疫治疗疗效,且忽视了复杂模型的可解释性。因此,亟需开发一种直接、高效且可解释的病理组学模型来精准预测胃癌免疫治疗应答。
研究目的
本研究旨在开发并验证一个基于病理组学的集成模型(PDEM) ,用于直接预测胃癌患者对免疫检查点抑制剂治疗的疗效。研究团队从H&E染色的全切片图像中提取了三类定量病理组学特征:细胞核特征(pNUC) 、单细胞空间分布特征(pSCSD) 和深度微环境特征(pMENV) ,分别从个体细胞形态、细胞空间分布及整体微环境 三个层面全面刻画肿瘤微环境。在此基础上,集成LASSO、K近邻(KNN)、决策树和随机森林 四种分类器构建集成模型,并在多中心队列(共584例患者)中进行训练和验证。模型性能采用AUC、敏感性和特异性 等指标评估。同时,研究采用SHAP分析 对集成模型的预测结果进行解释,量化每个输入特征对预测的贡献。进一步通过病原基因组学分析 (利用TCGA-STAD队列的转录组数据和WSI),探究模型预测背后的分子机制 ,包括免疫相关通路、代谢通路以及免疫评分、肿瘤纯度等免疫微环境特征,旨在为胃癌精准免疫治疗提供一种高精度、鲁棒且可解释的新型预测工具。
03
数据和方法
数据: 本研究为多中心回顾性研究,共纳入584例接受免疫检查点抑制剂治疗的胃癌患者,其中来自中山大学癌症中心的174例被分为训练队列(130例) 和内部验证队列(44例) ,来自南方医科大学南方医院的71例作为外部验证队列1 ,来自广东省中医院的28例作为外部验证队列2 ;此外,从TCGA数据库获取416例胃癌患者(其中311例有高质量基因表达及全切片图像)用于病原组学分析与分子验证。
方法: H&E 染色全切片图像 → 提取三类定量病理组学特征 :细胞核特征(pNUC)、单细胞空间分布特征(pSCSD)、深度微环境特征(pMENV) → 集成模型开发 :采用LASSO、KNN、决策树、随机森林 四个基分类器,通过投票回归器 集成构建预测模型 → 模型验证 :在内部及外部验证队列中评估AUC、灵敏度、特异度 等指标 → SHAP 分析 解释特征重要性及个体预测决策→ 病原组学分析 :对TCGA-STAD数据计算预测分类,进行差异表达基因、KEGG富集、GSEA ,并评估ESTIMATE评分、免疫评分、肿瘤纯度 等免疫相关特征 → 预后分析 :采用Kaplan-Meier曲线 和多因素Cox回归评估模型预测签名对无进展生存期的独立预测价值。
04
实验结果
预测性能:
训练集AUC:0.985
内部验证集AUC:0.921
外部验证集1 AUC:0.914
外部验证集2 AUC:0.927
优于PD-L1(CPS)、SVM、LR等模型
预后价值:
预测响应者的PFS显著优于非响应者
多因素Cox回归显示模型为独立预后因子(HR=0.34)
模型解释:
SHAP分析识别出关键病理特征(如pSCSD-534)
模型决策过程可视化
分子机制:
预测响应者富集于免疫相关通路(如干扰素γ、炎症反应)
高免疫评分、低肿瘤纯度
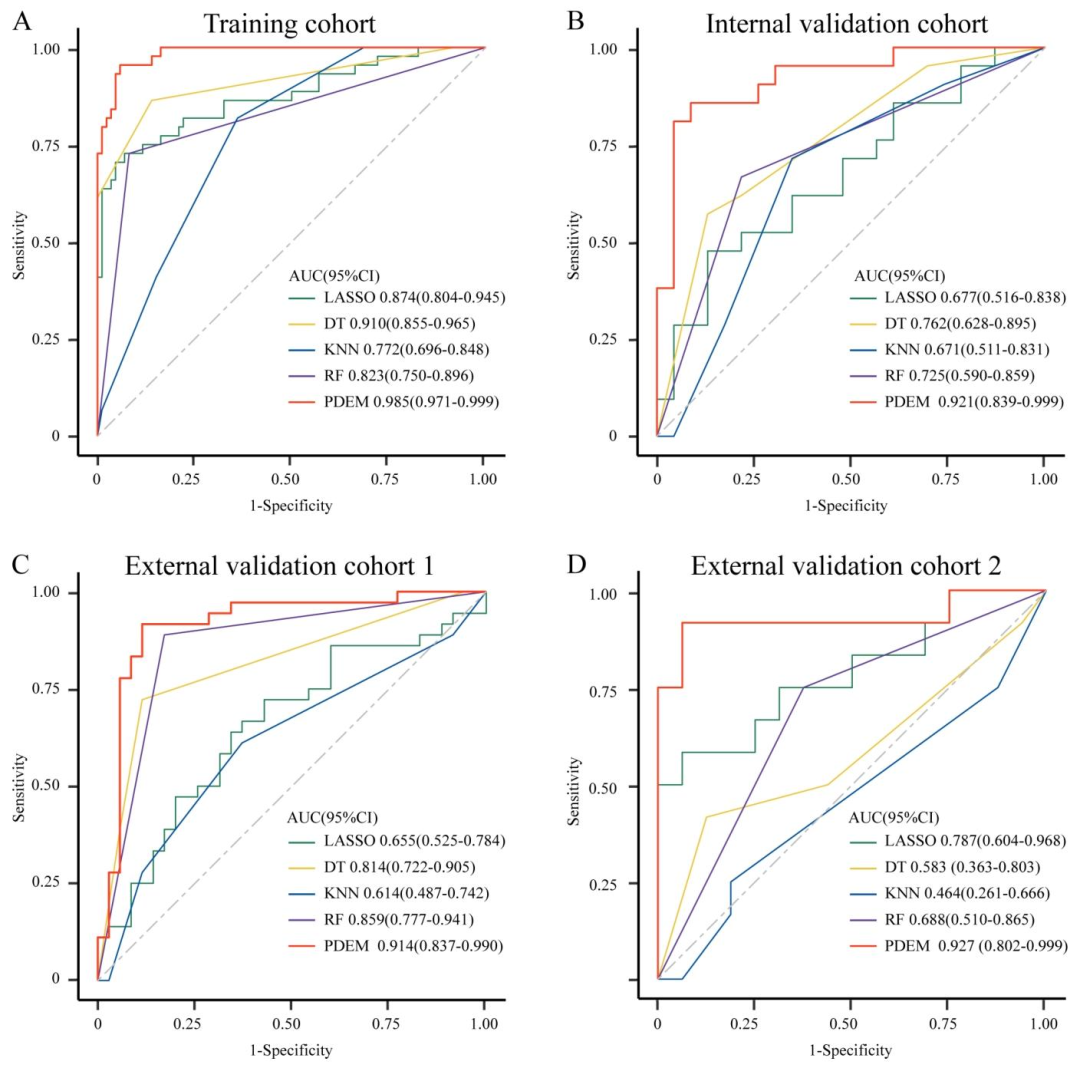
图 2:集成模型与单一模型预测性能的ROC曲线对比
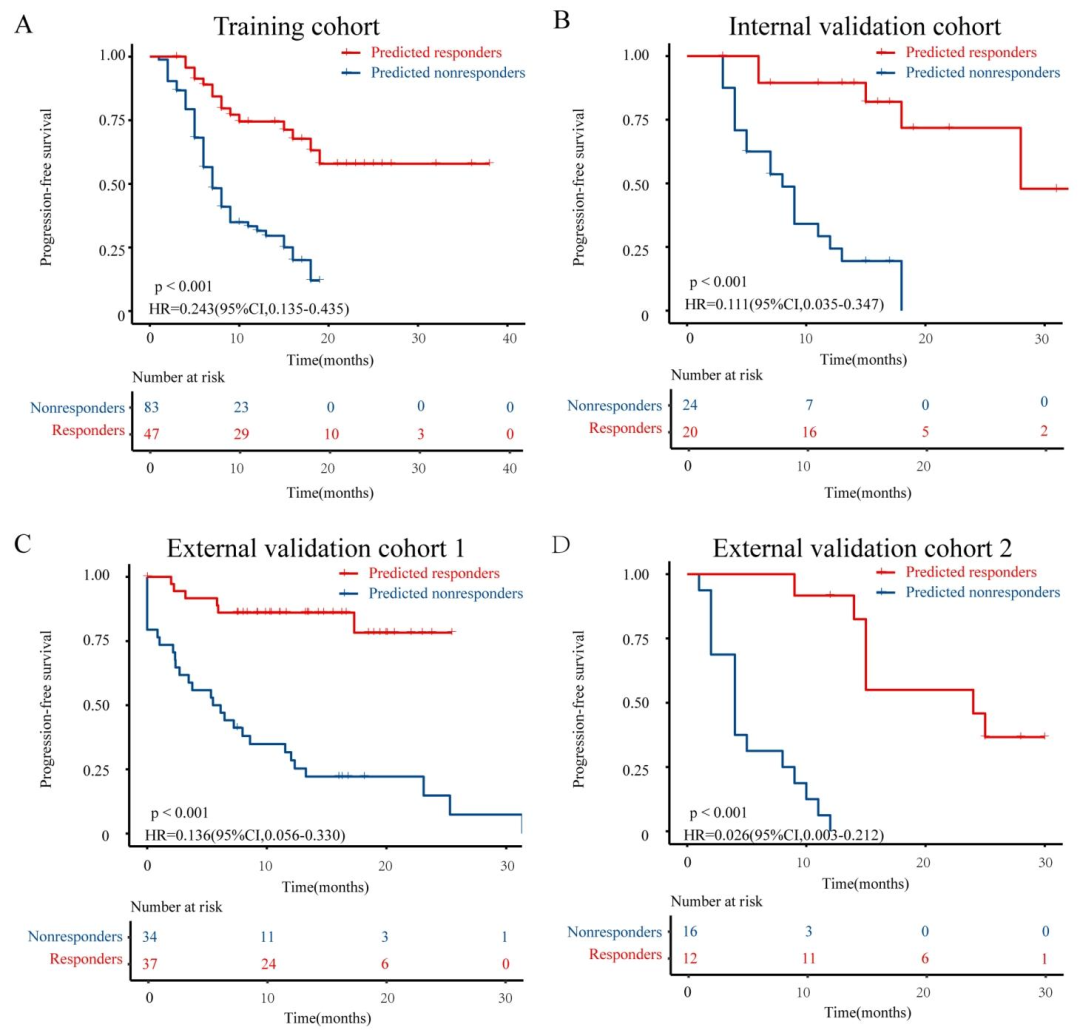
图 3:无进展生存期(PFS)的Kaplan-Meier生存曲线
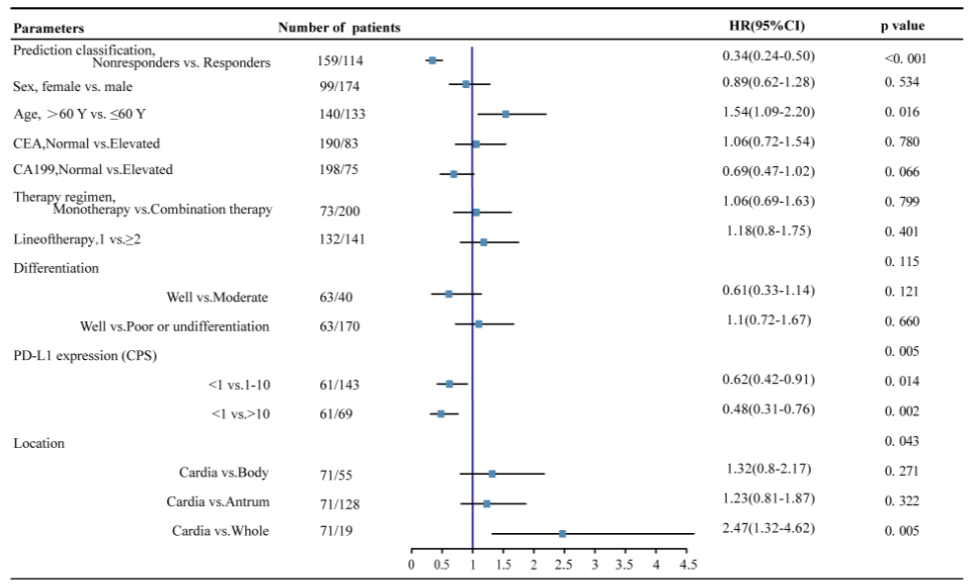
图 4:多因素Cox回归森林图(PFS)
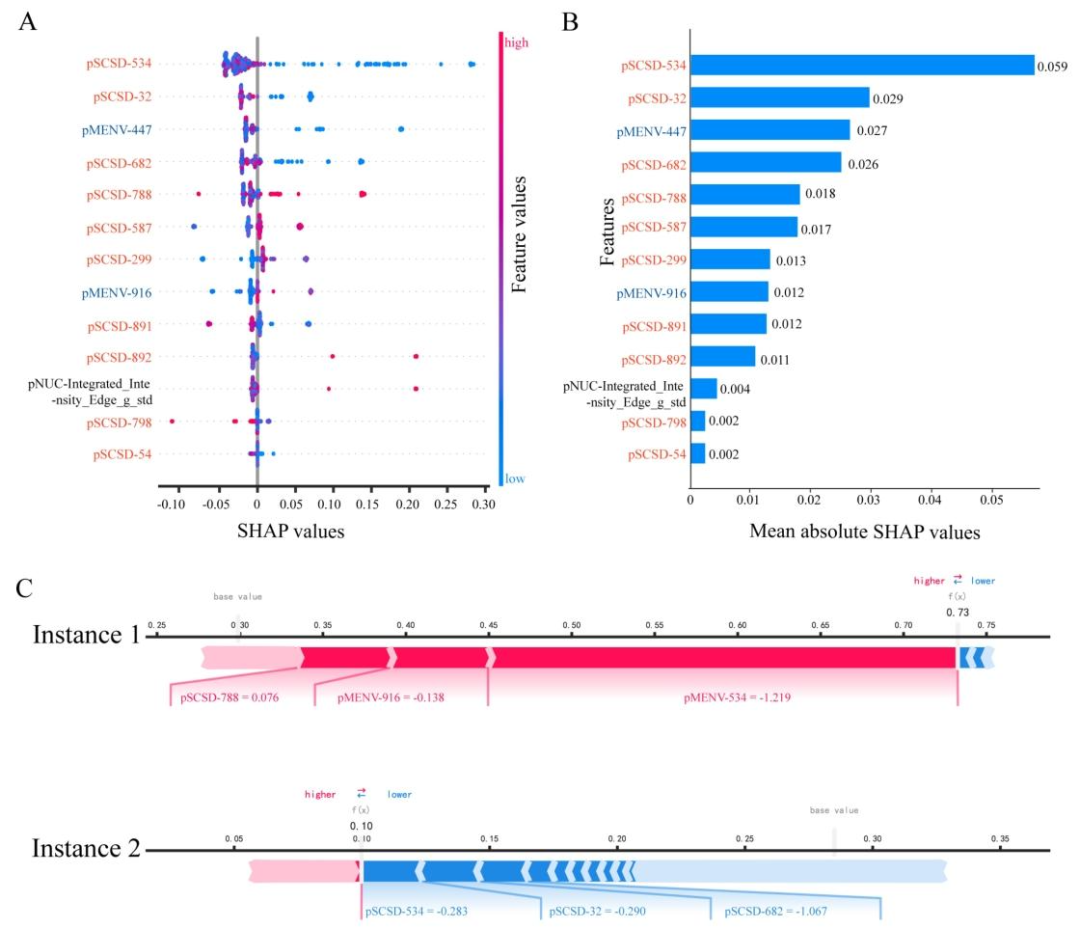
图 5:SHAP解析病理组学集成模型
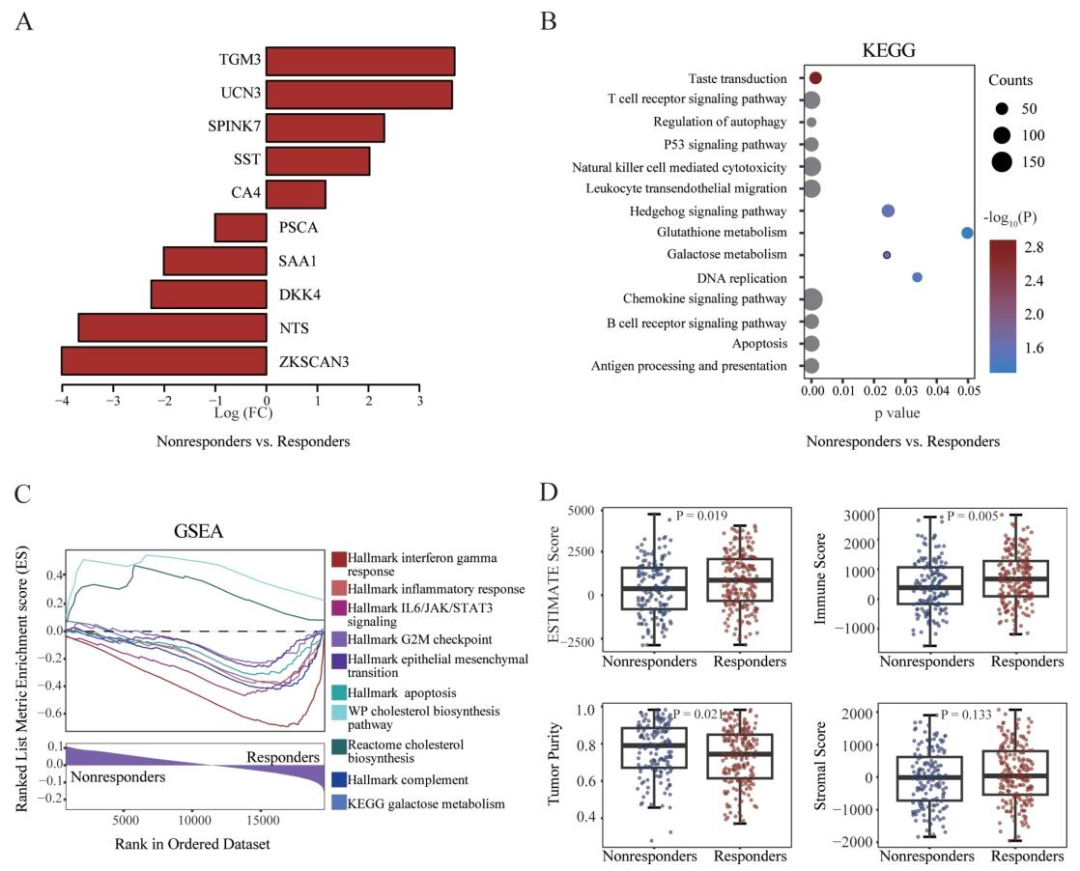
图 6:病理组学集成模型的病原组学分析
05
研究结论
该研究成功开发并验证了一个基于病理组学的集成模型(PDEM) ,用于预测胃癌患者对免疫检查点抑制剂(ICIs)的治疗反应。通过多中心回顾性分析584例患者的H&E染色全切片图像,提取细胞核、单细胞空间分布及微环境深度特征,并整合LASSO、KNN、决策树和随机森林四种分类器,PDEM在训练集及三个验证集中均表现出极高的预测性能 (AUC达0.921~0.985),显著优于传统的PD-L1联合阳性评分(CPS)及其他单一机器学习模型。该模型能有效区分免疫治疗的响应者与非响应者 ,且预测标签是患者无进展生存期的独立预后因素 (HR=0.34, p<0.001)。借助SHAP分析,模型决策过程得以解释,关键病理特征如pSCSD-534对预测贡献最大。进一步的病原组学分析揭示,模型所区分的响应组富集了免疫相关通路(如补体、干扰素γ应答)、肿瘤抑制通路(如凋亡、G2/M检查点)及半乳糖代谢通路,而非响应组则富集胆固醇生物合成通路;同时响应者表现出更高的免疫评分和更低的肿瘤纯度。综上,PDEM作为一种无创、可解释且高精度的预测工具,为胃癌精准免疫治疗提供了有力支持,但仍需前瞻性大样本研究验证其临床适用性。
参考文献:Han Z, Zhang Z, Yang X, Li Z, Sang S, Islam MT, Guo AA, Li Z, Wang X, Wang J, Zhang T, Sun Z, Yu L, Wang W, Xiong W, Li G, Jiang Y. Development and interpretation of a pathomics-driven ensemble model for predicting the response to immunotherapy in gastric cancer. J Immunother Cancer. 2024 May 15;12(5):e008927. doi: 10.1136/jitc-2024-008927.