01
文献学习

今天分享的文献是由复旦大学附属金山医院强金伟教授等团队于2026年4月3日在《Radiology: Imaging Cancer》(中科院2区,IF=6.3)上发表的研究"Multiparametric MRI-based Deep Learning and Radiomics for Evaluating Lymph Node Metastasis in Early-Stage Cervical Cancer"即基于多参数MRI的深度学习和影像组学评估早期宫颈癌淋巴结转移,该研究是一项多中心回顾性研究,旨在利用术前多参数MRI图像,分别基于影像组学和深度学习-影像组学融合方法,构建预测早期宫颈癌淋巴结转移(LNM)的模型。研究纳入862例患者,分为训练集、内部测试集和外部测试集。结果显示,联合肿瘤和淋巴结的影像组学模型(Rad_T+LN)在外部测试集中AUC达0.77,而加入深度学习特征后模型性能未显著提升。两个模型均具有良好的校准度和临床净获益,且敏感性显著高于放射科医师。
创新点:①首次融合原发灶与淋巴结 的多参数MRI影像组学和深度学习特征,预测早期宫颈癌淋巴结转移。② 构建影像组学-深度学习融合模型 ,系统比较2D与3D特征性能,并经独立外部验证。③ 针对小淋巴结(<10mm)等难题进行亚组分析,揭示模型在常规影像漏诊病例中的优势。
临床价值:① 术前无创预测淋巴结转移,可避免不必要的淋巴结清扫术 及相关手术并发症。② 模型敏感性显著优于放射科医生 (最高提升至75.8%),有效降低漏诊风险。③ 提供个体化辅助决策工具,帮助区分早期手术与放化疗适应人群,优化治疗策略。
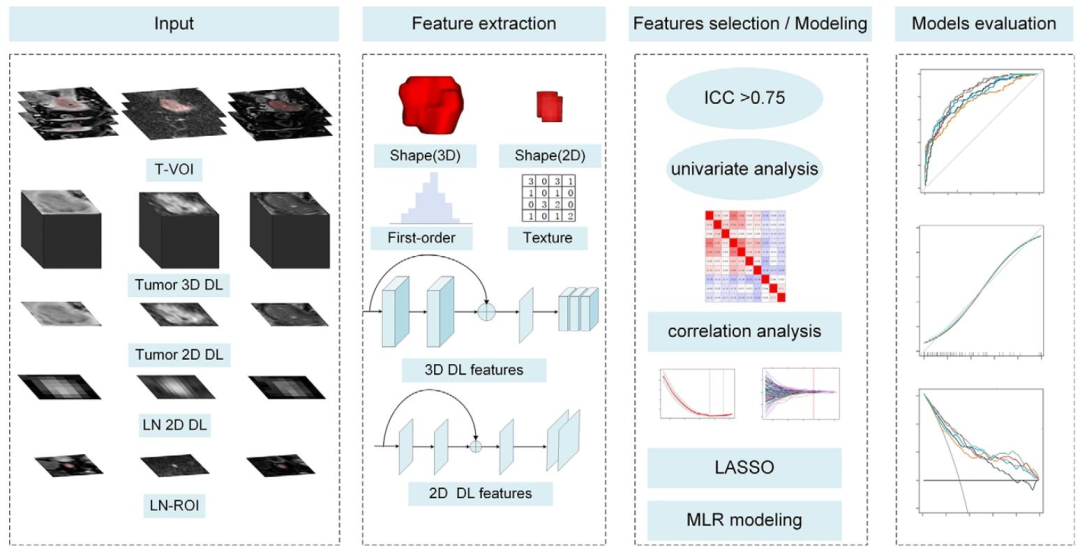
图 2:宫颈癌淋巴结转移预测模型构建技术流程图
数据输入
影像:多中心多参数MRI(T2WI、DWI、增强T1WI)
临床:年龄、SCCA、FIGO分期等
病理:淋巴结转移状态(金标准)
图像分割
肿瘤:逐层手动勾画ROI→自动生成3D肿瘤体积感兴趣区(T-VOI)
淋巴结:选取最大短径可疑淋巴结,勾画2D最大截面ROI(LN-ROI)
一致性验证:组内/组间ICC>0.75的特征才保留,保证分割可靠性
特征提取
影像组学:提取肿瘤3D+淋巴结2D的多序列组学特征
深度学习:ResNet50提取2D深度特征 ;Med3D提取3D深度特征
数据校正:ComBat方法消除多中心MRI设备、扫描参数的差异
特征筛选
初筛:Mann-Whitney U检验(P<0.01)+Spearman相关性过滤(r>0.8剔除)
降维:LASSO算法
模型构建(多因素逻辑回归)
单部位组学:Rad_T(仅肿瘤)、Rad_LN(仅淋巴结)
联合组学:Rad_T+LN(肿瘤+淋巴结)
深度融合:DLR(2D)_T+LN、DLR(3D)_T+LN
临床融合:DLRC(2D)(融合SCCA)
模型评估:ROC曲线、校准曲线、决策曲线、亚组分析、误差分析
02
研究背景和目的
研究背景
宫颈癌是全球女性第四大常见恶性肿瘤,淋巴结转移(LNM) 是其关键的预后因素。LNM阳性患者的复发风险高达37.5%,5年生存率仅20%~60%,而阴性患者的复发风险仅为6.66%,生存率超过90%。2018年FIGO分期将影像学(MRI、CT、PET/CT)纳入LNM评估,一旦确诊LNM即分期上调至IIIC期。对于早期宫颈癌(≤IIA期),首选根治性手术;而晚期(≥IIB期)则推荐放化疗。然而,约10%~30%的早期患者术后病理证实存在LNM ,这意味着大量患者接受了无效的淋巴结清扫术,承受着出血、感染、淋巴囊肿、下肢淋巴水肿等并发症风险。目前LNM诊断的金标准是术后病理,属于有创检查;临床常用MRI因软组织分辨率高而被广泛应用,但其汇总灵敏度仅57% ,存在明显局限。近年来,影像组学 通过高通量特征提取将医学图像转化为定量生物标志物,深度学习 则能直接获取图像特征,两者在肿瘤预测中展现出潜力。既往研究多仅从原发肿瘤提取影像组学特征构建LNM预测模型,尚未有研究联合原发肿瘤和淋巴结的影像组学及深度学习特征对宫颈癌LNM状态进行分析。
研究目的
本研究旨在基于多参数MRI ,开发两种术前预测早期宫颈癌淋巴结转移的模型:一是仅利用影像组学特征 的模型,二是融合深度学习与影像组学(DLR) 的模型。与既往研究不同,本研究同时纳入原发肿瘤和盆腔可疑淋巴结 两大感兴趣区,分别提取其影像组学和深度学习特征,以全面捕捉与LNM相关的影像信息。具体而言,研究构建了基于肿瘤三维影像组学特征的模型(Rad_T)、基于淋巴结二维影像组学特征的模型(Rad_LN),以及联合两者的组合模型(Rad_T+LN)。在此基础上,进一步融合ResNet50提取的二维深度学习特征和Med3D提取的三维深度学习特征,构建DLR_T+LN融合模型 ,并探索加入临床变量(如鳞状细胞癌抗原SCCA水平)能否提升性能。通过多中心回顾性研究 (862例患者,分为训练集、内部测试集和外部测试集),采用ROC曲线、校准曲线、决策曲线等评估模型的诊断效能、校准度和临床净收益,旨在验证联合肿瘤与淋巴结的多参数MRI影像组学及深度学习模型能否提高术前预测LNM的准确性,从而辅助临床制定个体化治疗策略、改善患者预后。
03
数据和方法
研究数据
数据来源:五家医疗中心(复旦大学附属金山医院、妇产科医院、肿瘤医院、同济大学附属第一妇婴保健院、上海交通大学医学院附属国际和平妇幼保健院)
时间范围:2020年1月至2022年12月
纳入患者:共862例早期宫颈癌女性患者(中位年龄53岁)
分组:训练集381例,内部测试集162例,外部测试集319例
LNM阳性率:训练集31.5%,内部测试集31.5%,外部测试集32.6%
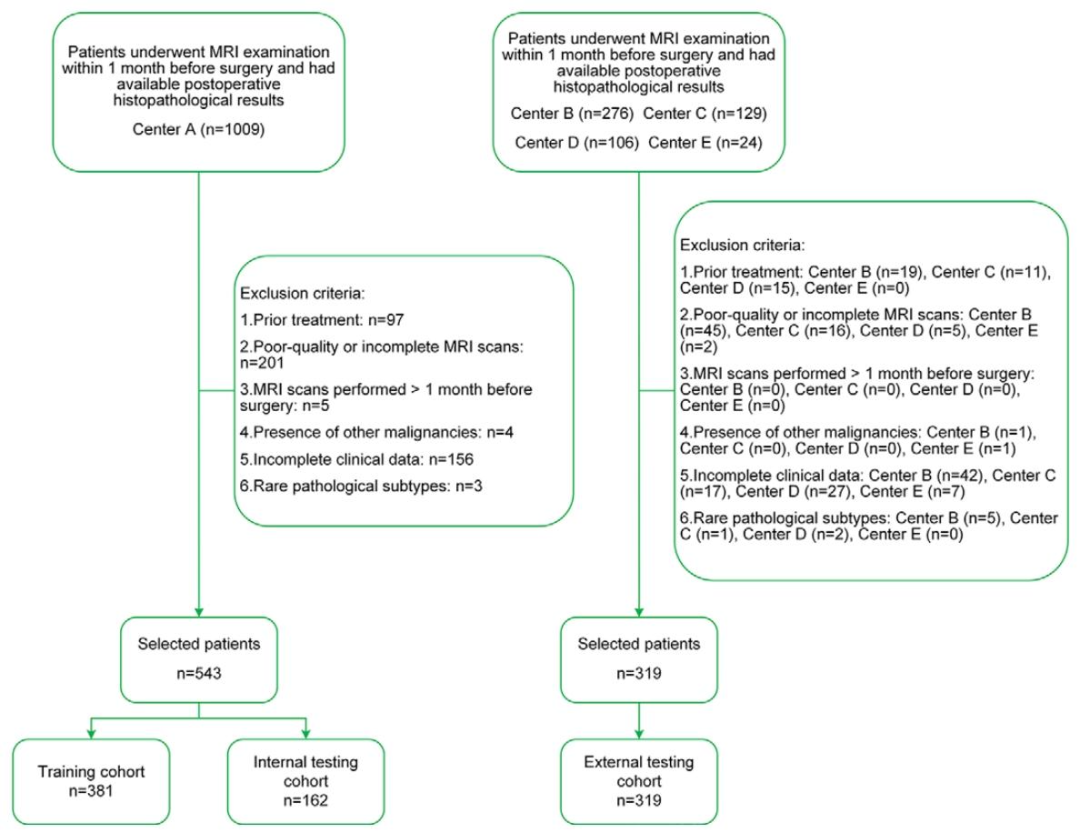
图 1:五中心宫颈癌患者纳入与排除流程图
技术方法
图像序列:多参数MRI(T2WI、DWI、T1CE)
特征提取:
影像组学特征:从肿瘤(3D)和淋巴结(2D)分别提取
深度学习特征:使用预训练ResNet50(2D)和Med3D(3D)网络提取
特征校正:ComBat方法消除多中心扫描差异
模型构建:
Rad_T:仅肿瘤影像组学
Rad_LN:仅淋巴结影像组学
Rad_T+LN:联合肿瘤+淋巴结影像组学
DLR(2D)_T+LN:联合肿瘤+淋巴结的影像组学+2D DL特征
DLR(3D)_T+LN:进一步加入3D肿瘤DL特征
DLRC(2D):加入临床特征(SCCA水平)
特征选择:Mann-Whitney U检验、Spearman相关性、LASSO回归、逐步逻辑回归
评估指标:AUC、准确性、敏感性、特异性、校准曲线、决策曲线分析
04
实验结果
Rad_T+LN模型:训练集AUC 0.81 (0.76--0.86),内部测试0.79 (0.72--0.87),外部测试0.77 (0.71--0.82)。在外部测试中显著优于单独肿瘤模型(P=0.04)和单独淋巴结模型(P=0.02)。
DLR(2D)_T+LN模型:训练集AUC 0.84 (0.80--0.88),内部测试0.83 (0.76--0.91),外部测试0.79 (0.74--0.84)。与Rad_T+LN相比无显著提升(P>0.05)。
DLR(3D)_T+LN模型:与2D版本性能相当(P>0.05)。
加入临床特征:未改善模型性能(P>0.05)。
与放射科医师比较:模型敏感性显著提高(外部测试中Rad_T+LN敏感性69.2% vs. 医师39.4%),但特异性和阳性预测值较低。
校准与决策曲线:模型校准良好,在较宽阈值范围内提供正向净临床获益。
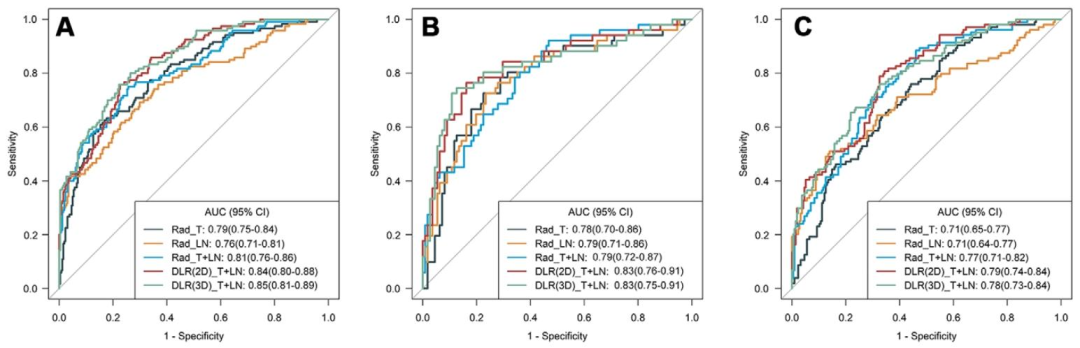
图 3:各模型在训练、内部测试、外部测试队列的ROC曲线
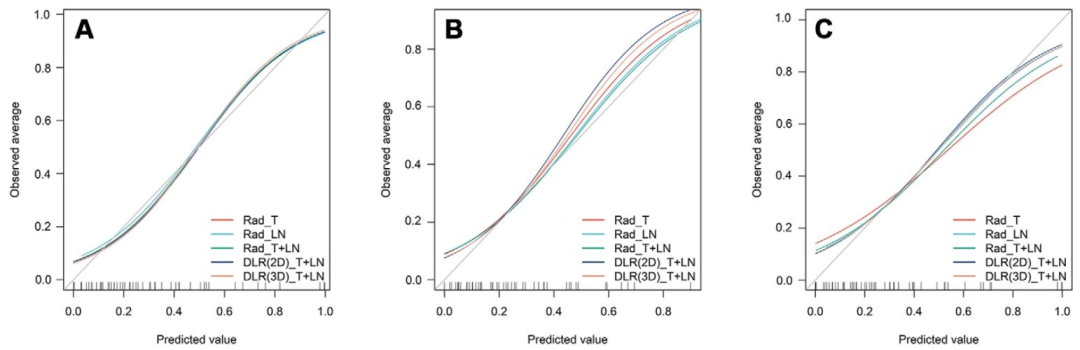
图 4:各模型在三个队列的校准曲线
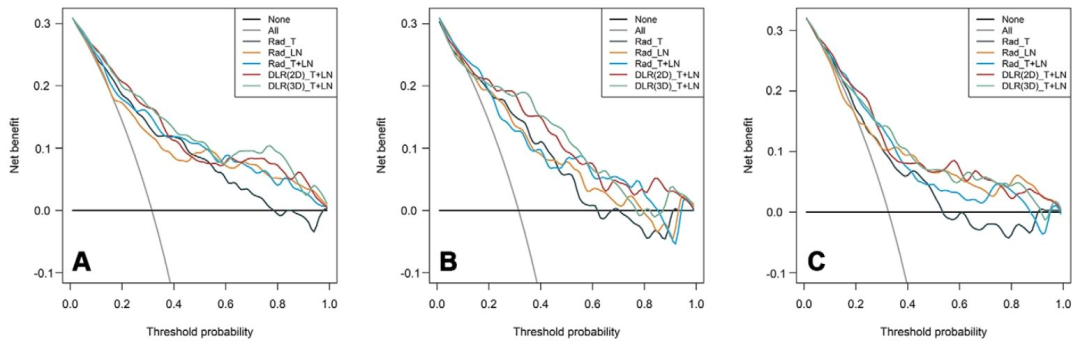
图 5:各模型在三个队列的决策曲线
05
研究结论
该研究证明基于肿瘤和淋巴结的放射组学特征 构建的联合模型(Rad_T+LN)以及融合深度学习与放射组学 的模型(DLR_T+LN),均能在术前较准确地预测早期宫颈癌的淋巴结转移状态。在外部测试队列中,Rad_T+LN模型的AUC为0.77,DLR(2D)_T+LN模型的AUC为0.79,两者诊断性能无显著差异 ,且均优于仅基于肿瘤或仅基于淋巴结的单源模型。值得注意的是,这些模型在灵敏度方面显著优于临床放射科医生 ,尤其在识别直径小于10毫米的小淋巴结转移 或单侧转移 等挑战性场景下表现突出,有助于降低漏诊风险 。然而,模型的特异性和阳性预测值相对较低 ,主要受限于MRI图像层厚较厚导致的容积效应、微转移灶难以识别以及良性增生等生物学重叠因素。此外,添加深度学习特征或临床指标(如SCCA水平)未能进一步提升预测效能。总体而言,所建模型可作为术前辅助诊断工具,指导个体化治疗决策,但未来需结合自动分割技术、薄层扫描及前瞻性研究来优化其临床适用性和可解释性。
参考文献:Bao YH, Xiao ML, Li YA, Ma FH, Chen Y, Lin ZJ, Wu JY, Zhang GF, Qiang JW. Multiparametric MRI-based Deep Learning and Radiomics for Evaluating Lymph Node Metastasis in Early-Stage Cervical Cancer. Radiol Imaging Cancer. 2026 May;8(3):e250345. doi: 10.1148/rycan.250345.