01
文献学习

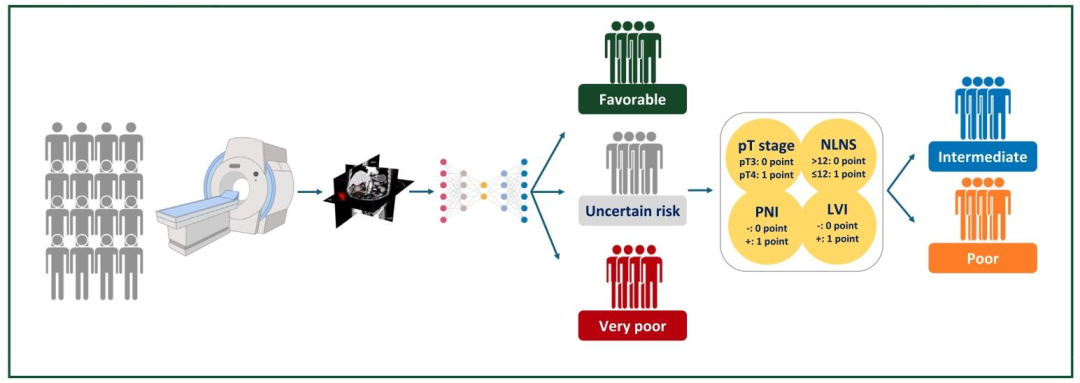
今天分享的文献是由广东省人民医院放射科刘再毅等团队联合 **南方医科大学 **、**山西省肿瘤医院 **、**中国医科大学第一医院 **、广西医科大学肿瘤医院 、重庆医科大学第一附属医院 等团队 于2025年7月在肿瘤学领域顶级期刊《Annals of Oncology》(中科院1区top,IF=65.4) 上发表的研究"Enhanced risk stratification for stage II colorectal cancer using deep learning-based CT classifier and pathological markers to optimize adjuvant therapy decision"即基于深度学习的CT分类器结合病理标志物增强II期结直肠癌风险分层以优化辅助治疗决策,该研究旨在开发一个整合术前CT影像深度学习分析与术后病理标志物的新型风险分层系统(IRIS-CRC),以更精准地识别II期结直肠癌患者中哪些人真正需要辅助化疗,从而避免过度治疗或治疗不足。
创新点:①多平面深度学习架构创新 :采用Swin Transformer构建多平面CT基础模型,通过平面特异性微调与投票机制,提升影像特征提取的全面性与稳健性。②影像-病理融合分层策略 :首次将深度学习CT分类器与指南病理标志物结合,构建四层风险分层系统(IRIS-CRC),实现从三组到四组的精准再分层。③可解释性与临床适配性设计:通过放射基因组学分析揭示风险组生物学差异,并开发用户友好界面,支持临床直接输入与风险评估,提升系统可操作性。
临床价值:①精准识别化疗获益人群 :显著减少过度治疗,将27.1%传统高危患者降为低危,同时识别出6.5%传统低危患者为极高危,优化治疗决策。②提升分层判别能力与预后预测 :IRIS-CRC的C指数显著高于传统系统,实现四个预后组明显区分,DFS差异显著,助力个体化预后评估。③跨中心与治疗场景适用性强:在多个外部验证集中表现一致,无论患者是否接受化疗,均保持稳定分层能力,具备临床推广潜力。
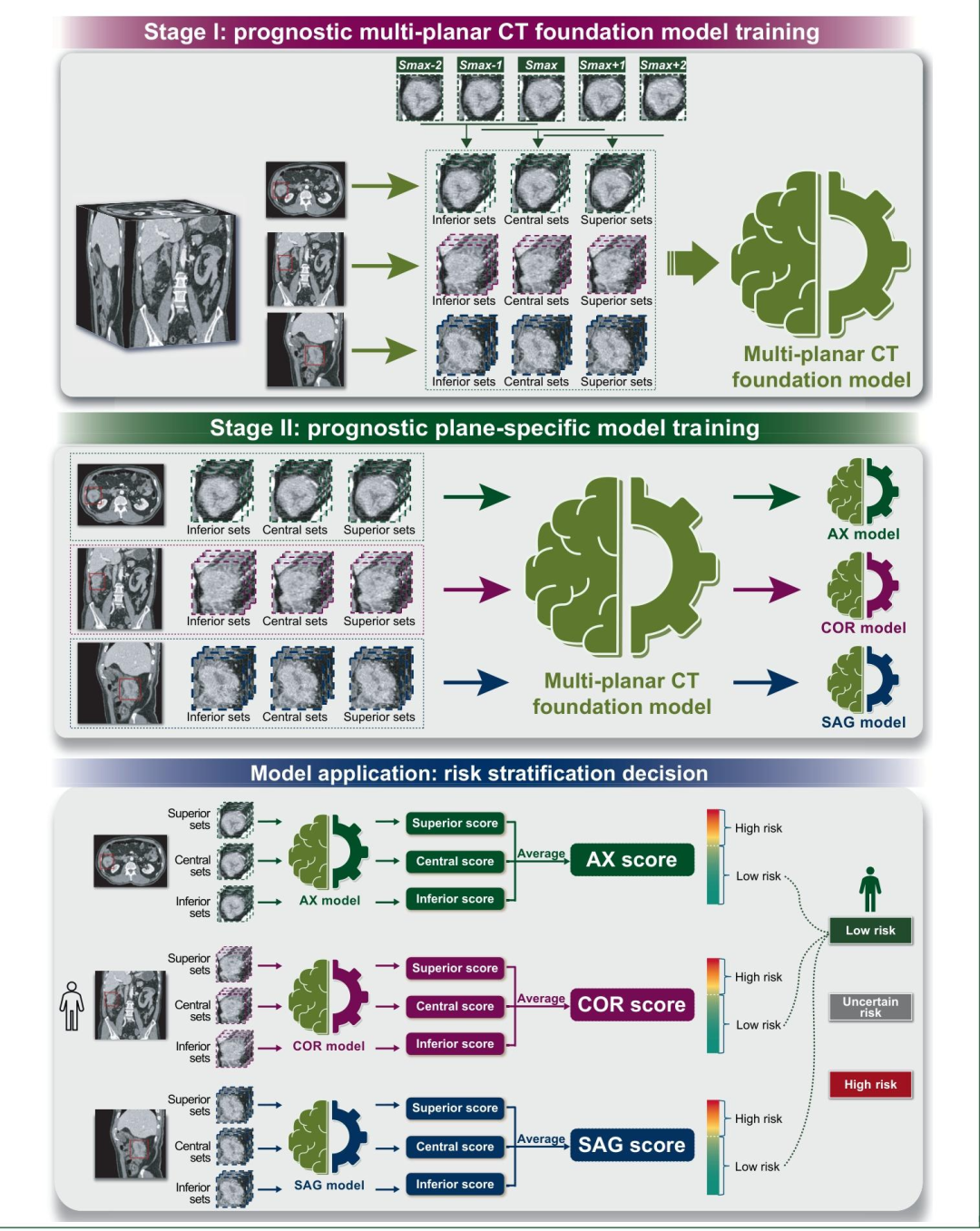
图 1:STAR-CRC深度学习模型的构建流程
展示基于Swin Transformer的CT影像分类器(STAR-CRC)的两阶段训练逻辑及风险分层决策机制,为IRIS-CRC系统提供基础影像分层工具。
第一阶段:多平面CT基础模型训练(上面板)
输入数据:结直肠癌患者术前多平面CT图像(轴向、冠状、矢状位);
核心操作:提取每个解剖平面中"肿瘤最大横截面切片(Smax)"及其相邻2层切片(Smax-2、Smax-1、Smax+1、Smax+2),分为上、中、下三组(Superior/Central/Inferior sets);
输出结果:训练得到可捕捉肿瘤多维度特征的基础模型,为后续细化模型提供统一特征框架。
第二阶段:平面特异性模型微调(中面板)
将基础模型分别针对轴向(AX)、冠状(COR)、矢状位(SAG)图像进行微调,生成3个独立的平面特异性模型;
模型应用:风险分层决策(下面板)
评分计算:对每个平面的上、中、下三组切片分别输入对应平面模型,生成3个切片评分,取平均值作为该平面的最终评分;
二分类与投票机制:通过训练集中的"最小log-rank P值法"确定最佳阈值,将平面评分转化为"低危/高危"二分类结果;
一致低危(3个模型均判定低危)→低危组;
一致高危(3个模型均判定高危)→高危组;
存在分歧(任意模型判定结果不同)→不确定风险组;
02
研究背景及目的
研究背景
结直肠癌(CRC)是全球第三大常见癌症,也是癌症相关死亡的第二大原因,其临床管理尤其在二期结直肠癌 中面临重大挑战。当前二期CRC的辅助化疗决策主要依赖于传统的临床病理特征(如pT分期、淋巴结采样数、淋巴血管侵犯等),但这些特征在识别真正受益于辅助化疗的患者方面准确度有限 。多项系统评价和临床试验表明,辅助化疗仅能提高约3%-5%的生存率和无病生存率 ,且常伴随着显著的毒副作用,导致部分低风险患者被过度治疗 ,而高风险患者则可能治疗不足 。尽管已有一些组织生物标志物(如免疫评分、Oncotype DX等)显示出一定的预后价值,但其临床应用仍受限于成本效益、可及性及预测效能的不一致性 。与此同时,CT影像在CRC的诊断与随访中扮演关键角色,而基于人工智能尤其是深度学习的影像分析技术,能够从多平面CT图像中提取与肿瘤行为和患者预后相关的影像生物标志物 ,为风险分层提供新的维度。因此,亟需一种能够整合影像信息与病理特征的精准分层系统,以弥补当前指南依赖系统的不足,实现个体化治疗决策,优化患者结局。
研究目的
本研究旨在构建一个更为精确、个性化的风险分层系统 ,以优化二期结直肠癌患者的辅助治疗决策。具体目标包括:首先 ,开发一个基于术前多平面CT影像的深度学习分类器------STAR-CRC (Swin Transformer Assisted Risk-stratification for CRC),该模型通过训练多平面CT基础模型并进行平面特异性微调,能够将患者分为低风险、不确定风险和高风险 三类;其次 ,针对STAR-CRC中分类为"不确定风险"的患者群体,进一步结合指南推荐的病理标志物(包括pT4分期、淋巴结采样数≤12、神经周围侵犯和淋巴血管侵犯 ),构建一个复合评分,从而实现对这一亚组的再分层;最终 ,将影像分类结果与病理评分整合,形成一个四层风险分层系统------IRIS-CRC (Intelligent Risk Integration System for Stage II Colorectal Cancer),将患者分为良好、中等、不良和极差预后组。该系统旨在显著提高风险分层的判别能力与临床适用性 ,力求准确识别那些可安全避免辅助化疗的低风险患者,同时甄别出需接受更积极治疗的高风险人群,从而在保证疗效的前提下减少不必要的治疗相关毒性,推动二期结直肠癌的精准医疗进程。
03
数据和方法
研究数据
**研究对象:**12个中心的2992例II期结直肠癌患者(均为R0切除,手术切缘阴性);
数据分组:
训练集+内部验证集:1587例(4个中心,2012年10月-2020年12月),按7:3分为训练集(1110例)和内部验证集(477例);
外部验证集:1405例(8个中心,2012年4月-2020年12月),用于独立模型评估;
数据类型:
临床病理数据:年龄、性别、pT分期、淋巴结取样数(NLNS)、肿瘤分化程度、神经侵犯(PNI)、脉管侵犯(LVI)、辅助化疗情况等;
影像数据:术前多平面(轴向、冠状、矢状位)CT图像;
分子数据:53例患者的批量RNA测序数据(用于生物学基础分析);
**主要终点:**3年无病生存期(DFS,从手术到复发、转移或任何原因死亡的时间);次要终点:总生存期(OS)。
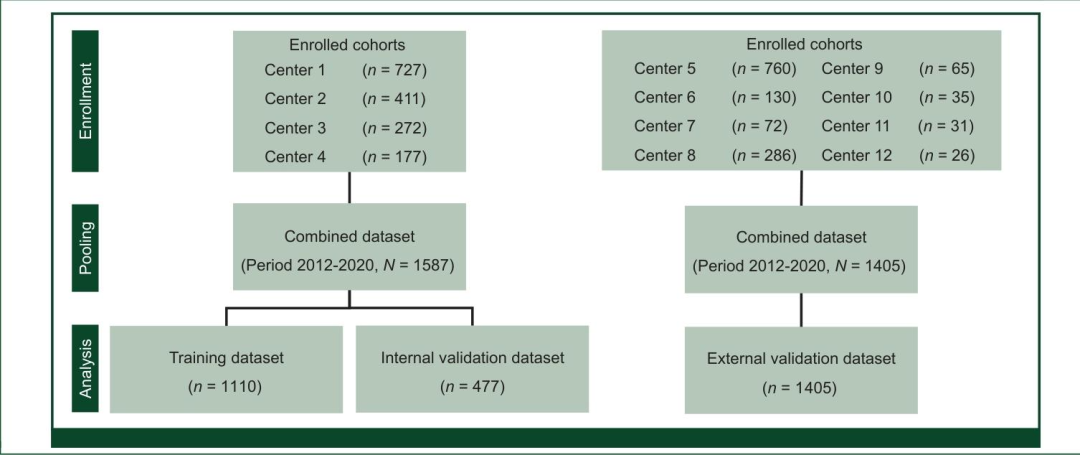
图 2:患者分组流程图
技术方法
(1)STAR-CRC深度学习模型开发
基于Swin Transformer构建两阶段多平面模型:
第一阶段:训练多平面CT基础模型,整合轴向、冠状、矢状位图像特征;
第二阶段:微调为3个平面特异性模型(AX/COR/SAG),输入每个平面的上、中、下三层切片图像,生成切片评分并平均为平面评分;
投票机制:通过最佳阈值将平面评分二分类(低危/高危),一致低危为低危组,一致高危为高危组,存在分歧为不确定风险组。
(2)IRIS-CRC风险分层系统构建
对STAR-CRC的不确定风险组,采用病理标志物复合评分:pT4分期(1分)、NLNS≤12(1分)、PNI阳性(1分)、LVI阳性(1分),总分0-4分;
评分0-1分为中间风险组,≥2分为差风险组;
最终IRIS-CRC分为四组:良好预后组(STAR-CRC低危)、中间预后组(不确定风险+评分0-1)、差预后组(不确定风险+评分≥2)、极差预后组(STAR-CRC高危)。
(3)模型评估与比较
对照系统:GRSS-CRC(基于ESMO/NCCN指南,纳入pT分期、NLNS、PNI、LVI,分为低危、中间危、高危);
统计方法:C指数(评估区分度)、Kaplan-Meier生存分析(比较各组DFS)、Cox比例风险回归(验证独立性)、多重插补处理缺失数据、倾向评分匹配(分析化疗获益)。
(4)分子机制探索
对53例患者的RNA测序数据进行放射基因组学分析,比较不同风险组的基因表达差异和通路富集情况。
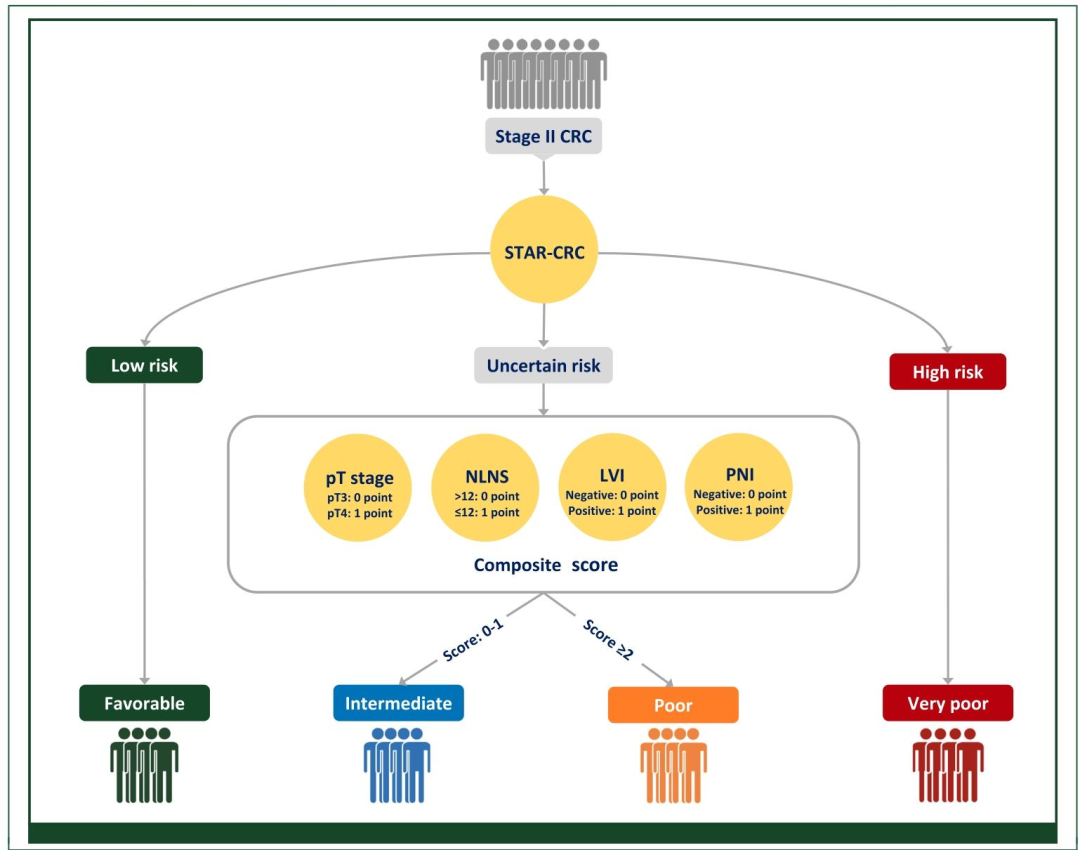
图 3:IRIS-CRC风险分层系统的核心框架图
第一步:STAR-CRC初步分层
输入:术前多平面CT图像;
输出:将患者分为三类:低危组、不确定风险组、高危组。
第二步:病理标志物评分细化(针对不确定风险组)
纳入的病理指标(均来自术后病理报告)及评分规则:
pT分期:pT3(0分)、pT4(1分);
淋巴结取样数(NLNS):>12个(0分)、≤12个(1分);
神经侵犯(PNI):阴性(0分)、阳性(1分);
脉管侵犯(LVI):阴性(0分)、阳性(1分);
评分范围:0-4分,设定阈值:0-1分为"中间风险",≥2分为"差风险"。
第三步:最终四层级风险分组
良好预后组(Favorable):STAR-CRC低危组(无需病理评分);
中间预后组(Intermediate):STAR-CRC不确定风险组+病理评分0-1分;
差预后组(Poor):STAR-CRC不确定风险组+病理评分≥2分;
极差预后组(Verypoor):STAR-CRC高危组(无需病理评分)。
04
实验结果
- IRIS-CRC在外部验证中表现出优异的预后分层能力,四组患者的3年DFS率分别为>95%、95%--75%、75%--55%、<55%。
- 与GRSS-CRC相比,IRIS-CRC将27.1%的原高危患者降级为良好预后组,将6.5%的原低危患者升级为极差预后组。
- 在化疗与非化疗患者中,IRIS-CRC均保持稳定的分层能力。
- 分子分析显示低危组免疫活性增强,高危组细胞周期通路激活。
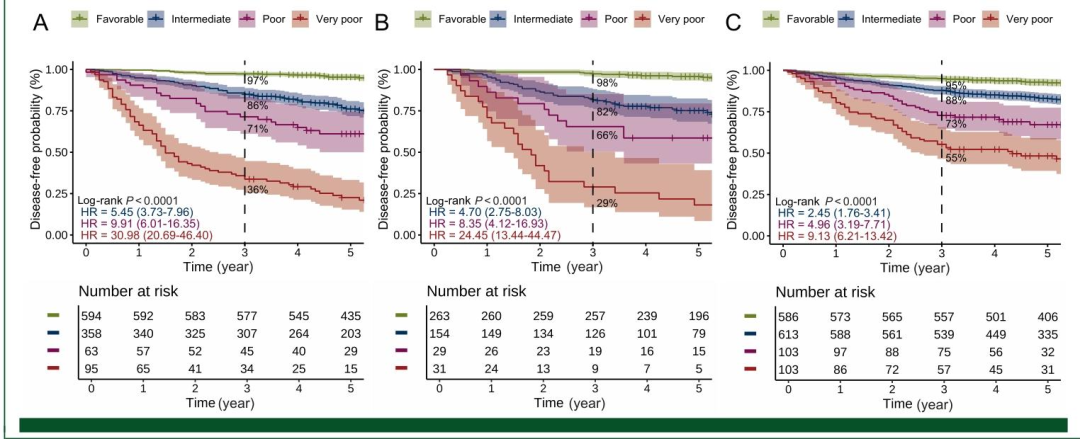
图 4:IRIS-CRC系统在三个数据集的生存分析曲线
通过Kaplan-Meier生存曲线,验证IRIS-CRC四层级风险分组的预后区分能力,展示不同风险组的3年无病生存期(DFS)差异。
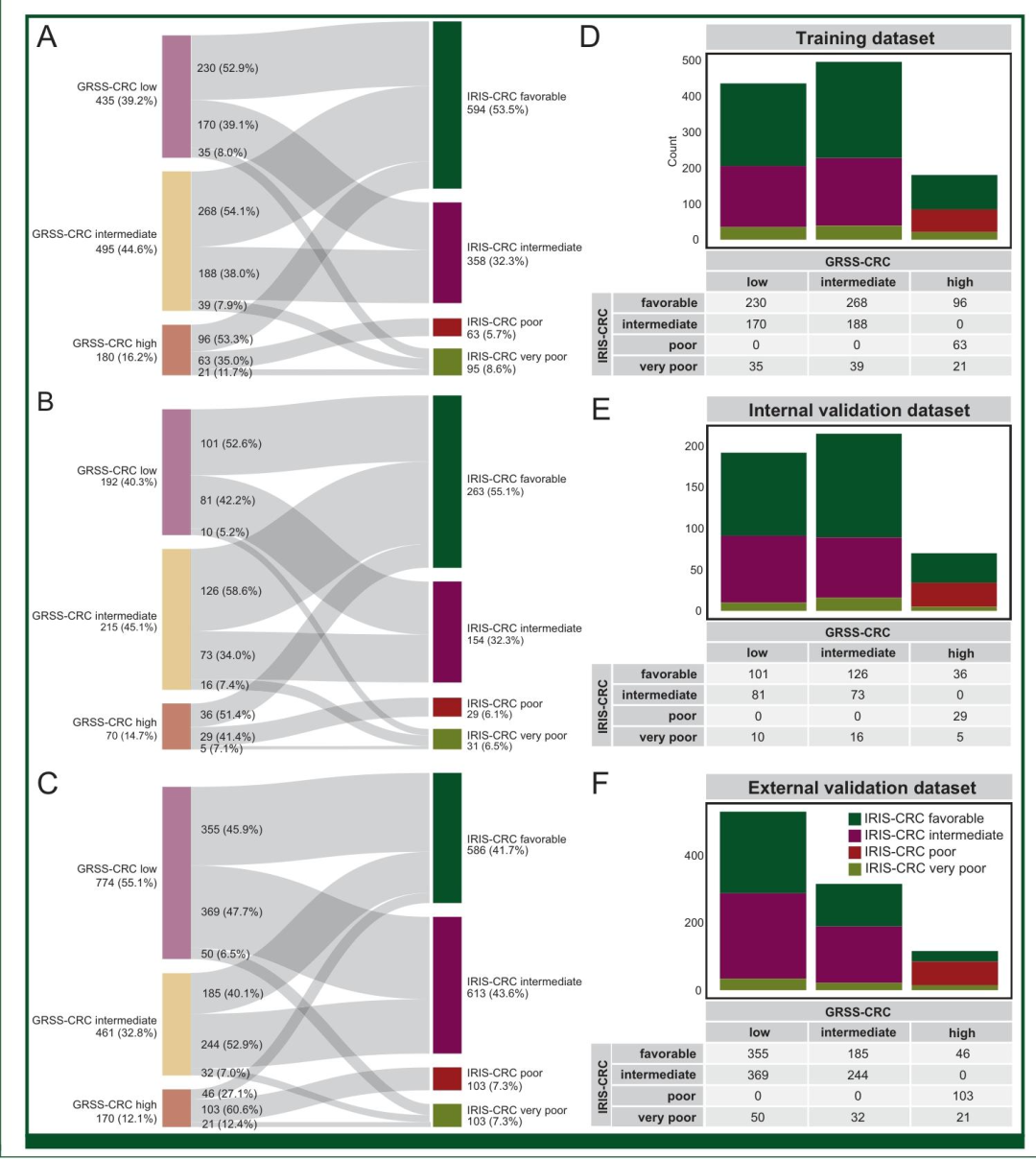
图 5:GRSS-CRC与IRIS-CRC的患者风险重分类对比图
05
研究结论
本研究提出并验证了一种新型的II期结直肠癌风险分层系统------IRIS-CRC ,该系统通过整合基于深度学习(Swin Transformer)的CT影像分析(STAR-CRC)与传统病理标志物(pT4、淋巴结采样数≤12、神经侵犯、脉管侵犯) ,实现了比传统指南依赖系统(GRSS-CRC)更精准、个体化的预后评估 。在包含2992例患者的多中心回顾性研究中,IRIS-CRC将患者分为四个具有显著差异3年无病生存率的预后组 (>95%、95%--75%、75%--55%、<55%),显著改善了风险区分能力 (C指数显著高于GRSS-CRC)。尤为关键的是,IRIS-CRC重分类了27.1%的传统高危患者为低危 (可能避免不必要的化疗),同时将6.5%的传统低危患者上调为极高危 (提示需强化治疗)。该系统在外部验证及不同治疗亚组中均保持稳定的分层性能,有望优化II期结直肠癌辅助化疗决策,推动治疗个体化。未来需前瞻性试验进一步验证其在指导治疗中的实际效益。
参考文献:Huang YQ, Chen XB, Cui YF, Yang F, Huang SX, Li ZH, Ying YJ, Li SY, Li MH, Gao P, Wu ZQ, Wen G, Wang ZS, Wang HX, Hong MP, Diao WJ, Chen XY, Hou KQ, Zhang R, Hou J, Fang Z, Wang ZN, Mao Y, Wee L, Liu ZY. Enhanced risk stratification for stage II colorectal cancer using deep learning-based CT classifier and pathological markers to optimize adjuvant therapy decision. Ann Oncol. 2025 Oct;36(10):1178-1189. doi: 10.1016/j.annonc.2025.05.537.