01
文献学习
今天分享的文献是由中国医学科学院肿瘤医院(国家癌症中心/国家肿瘤临床医学研究中心)团队于2025年2月在《ESMO Open》(中科院1区top,IF=8.3)上发表的研究"Integrating radiomics, pathomics, and biopsy-adapted immunoscore for predicting distant metastasis in locally advanced rectal cancer"即结合放射组学、病理组学和活检适应性免疫评分预测局部晚期直肠癌远处转移,该研究旨在构建并验证一个整合宏观放射学特征(放射组学)、微观病理学特征(病理组学)以及活检适应性免疫评分(ISB)的列线图模型,用于在接受新辅助放化疗的局部晚期直肠癌患者中预测远处转移风险。
创新点:①首次将宏观影像与微观病理信息整合预测 :创新性地融合影像组学、病理组学与活检免疫评分,构建多尺度预测模型,提升预测维度。②建立基于活检的免疫评分系统 :在治疗前通过活检样本评估肿瘤免疫浸润状态,为术前风险分层提供新依据,突破传统术后评估限制。③揭示多组学特征与免疫状态的内在关联:发现低免疫评分患者影像与病理特征风险更高,为肿瘤生物学行为提供跨尺度解释。
临床价值:①实现治疗前个体化风险分层 :模型可在新辅助治疗前识别高远处转移风险患者,为早期强化治疗提供决策支持。②辅助制定精准新辅助治疗策略 :帮助临床医生选择适合患者的治疗方案,如是否需加强全身治疗或调整放疗计划。③减少不必要治疗并改善预后:通过准确风险分层,避免低危患者过度治疗,同时加强高危患者管理,有望提升整体生存率。
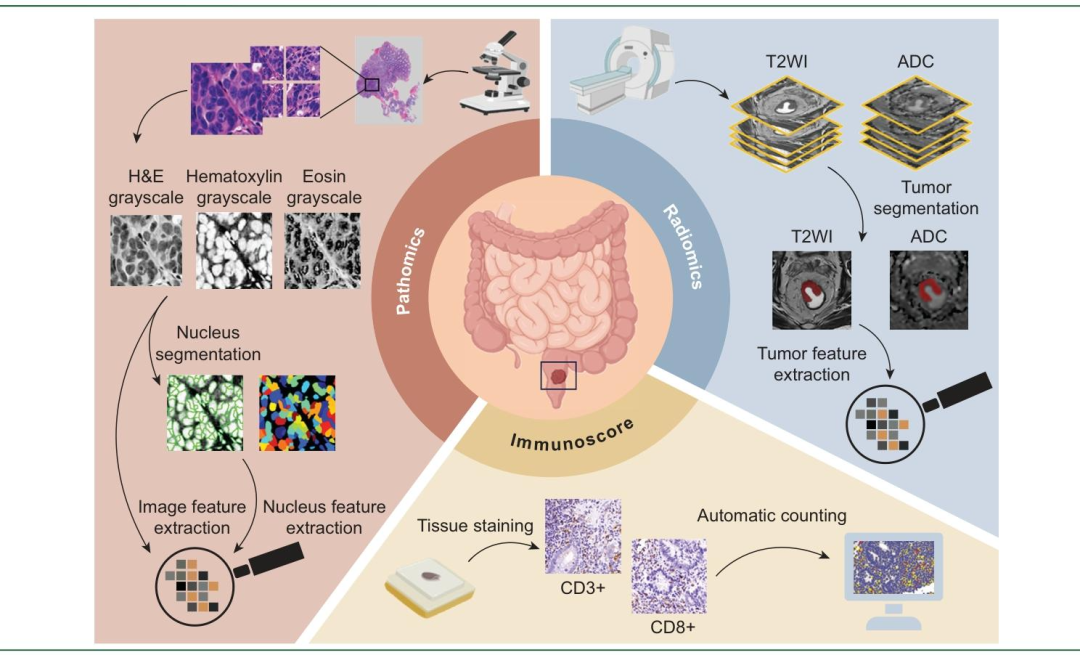
图 1:研究流程示意图
数据输入层:
影像数据:T2加权成像(T2WI)和表观扩散系数(ADC)图(均为灰度图格式);
病理数据:苏木精-伊红(H&E)染色活检标本的全切片图像(WSI,灰度图格式);
免疫组化数据:经组织染色后的CD3+、CD8+T细胞检测样本。
处理流程层:
影像处理:对T2WI和ADC图进行"肿瘤分割(Tumors egmentation)"→提取"肿瘤特征(Tumor feature extraction)",最终获得影像组学特征;
病理处理:对H&E染色WSI进行"细胞核分割(Nucleuss egmentation)"→分别提取"图像特征(Image feature extraction)"和"细胞核特征(Nucleus feature extraction)",最终获得病理组学特征(含全局模式和局部模式);
免疫评分处理:对CD3+、CD8+T细胞样本进行"自动计数(Automatic counting)",基于计数结果计算IS_B。
02
研究背景及目的
研究背景
局部晚期直肠癌(LARC)目前的标准治疗模式是新辅助放化疗(nCRT)联合全直肠系膜切除术。虽然该策略能显著降低局部复发率至5%--10%,但对远处转移(DM)的控制效果仍不理想 ,DM发生率仍高达25%--40%,并成为LARC患者死亡的主要原因。nCRT后手术的流程不可避免地延迟了全身性治疗的介入,而术后辅助化疗因患者依从性差、生存获益不明确,其在临床中的应用仍存在争议。因此,在治疗前精准识别高转移风险患者 ,从而制定前置性全身治疗策略 (如更早的系统治疗),对于控制潜在微转移、改善患者预后具有迫切临床意义。近年来,高通量组学技术如放射组学和病理组学的发展,为肿瘤异质性和微环境提供了量化分析手段。放射组学可从MRI图像(如T2加权像和ADC图)中提取大量肉眼难以辨别的影像特征;病理组学则可基于HE染色活检切片,通过计算分析获取肿瘤核形态与全局组织的微观表型信息。此外,肿瘤原位免疫浸润状态(特别是CD3+与CD8+ T细胞密度)已被证实与患者预后密切相关,而基于活检标本的免疫评分(ISB)可作为评估治疗反应和预后的可靠生物标志物。然而,目前尚缺乏将宏观放射学信息与微观病理学、免疫微环境信息相结合,用于LARC患者生存预测的研究,多尺度信息整合有望构建更强大的风险分层模型。
研究目的
本研究旨在开发并验证一个整合多尺度肿瘤特征的列线图(nomogram)模型 ,用于在治疗前准确预测接受新辅助放化疗的局部晚期直肠癌患者的远处转移风险。具体而言,研究系统性整合了三类基线特征 :放射组学特征 (从ADC图和T2WI中提取)、病理组学特征 (从HE染色活检全片图像中提取的全局与局部核形态特征)以及活检适应的免疫评分(ISB) (基于活检组织中CD3+和CD8+ T细胞密度计算)。通过LASSO-Cox回归分析进行特征筛选与签名构建,并利用单变量及多变量Cox回归确定独立预测因子,最终构建一个包含临床N分期、ISB、放射组学签名和病理组学签名的综合性预测模型。研究的核心目标是验证该整合模型在训练集和测试集中对1年、3年和5年无远处转移生存率的预测效能 ,并通过C-index、时间依赖ROC曲线下面积(AUC)及校准曲线等指标进行评估。此外,研究期望该模型能实现治疗前的有效风险分层,将患者区分为低危与高危群体,从而为个体化治疗决策(如强化新辅助治疗或密切随访)提供依据,最终改善LARC患者的临床管理策略与预后。
03
数据和方法
研究数据
①研究对象:2011年6月-2017年6月期间,中国医学科学院肿瘤医院收治的327例经确诊的LARC患者(T3-4和/或N1-2,M0),均在治疗前2周内接受直肠MRI检查。
②排除标准:黏液腺癌(28例)、有其他原发性恶性肿瘤病史(32例)、失访(31例)、MRI图像质量差(6例)、缺乏病理活检切片(29例)。
③最终样本量:201例患者,按7:3随机分为训练集(140例)和测试集(61例)。
④患者基线特征:
平均年龄54.5±10.6岁(23-79岁),男性142例(70.6%),女性59例(29.4%)。
所有患者均行R0根治性切除术,中位随访时间91个月(四分位距82-113个月)。
1年、3年、5年无远处转移生存率分别为85.6%、80.1%、75.6%。
训练集与测试集在年龄、性别、癌胚抗原(CEA)水平、CA19-9水平、肿瘤位置及临床T/N分期等基线特征上无统计学差异(P>0.05)。
技术方法
①影像组学特征提取:
图像来源:斜轴位T2加权成像(T2WI)和表观扩散系数(ADC)图。
感兴趣区(VOI)勾画:由2名经验丰富的放射科医生手动勾画肿瘤区域,通过组内相关系数(ICC>0.75)验证特征可重复性。
特征提取:基于pyradiomics模块,共提取2074个特征(T2WI和ADC图各1037个),经筛选后保留1328个稳定特征。
②病理组学特征提取:
图像来源:HE染色活检标本的全切片图像(WSIs)。
图像处理:选取10个无重叠的肿瘤细胞富集区域,使用CellProfiler软件提取621个特征(包括肿瘤整体图像特征和细胞核局部特征)。
③活检适应性免疫评分(IS_B)计算:
通过免疫组化检测活检标本中肿瘤区域CD3+和CD8+T细胞密度,采用HALO图像分析平台计数。
参考El Sissy等的方法,将CD3+和CD8+T细胞密度转换为百分位数,取平均值分为低(<25%)、中(25%-70%)、高(>70%-100%)三级。
④模型构建与验证:
特征筛选:通过单变量Cox分析(P<0.1)、相关性分析(|ρ|>0.8时剔除冗余特征)及LASSO-Cox分析(10折交叉验证)筛选关键特征,构建影像组学和病理组学签名。
列线图构建:整合影像组学签名、病理组学签名、IS_B及临床N分期(多变量Cox分析确定的独立预测因子)构建模型。
模型评估指标:一致性指数(C-index)、时间依赖性ROC曲线下面积(AUC)、校准曲线、决策曲线分析及Kaplan-Meier生存分析(log-rank检验)。
04
实验结果
①签名构建性能:
- 影像组学签名(7个关键特征):训练集C-index 0.811(95% CI 0.746-0.877),测试集0.752(95% CI 0.615-0.881)。
- 病理组学签名(7个关键特征):训练集C-index 0.713(95% CI 0.625-0.800),测试集0.702(95% CI 0.569-0.835)。
②IS_B的预后价值:
- 低IS_B患者的远处转移风险显著高于中、高IS_B患者(训练集:中vs低HR=0.224,P<0.001;高vs低HR=0.080,P<0.001;测试集结果一致)。
- 低、中、高IS_B患者的5年无远处转移生存率:训练集36.4%、79.0%、91.9%;测试集30.0%、86.8%、92.3%。
③列线图性能:
- C-index:训练集0.902(95% CI 0.870-0.933),测试集0.848(95% CI 0.743-0.951)。
- AUC:训练集1年0.930、3年0.947、5年0.950;测试集1年0.940、3年0.889、5年0.872。
- 校准曲线显示预测结果与实际结局一致性良好,决策曲线证实其临床净获益显著优于单一签名或IS_B。
④风险分层:
- 以风险评分0.188为临界值,将患者分为高、低危组。
- 训练集高风险组5年无远处转移生存率23.7%,低风险组95.1%(HR=25.168,P<0.001);测试集高风险组23.1%,低风险组89.6%(HR=11.772,P<0.001)。
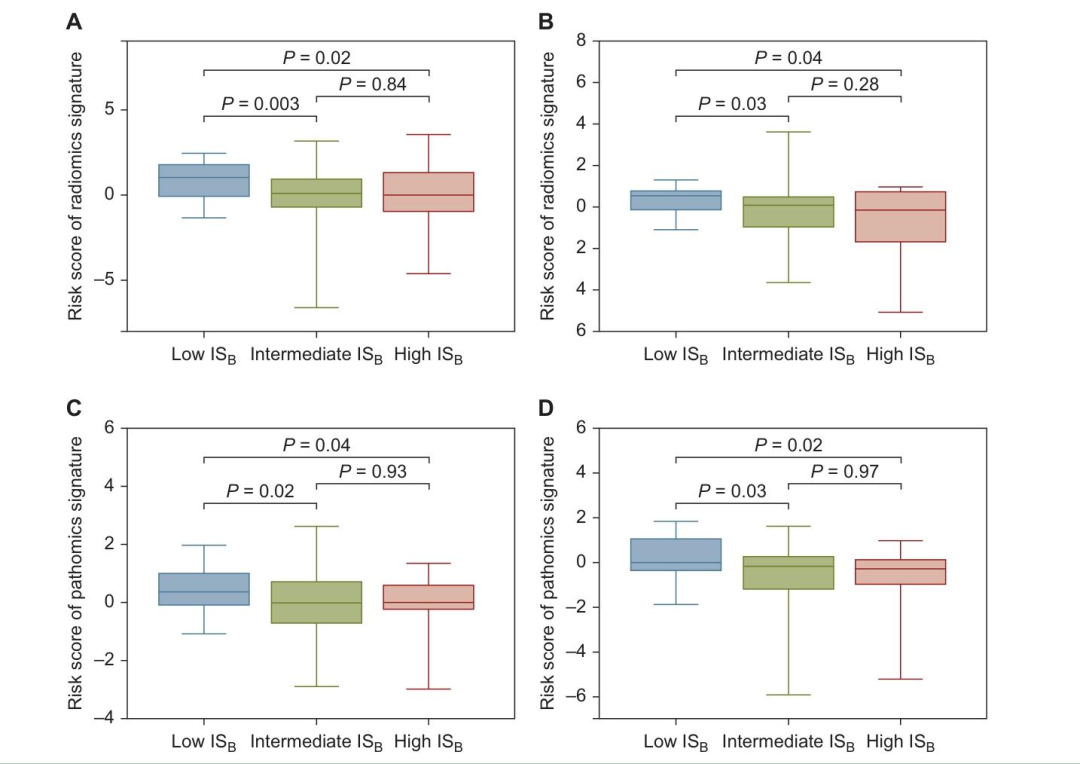
图 2:影像组学签名、病理组学签名与IS_B的相关性分析
探索不同IS_B分组(低、中、高)患者的影像组学、病理组学风险评分分布差异,验证免疫状态与肿瘤宏观/微观特征的内在关联。
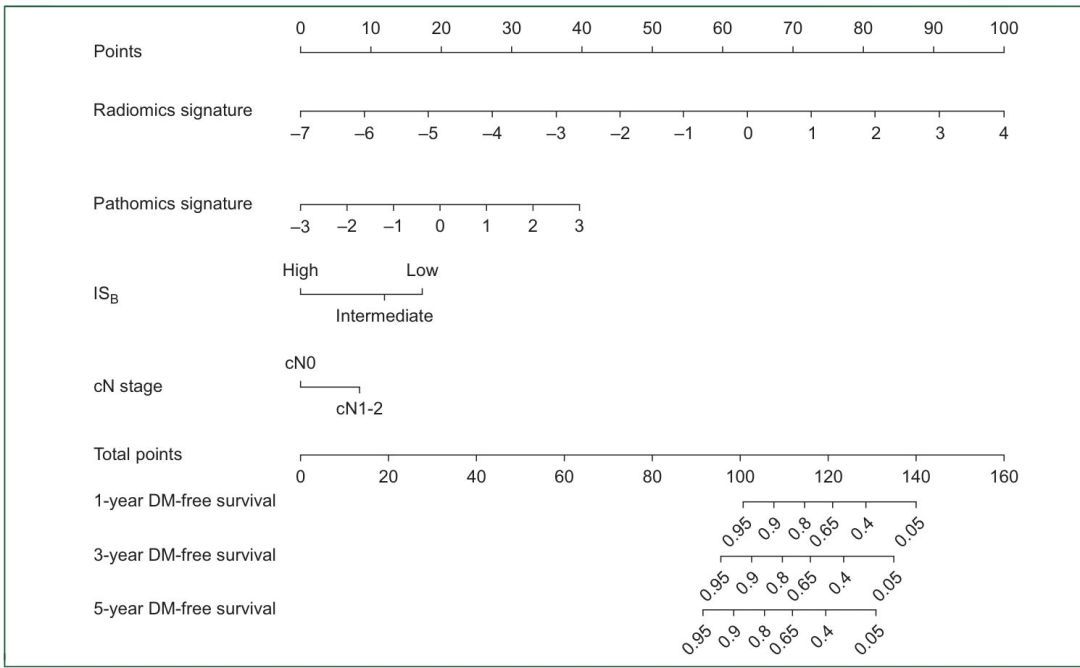
图 3:预测1、3、5年无远处转移生存的列线图
将多变量Cox分析筛选出的独立预测因子(临床N分期、IS_B、影像组学签名、病理组学签名)可视化,构建可直接用于临床的风险预测工具。
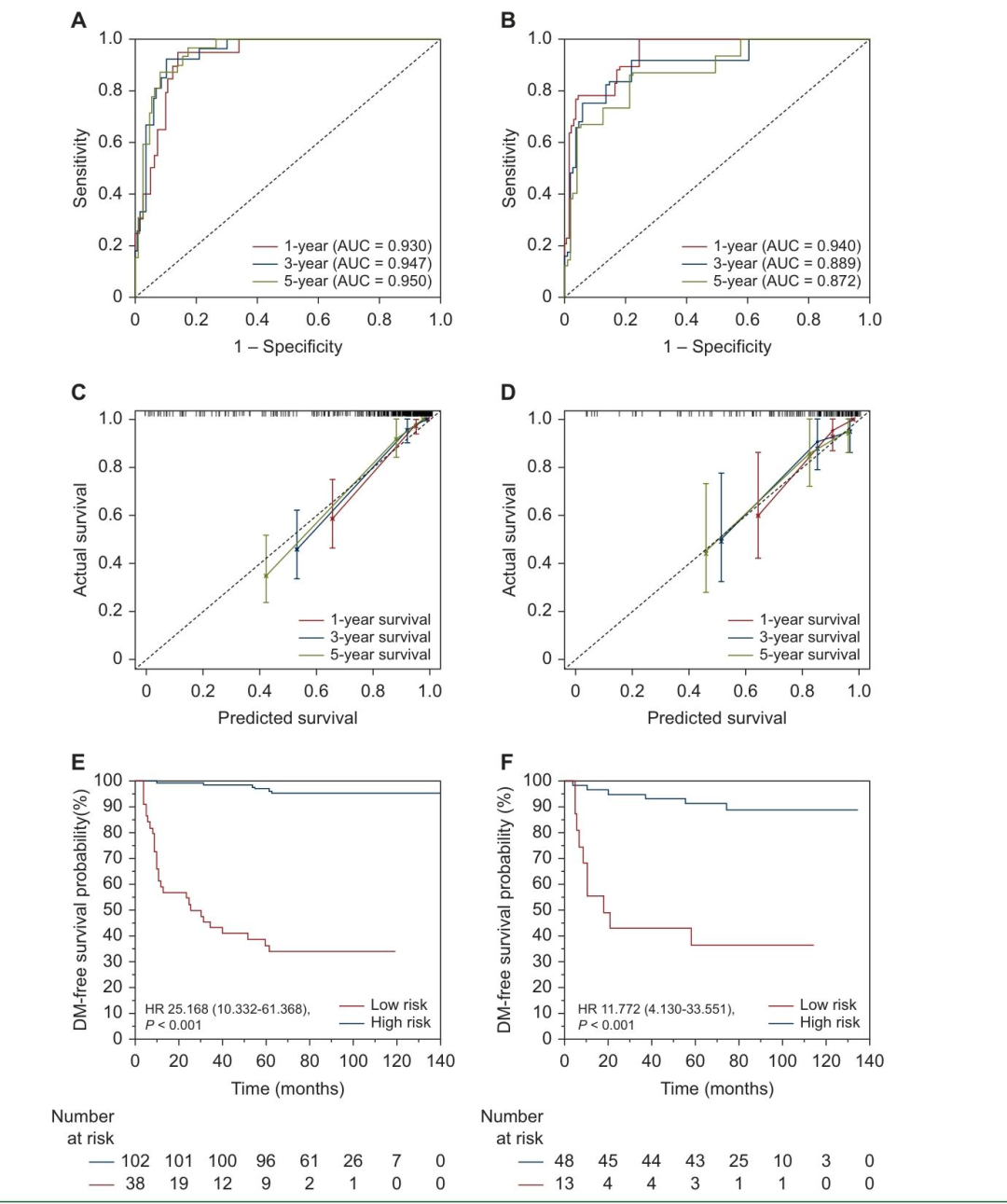
图 4:列线图的预测性能验证
从区分度、校准度、临床风险分层三个维度验证列线图的预测性能,确保模型的可靠性和临床适用性。
05
研究结论
该研究成功开发并验证了一种整合宏观放射组学与微观病理组学及活检免疫评分(ISB)的列线图(nomogram)模型,用于预测局部晚期直肠癌(LARC)患者在接受新辅助放化疗(nCRT)后的远处转移(DM)风险 。研究纳入201例患者,通过提取MRI影像的放射组学特征及活检HE切片的病理组学特征,并结合CD3+、CD8+ T细胞密度计算的ISB,构建多尺度预测模型。结果显示,低ISB患者具有显著更高的放射组学与病理组学风险评分 ,且ISB、临床N分期、放射组学与病理组学特征均为DM无生存期的独立预测因素 。该列线图在训练集与测试集中表现出优异的预测效能,C指数分别为0.902和0.848,5年DM无生存期的AUC分别达0.950和0.872 ,并能够有效将患者分为低危与高危组 ,高危组5年DM无生存率显著低于低危组(训练集:23.7% vs. 95.1%)。研究表明,整合多尺度肿瘤特征的列线图可在治疗前实现精准风险分层,有助于识别高危患者并指导个体化治疗决策,为LARC的预后评估与治疗优化提供了有力工具。
参考文献:Zhao R, Shen W, Zhao W, Peng W, Wan L, Chen S, Liu X, Wang S, Zou S, Zhang R, Zhang H. Integrating radiomics, pathomics, and biopsy-adapted immunoscore for predicting distant metastasis in locally advanced rectal cancer. ESMO Open. 2025 Mar;10(3):104102. doi: 10.1016/j.esmoop.2024.104102.