01
导语
各位同学,大家好。现在做影像组学,如果还只停留在"提取特征---建个模型---算个AUC ",那就有点像算命算得挺准,但为啥准,自己也说不明白。别人一问:你这特征到底代表啥?背后有啥道理?瞬间就成了黑箱本箱 。而真正能打高分、站得住脚的研究,都在干一件事------给影像组学找"生物学娘家" ,让宏观图像和微观病理、细胞、基因、通路对上话。今天咱们就通过一篇最新文献,看看人家是怎么把CT影像特征与肿瘤免疫微环境中的IL6/JAK/STAT3通路、干扰素应答、T细胞浸润 直接挂钩,不仅预测胃癌术后复发,还能解释为什么低风险组免疫激活、高风险组免疫抑制 。用轻松又实在的方式,聊聊影像组学怎么优雅、合理、不硬凑地挂靠生物学机制 ,从"只会算分的工具人 ",升级成"能讲清疾病故事的研究者"。

**★题目:**Radiomics-based ensemble model predicts postoperative recurrence of gastric cancer
(基于放射组学的集成模型预测胃癌术后复发)
★期刊:《BMC Medicine》(中科院1区,IF=8.3)
**★研究疾病:**胃癌
**★生物学机制:**肿瘤免疫微环境的异质性
**★发表时间:**2025年11月
02
研究背景-从 "临床问题" 落到 "生物学问题"
局部进展期胃癌(LAGC)术后早期复发是影响患者长期生存的关键瓶颈,尽管根治性手术联合辅助化疗 已成为标准治疗模式,但仍有超过半数患者在术后两年内出现复发,预后极差。当前临床广泛依赖的TNM分期系统 虽能提供基础预后信息,却难以捕捉肿瘤内在的生物学异质性 ,尤其是肿瘤免疫微环境(TIME) 的差异,这被认为是导致不同患者复发风险差异的根本原因之一。然而,免疫微环境的评估通常依赖于术后组织样本,具有侵入性且无法在术前或动态监测中应用。近年来,影像组学 作为一种高通量医学图像分析方法,能够从常规CT图像中提取数百个定量特征,反映肿瘤的异质性、形态、纹理和强度 等信息,理论上可作为一种非侵入性的"虚拟活检" 手段。尽管已有研究尝试构建基于影像组学的胃癌复发预测模型,但普遍存在特征选择不一致、缺乏多中心外部验证、模型可解释性差 等关键问题,尤其缺乏与生物学机制 的关联验证,导致其临床转化受限。因此,如何将影像组学从"统计预测工具"提升为"具有生物学内涵的临床决策支持系统 ",是当前该领域亟待解决的核心科学问题。本研究正是立足于这一背景,试图通过大规模多中心数据、严谨的建模流程和深入的转录组机制分析,填补影像组学预测模型与肿瘤免疫生物学之间的鸿沟。
03
研究目的(明确写出"三层目的")
本研究围绕"能否通过影像组学非侵入性地评估胃癌术后复发风险及其背后的免疫微环境机制 "这一核心问题,设定了三个层层递进的研究目的。第一层(临床层) :构建一个能够准确预测LAGC患者术后早期复发 的集成预测模型,该模型需整合临床参数与影像组学特征,并在多中心、前瞻性及公共数据集中验证其泛化能力 。第二层(技术层) :开发一个名为RSA(Radiomics-Clinical Integrated Risk Stratification Assessment) 的多模态诺模图模型,使其在预测性能上显著优于单纯的临床模型或影像组学模型,并通过净重分类改善指数(NRI)、综合判别改善指数(IDI)、决策曲线分析 等指标量化其增量价值。第三层(机制层) :这是本研究的核心创新所在 ------通过配对肿瘤组织的转录组测序(RNA-seq) ,结合CIBERSORTx、EcoTyper、ssGSEA 等免疫分析工具,揭示RSA模型所定义的高/低风险组之间在免疫通路激活、免疫细胞浸润、免疫检查点分子表达等方面的显著差异 ,从而为影像组学特征赋予生物学解释性 。最终目标是证明:RSA模型不仅仅是统计意义上的预测工具,更是肿瘤免疫微环境状态的非侵入性反映,为个性化术后管理提供机制驱动的决策支持。
04
研究思路(最核心:怎么挂靠机制)
本研究的整体思路遵循"从影像表型到分子机制 "的递进逻辑,核心在于用转录组数据"挂靠"影像组学风险评分的生物学内涵 。具体而言,首先构建一个大规模、多中心的回顾性队列 (2,516例,来自中国南北六家医院),采用nnU-Net深度学习模型 自动分割门静脉期CT图像中的胃癌原发灶,提取1,130个影像组学特征。通过mRMR + LASSO 分层筛选框架,最终保留8个最具预测价值的影像组学特征 。接着,整合病理类型、pT分期、pN分期 等独立临床预测因子,构建RSA多模态诺模图模型 ,并在内部、外部、前瞻性(NCT01516944)及公共TCIA数据集 中反复验证其预测性能。最关键的一步是机制挂靠 :对114例患者的新鲜肿瘤组织进行RNA-seq ,将RSA模型计算出的风险评分分为高风险组与低风险组 ,然后系统比较两组的转录组差异 。通过GSEA、GSVA 识别富集的信号通路(如IL6/JAK/STAT3、干扰素应答),通过CIBERSORTx 和EcoTyper 量化免疫细胞组成与多细胞群落结构 ,并在TCGA-STAD公共数据 中复现上述免疫差异。此外,利用SHAP分析 解释单个影像组学特征对风险评分的贡献方向,进一步桥接影像特征与生物学行为。这一思路确保了预测性能与机制解释的双重可信度,使影像组学模型不再是"黑箱",而是可被生物学验证的临床决策工具。
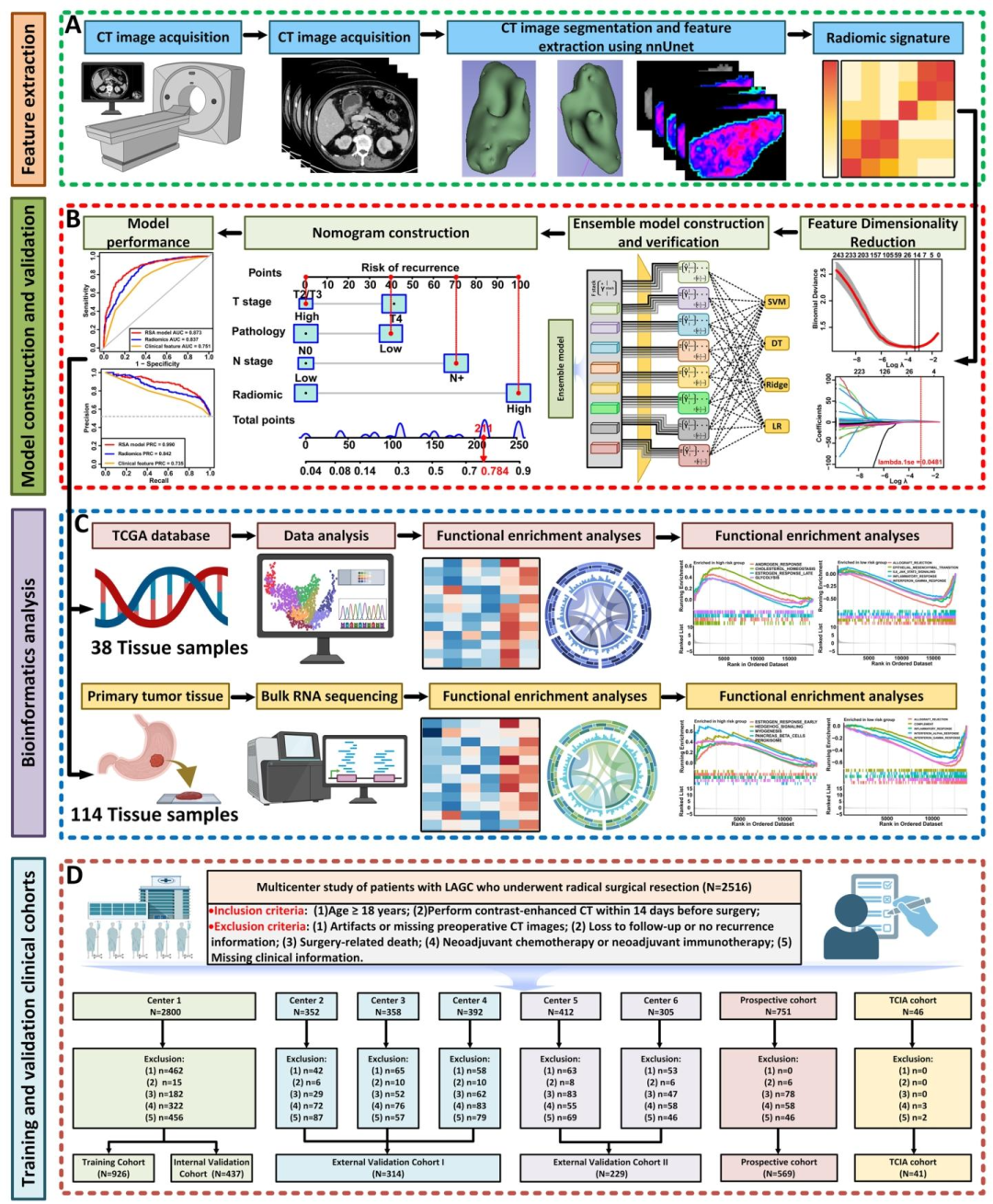
图 1:研究整体工作流程图
05
数据和方法(机制部分怎么设计)
数据: 本研究共纳入 2,516 例 局部进展期胃癌(LAGC)患者,来自中国南北六家医院:其中 926 例 (河北医科大学第四医院,2014‑2017)作为训练集 ;437例 (同一医院,2012‑2013及2018‑2019)作为内部验证集 ;543例 (其余五家医院)作为外部验证集 (北方314例、南方229例)。此外,纳入569例 来自前瞻性多中心临床试验(NCT01516944)的患者作为前瞻验证集 ,41例 来自公共数据库TCIA作为独立测试集 ,并对其中114例 患者的新鲜肿瘤组织进行**转录组测序(RNA‑seq)**用于机制分析。
**方法:**CT图像获取 → nnU‑Net自动分割原发灶 → 提取1,130个影像组学特征 → ComBat去除中心效应 → mRMR筛选400个候选特征 → LASSO回归筛选出8个关键特征 → 整合临床独立预测因子(病理类型、pT、pN) → 构建RSA多模态诺模图模型 → 内部/外部/前瞻/TCIA验证 → 计算风险评分并依Youden指数分为高/低风险组 → 对114例配对肿瘤组织行RNA‑seq → GSEA/GSVA通路富集分析 → CIBERSORTx/EcoTyper评估免疫细胞浸润 → SHAP解释特征贡献 → TCGA‑STAD数据复现免疫差异。
06
研究结果("从表型到机制")
1. 表型层面:模型预测性能强
RSA模型在训练集AUC达0.873,内部验证集0.871‑0.872,外部验证集0.870‑0.873,前瞻集0.857,TCIA集0.850,显著优于临床或影像组学单模态模型,且校准良好、净获益最高。
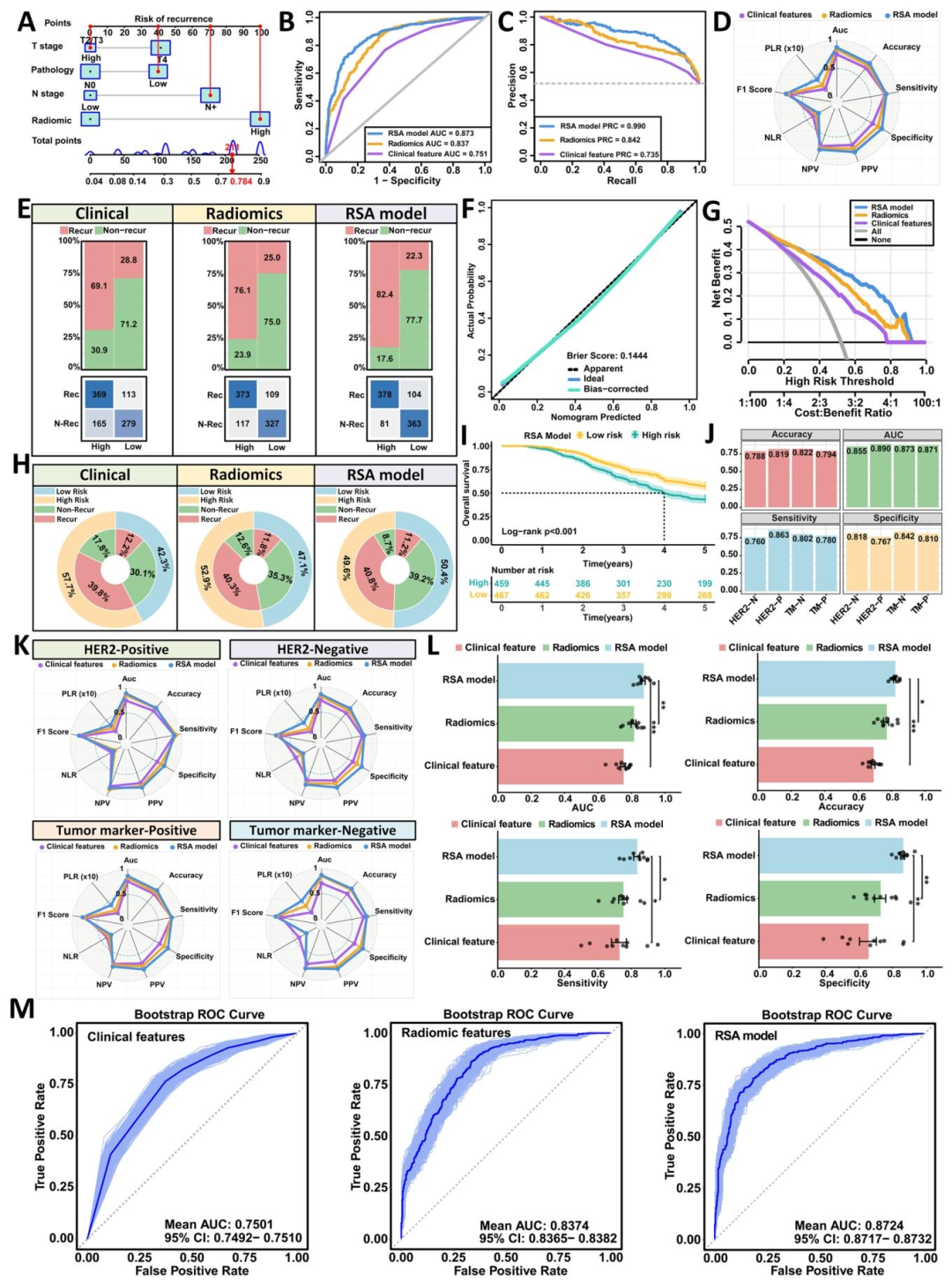
图 2(RSA模型整体性能与诺模图): 该图展示了RSA模型的诺模图 (整合病理类型、pT、pN及8个影像组学特征),其训练集AUC达0.873 ,校准曲线(Brier评分0.144)和决策曲线均优于单模态模型。同心圆图显示高风险组识别出更多复发患者,Kaplan‑Meier曲线证实高风险组5年OS显著更差。该图首次将影像组学风险评分与临床结局直接关联,为后续机制分析提供表型基础,证明影像特征具有预后价值。
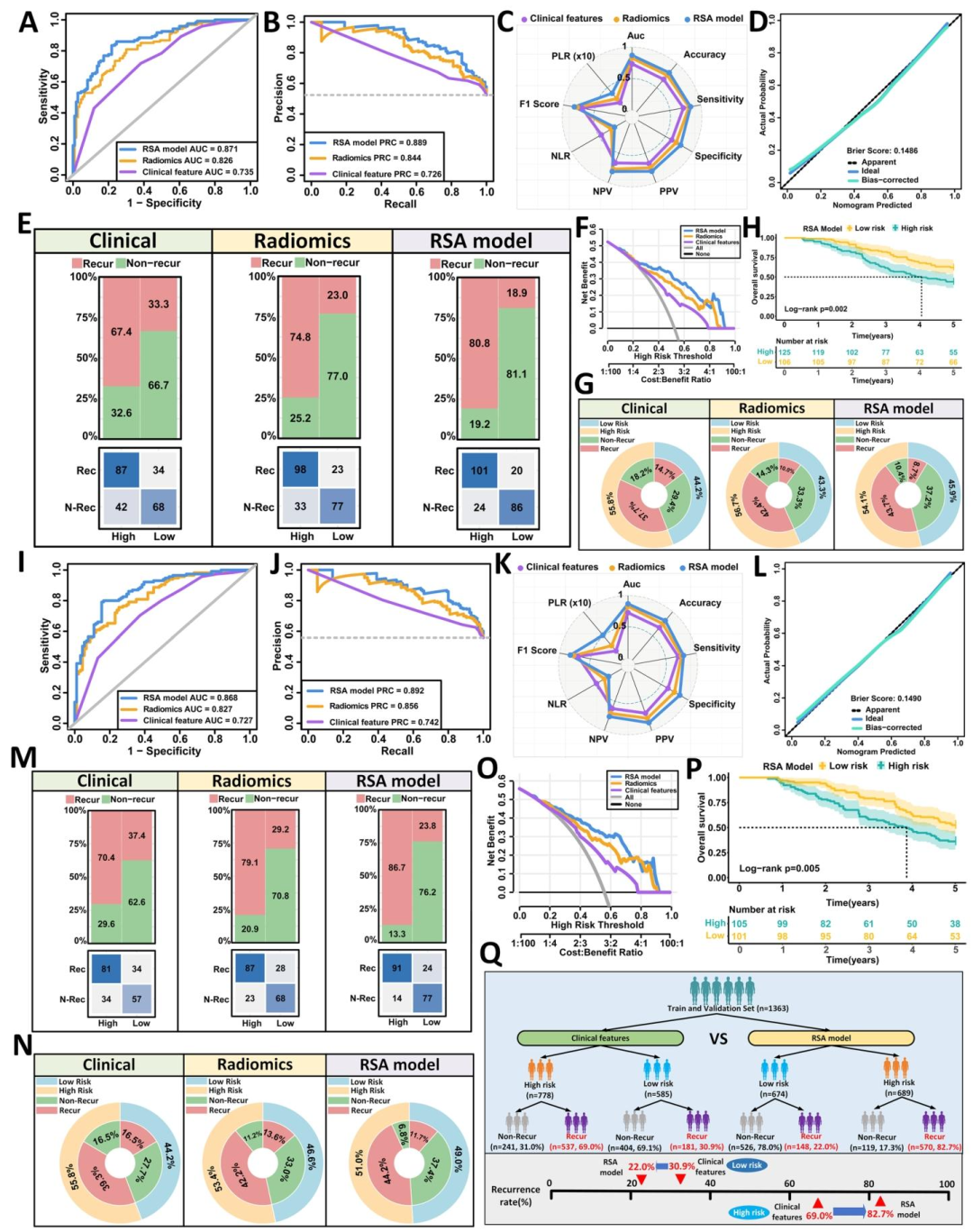
图 3(内部验证集性能与生存):图3 在内部验证集(两个时间亚组)中复现了RSA模型的优越性能:AUC约0.871,NRI和IDI显著提升,校准良好。同心圆图显示RSA较临床模型多识别出6%的高危复发患者 ,且高风险组5年OS降低约18%。Kaplan‑Meier曲线和Cox回归证实RSA为独立预后因子。该图强化了影像组学特征的稳定性和泛化能力,为后续将风险评分用于免疫分组提供了可靠的临床依据。
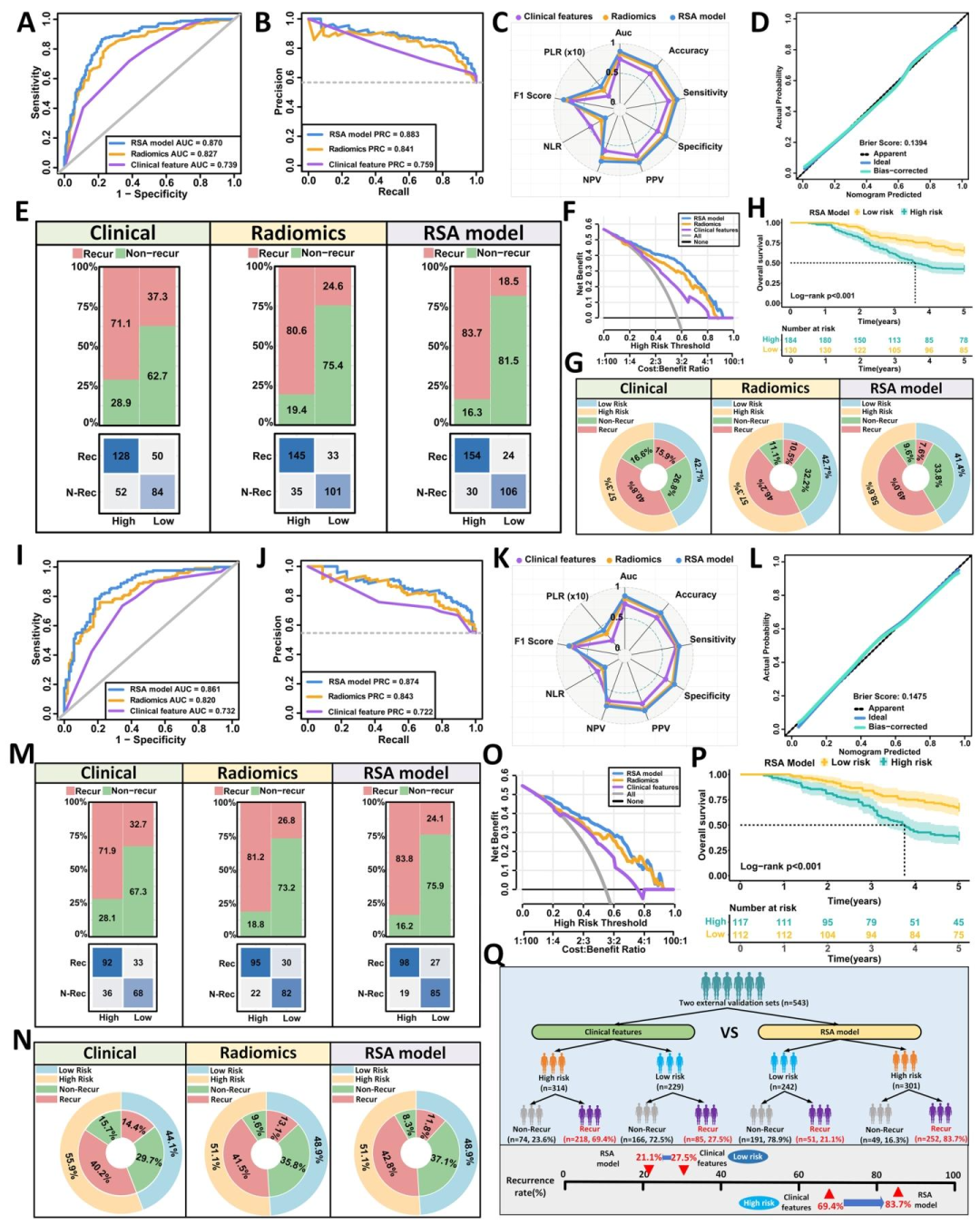
图 4(外部验证集性能):图4 在南北两个独立外部队列(共543例)中验证了RSA模型的泛化性:AUC分别达0.870和0.873,决策曲线净获益最高。同心圆图显示RSA较临床模型将高危识别率提高14.3% ,低危误判率降低6.4%。生存分析表明高风险组5年OS降低约23%‑28%。该图证明影像组学特征不受地域和扫描协议差异影响,为后续将RSA评分用于跨中心免疫机制验证提供了可信的输入标签。
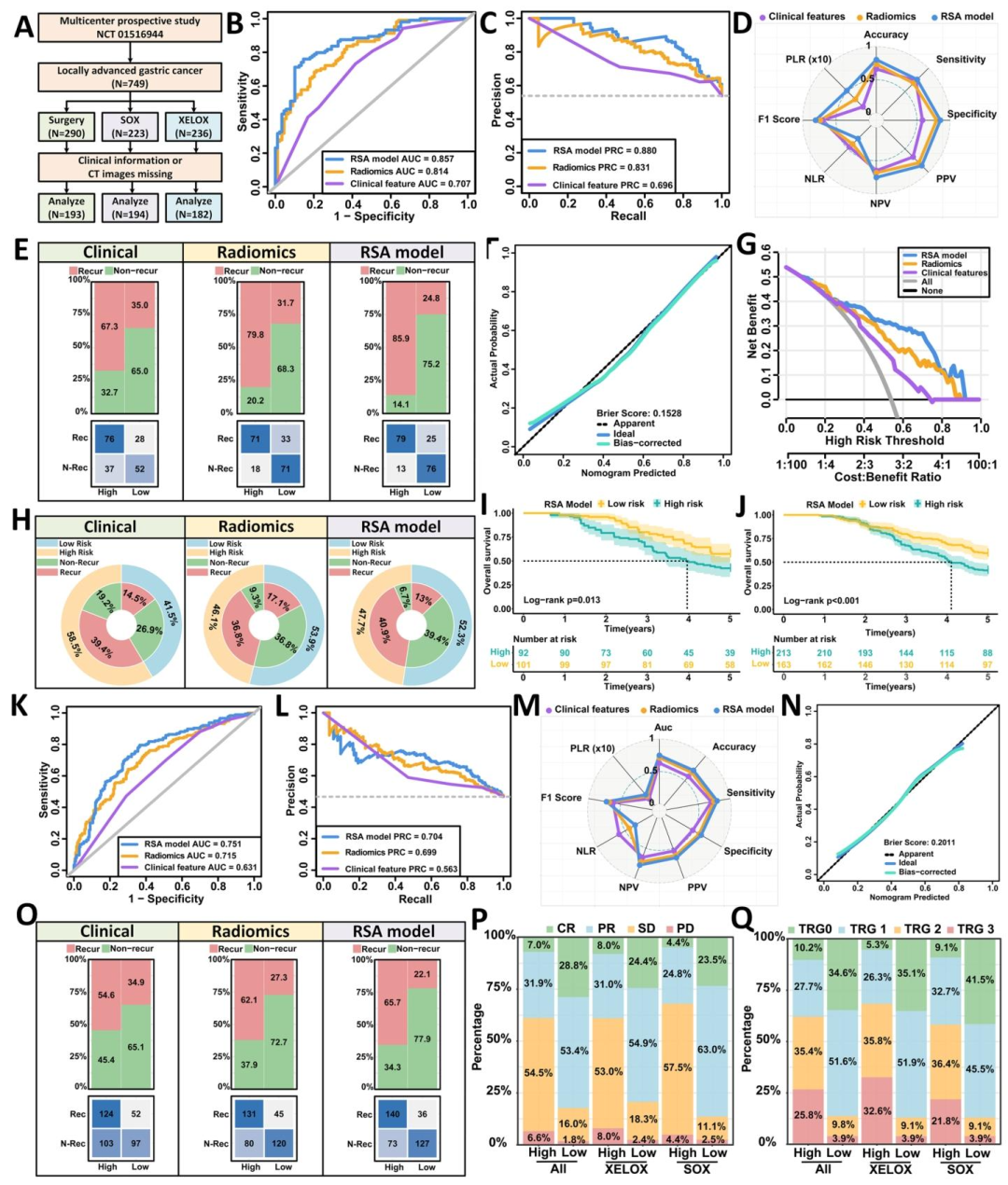
图 5(前瞻性队列与NAC亚组):图5 在前瞻性临床试验(NCT01516944,569例)中评估RSA模型。手术直接组AUC达0.857,而新辅助化疗(NAC)组AUC降至0.751 ,且与治疗反应无明确关联。尽管NAC组预测效能下降,但高风险组5年OS仍显著更差。该图揭示了化疗对影像组学特征的干扰,提示肿瘤坏死、纤维化等治疗诱导的改变可能掩盖原始免疫表型,为后续机制讨论中"动态模型"需求提供了直接证据。
2. 分层能力:优于TNM分期
在相同TNM分期(I‑III期)内,RSA模型仍能显著区分高/低风险患者的五年总生存期(P均<0.05)。倾向评分匹配后生存差异依然存在,证明其分层能力超越传统分期。
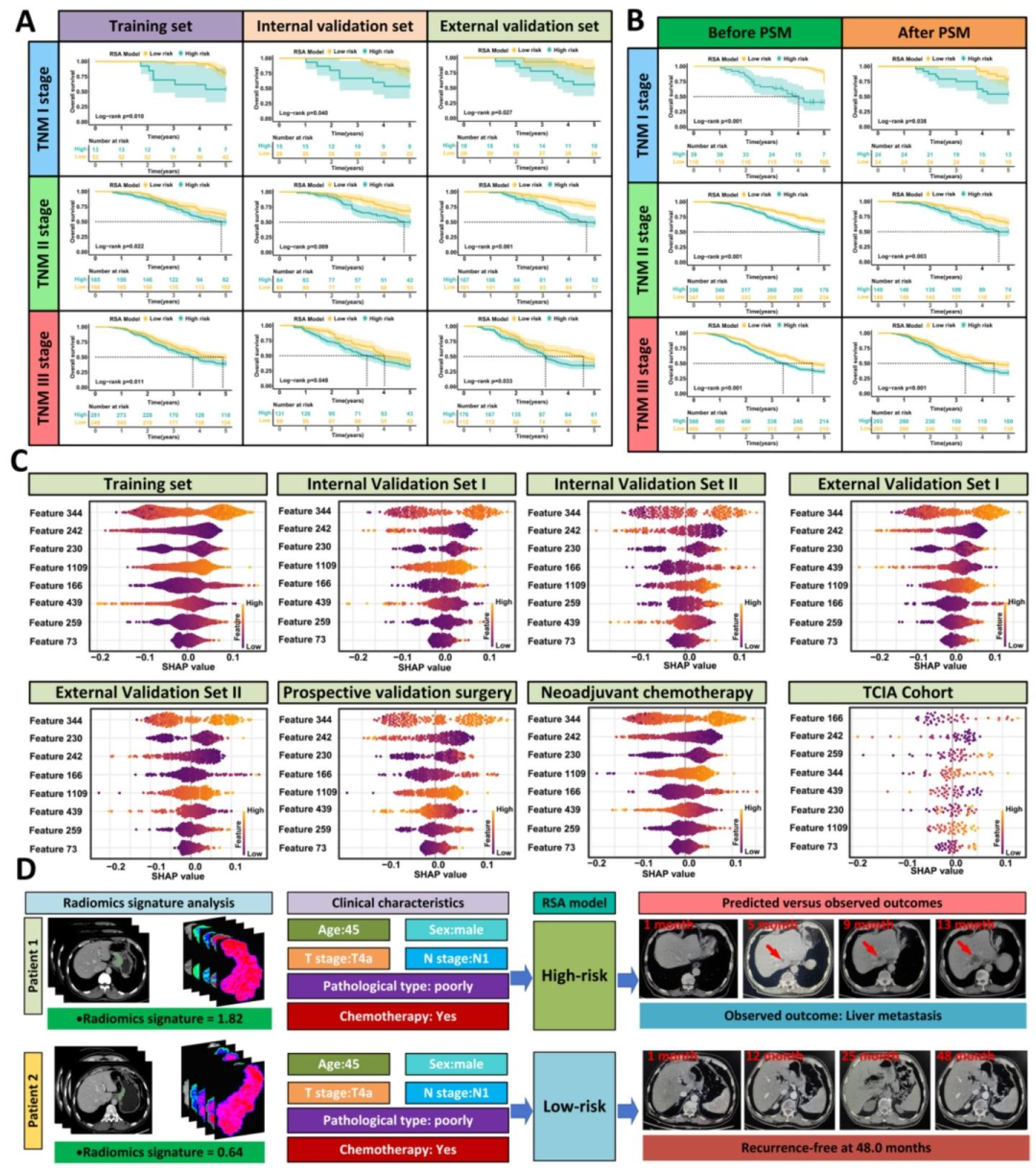
图 6(TNM分层、SHAP与患者轨迹): 该图展示了RSA模型超越传统TNM分期的能力:在I‑III期内部,RSA高风险组OS均显著低于低风险组(log‑rank P<0.05),PSM匹配后差异依然存在 。SHAP摘要图显示影像组学特征(如形状、纹理)与临床参数共同驱动风险评分,并给出两个患者的临床轨迹对比。该图将影像特征贡献度可视化,桥接了影像表型与个体预后,为后续免疫机制分析提供了可解释的中间变量。
3. 机制层面:低风险组免疫激活
低风险组显著富集IL6/JAK/STAT3、干扰素应答等免疫通路,CIBERSORTx显示T细胞等免疫细胞浸润更高,免疫检查点分子表达上调,提示免疫微环境处于活化状态。
4. 高风险组:免疫抑制
高风险组免疫相关通路下调,免疫细胞浸润减少,呈现免疫抑制表型。转录组与免疫评分均证实其微环境不利于抗肿瘤免疫,与不良预后及高复发风险一致。
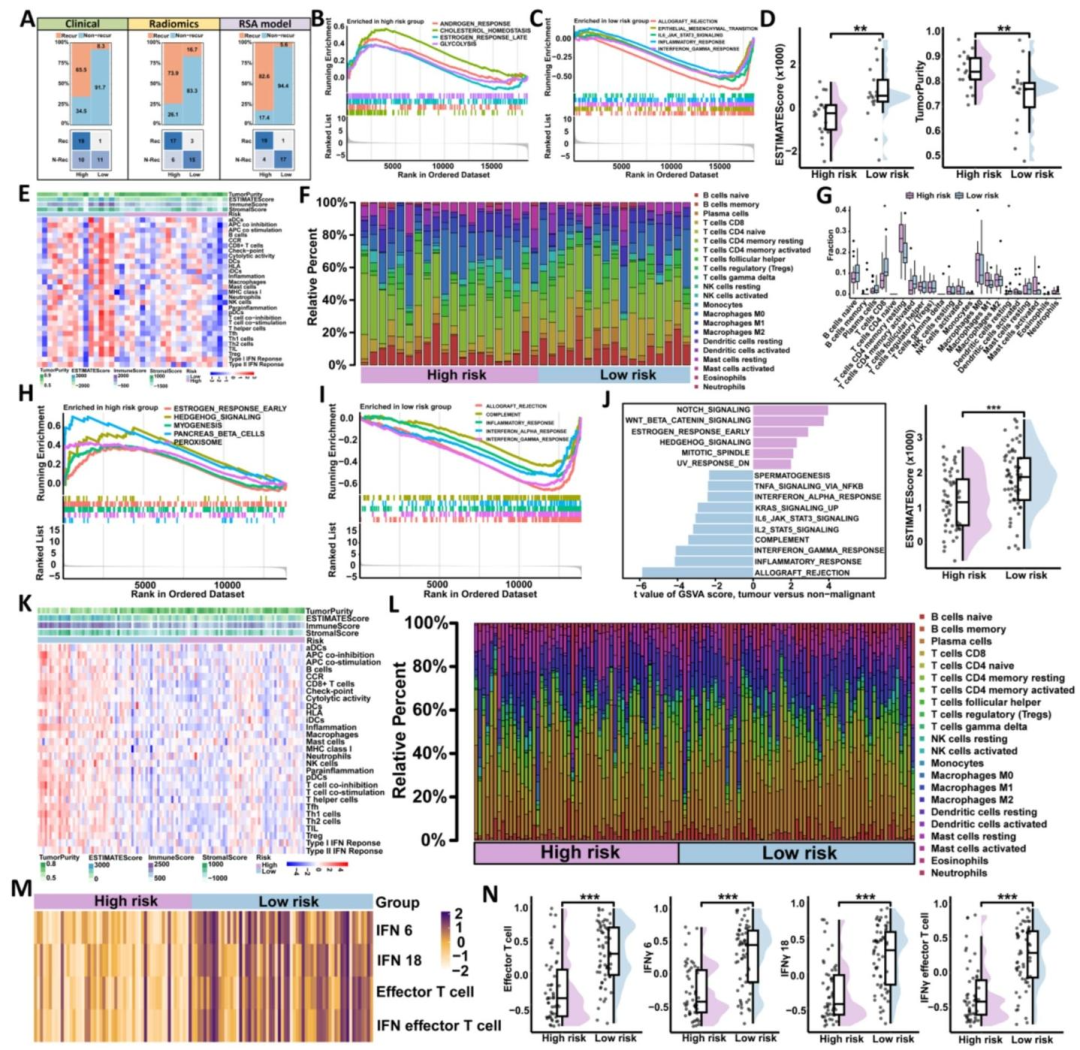
图 7(机制:免疫通路与细胞浸润): 该图是影像组学挂靠生物学机制的核心图 。通过转录组分析显示:低风险组显著富集IL6/JAK/STAT3、干扰素α/γ应答通路 ,CIBERSORTx证实其T细胞、细胞毒性淋巴细胞浸润更高,免疫检查点分子表达上调。高风险组则呈现免疫抑制表型。该图直接证明RSA风险评分反映肿瘤免疫微环境状态,即影像组学特征可作为"非侵入性免疫成像"标志物,从而赋予预测模型生物学内涵。
07
讨论(把机制故事讲圆)
本研究通过大规模多中心数据验证,成功构建了整合影像组学与临床参数的RSA模型,其在预测LAGC术后早期复发方面表现出稳定且优越的性能 (AUC 0.85‑0.87),显著优于传统临床模型或单一影像组学模型。更重要的是,本研究突破了既往影像组学研究的"黑箱"局限 ,通过配对肿瘤组织的转录组测序,将影像组学风险评分与肿瘤免疫微环境状态直接挂钩 :低风险组呈现IL6/JAK/STAT3、干扰素信号通路激活 及高免疫细胞浸润 ,而高风险组则表现为免疫抑制表型 。这一发现不仅解释了模型为何能预测复发,更从生物学层面验证了影像组学特征的非侵入性"免疫成像"价值 。研究还发现,RSA模型在新辅助化疗亚组中预测效能下降(AUC降至0.751) ,提示化疗引起的肿瘤坏死、纤维化等改变可能破坏原始影像特征的稳定性 ,这为后续研究指明了方向------需要开发动态影像组学模型 或针对NAC人群的专用重训练策略 。尽管存在回顾性设计、影像协议差异等局限,但研究通过ComBat校正、多中心验证、前瞻队列及公共数据复现 等措施最大程度控制了偏倚。总体而言,本研究不仅提供了一个可直接用于临床决策的预测工具 ,更重要的是建立了影像组学与肿瘤免疫生物学之间的桥梁 ,为精准医学时代的非侵入性免疫表型评估提供了范式。
08
这篇文献的可借鉴思路
这篇文献为从事影像组学或医学人工智能研究的学者提供了多条可直接迁移的思路 。第一,"预测 + 机制"双驱动设计 :不要满足于构建一个高AUC模型,应尽可能收集配对的组织样本或公共转录组数据 ,用CIBERSORTx、ssGSEA、GSVA 等工具将风险评分与免疫微环境特征 关联,这能极大提升论文的深度和审稿人的认可度。第二,多源验证策略 :除了常规的内部和外部验证,积极利用前瞻性临床试验数据 和TCIA/TCGA公共数据 进行独立验证,不仅能证明泛化能力,还能借助公共数据的多组学信息 强化机制结论。第三,亚组分析揭示局限性 :不要回避模型在特定亚组(如新辅助化疗患者)中表现下降的事实,反而可以将其作为**"讨论"部分的亮点** ,提出动态模型、域适应、迁移学习 等改进方向,体现科研严谨性。第四,特征筛选流程可复现 :mRMR + LASSO + 相关性过滤 的分层筛选框架适用于大多数高通量特征降维场景,可直接用于其他癌种或其它模态(如病理组学、基因组学)。第五,SHAP增强可解释性 :用SHAP图展示每个影像特征对风险评分的贡献方向和幅度,使模型从"黑箱"变为"可解释的临床决策辅助工具 "。第六,伦理与数据共享意识 :论文公开了代码和特征筛选逻辑,这种做法在影像组学领域仍属少数,但可显著提升论文的引用潜力与学术影响力 。以上思路不限于胃癌,可直接迁移至肺癌、结直肠癌、肝癌等实体瘤的影像组学或多模态研究。
09
结语
总而言之,做影像组学不只是拼AUC、堆模型,更要学会给特征找意义、给模型讲道理 。这篇文献告诉我们:用配对转录组数据验证风险分组的免疫差异,用CIBERSORTx量化细胞浸润,用GSEA锁定关键通路 ,就能让影像组学从"黑箱预测 "变成"非侵入性免疫成像 "。只有把宏观影像和微观机制真正打通,我们的研究才不是"玄学算命 ",而是有根有据、有血有肉、能讲好疾病故事的真科研 。希望大家以后都能少走弯路,轻松写出有机制、有深度、能发高分的好文章!
参考文献:Ding P, Chen S, Guo H, Yang J, Fu Q, Wang B, Gu R, Zhang L, Wu J, Wu H, Meng N, Li X, Guo Z, Tian Y, Meng L, Zhao Q. Radiomics-based ensemble model predicts postoperative recurrence of gastric cancer. BMC Med. 2025 Nov 25;23(1):656. doi: 10.1186/s12916-025-04393-4.