A haplotype-resolved chromosome-level genome assembly of autotetraploid Chinese yam ( Dioscorea polystachya ) elucidates dioscin biosynthesis and regulation
同源四倍体山药( Dioscorea polystachya )染色体水平单倍型解析基因组揭示薯蓣皂苷的生物合成与调控机制

大麻(Cannabis sativa)单倍型基因组--文献精读222-CSDN博客
山药(Dioscorea polystachya )是广泛栽培的药食同源作物,兼具营养价值与药用价值。然而,高质量参考基因组的匮乏,严重制约了山药分子遗传解析与品种改良育种工作。本研究针对该同源四倍体 物种,组装获得单倍型分辨的染色体水平参考基因组 ;基因组大小 1.56 Gb,完整锚定至 4 套单倍型共 80 条染色体,共注释得到 95 668 个蛋白编码基因。
山药与大薯(Dioscorea alata )约在 464 万年前发生物种分化;随后在约 142 万年前经历一次物种特异性全基因组复制事件,最终形成无亚基因组优势的同源四倍体。薯蓣皂苷是山药块茎中主要积累的重要甾体皂苷,相较于二倍体近缘物种大薯,山药中薯蓣皂苷合成通路相关基因发生显著保留扩张。
结合转录组与基因功能验证发现:7 - 脱氢胆固醇还原酶基因( Dp7-DR ) 可正向促进薯蓣皂苷积累,该基因呈块茎特异表达,且受脱落酸显著诱导。酵母单杂交、双荧光素酶报告实验与凝胶迁移实验证实,转录因子DpbZIP12 可直接结合并激活 Dp7-DR 的转录。基因过表达结果表明,Dp7-DR 或 DpbZIP12 过表达可降低胆固醇含量、提升薯蓣皂苷积累;沉默上述基因则呈现完全相反的代谢特征。
本研究明确了调控薯蓣皂苷合成的关键靶点基因,为山药皂苷含量定向改良提供优异基因资源,同时也为提升山药营养与药用品质奠定理论基础。
引言
中国是山药属(Dioscorea )古老的起源与驯化核心区,种质资源丰富,现存山药物种共计 55 种。其中,山药( Dioscorea polystachya ) 分布最广、栽培规模最大,富含优质淀粉与多种功能性活性成分,千百年来既是优质药食同源蔬菜,也是传统中药材。薯蓣皂苷是山药关键特征性皂苷,可作为工业前体物质,用于合成可的松、孕烯醇酮、孕酮等甾体激素;同时兼具抗炎、降糖、抗肿瘤等药理活性。
植物体内薯蓣皂苷的合成起始于两种关键前体:甲羟戊酸途径生成的异戊烯焦磷酸,以及甲基赤藓醇 - 4 - 磷酸途径合成的二甲基丙烯焦磷酸。两类中间产物进一步转化为牻牛儿焦磷酸与法尼基焦磷酸,依次生成鲨烯、2,3 - 氧化鲨烯,最终合成胆固醇。胆固醇是植物甾体皂苷与甾体生物碱的共同合成前体,再经由细胞色素 P450 单加氧酶 (CYP90B、CYP94、CYP72A 等)与UDP - 糖基转移酶 修饰加工,完成薯蓣皂苷的合成。目前,本氏烟草与酵母体系已实现从胆固醇到薯蓣皂苷元的异源合成,但山药遗传转化体系效率低、操作困难,严重限制了皂苷合成关键基因的体内功能验证。此外,山药为雌雄异株 植物,长期以无性克隆繁殖为主,至今缺乏高质量参考基因组,极大阻碍了薯蓣皂苷生物合成关键酶基因的挖掘与调控机制解析。
近年来,研究者陆续发布了圆叶山药、大薯、盾叶薯蓣、穿龙薯蓣等二倍体山药物种的基因组,为解析薯蓣皂苷合成机制提供了重要基础。但山药属物种普遍存在倍性分化 现象:如白山药、大薯存在二倍体(2n=40)、三倍体(2n=60)、四倍体(2n=80)等核型;药用物种盾叶薯蓣也包含二倍体、三倍体、四倍体类群。然而,山药属多倍体起源演化机制、不同倍性物种间的进化关系,目前仍缺乏系统解析。
江西地方特色山药品种'瑞昌山药'栽培历史超 500 年,风味独特、品质优良,块茎碳水化合物积累量大,甾体皂苷含量丰富,具备极高的药用与开发价值。鉴于次生代谢产物的重要经济与药用价值,其合成通路及积累调控机制备受关注。本研究以同源四倍体瑞昌山药为材料,构建单倍型水平、染色体级别高质量参考基因组 ;结合比较基因组、转录组与基因功能验证,系统解析薯蓣皂苷的生物合成与分子调控网络,为深入阐明山药皂苷代谢调控机制奠定理论基础。
结果
基因组组装与注释
瑞昌山药茎秆纤细,呈绿色或紫红色,为右旋缠绕 生长;叶片多对生,心形至三角卵形;叶腋处常形成珠芽(地上块茎)。地下块茎呈圆柱形,长 60--80 cm,直径 6--8 cm,外皮黄褐色、肉质洁白。流式细胞术预估山药基因组大小约 1.6 Gb;k-mer 分析证实该物种为四倍体 ,基因组杂合度高达 3.9%。根尖压片染色观察共鉴定出 80 条染色体,单套单倍型染色体数为 20,核型为 2n=4x=80。
本研究共获得 41.20 Gb PacBio HiFi 长读长数据与 76.47 Gb 二代短读长数据,利用 hifiasm 软件完成四套单倍型从头组装 ;去除冗余序列后,组装基因组总长 1.56 Gb,contig N50 达 4.83 Mb。利用 268.12 Gb Hi-C 染色质互作数据(测序深度约 175×),对每套单倍型分别进行染色体挂载与排序,最终组装得到四组完整假染色体,每组含 20 条染色体。流程简述:将 Hi-C 测序读长比对至基因组草图,依据最优比对结果完成单倍型拆分;利用单倍型特异的染色质互作信号,完成 contig 的聚类、定位与方向矫正;整合全局 Hi-C 互作图谱优化挂载效果,人工修正错配片段,最终获得分型完整的四倍体单倍型参考基因组 。
四条单倍型分别命名为 Hap1、Hap2、Hap3、Hap4,组装总长依次为 393.53 Mb、380.31 Mb、325.91 Mb、323.70 Mb。与二倍体大薯基因组共线性分析显示:二者同源性极高,大薯的每条染色体,均可在山药四倍体基因组中对应四条同源假染色体,分别匹配四套单倍型,印证了山药同源四倍体的基因组特征。
|-----------------------------------------|------------------|
| Statistics | Value |
| Genome assembly | |
| Contig sequence total/count | 1562.96 Mb/653 |
| Contig N50 length/count | 4.83 Mb/105 |
| Contig N90 length/count | 1.32 Mb/351 |
| Scaffolds length total/count | 1437.24 Mb/80 |
| Scaffold N50 length/count | 19.04 Mb/32 |
| Scaffold N90 length/count | 13.53 Mb/68 |
| Hap1 total/count | 393.53 Mb/116 |
| Hap2 total/count | 380.31 Mb/117 |
| Hap3 total/count | 325.91 Mb/109 |
| Hap4 total/count | 323.70 Mb/120 |
| Genome annotation | |
| Total predicted gene/annotation gene | 98 699/95 668 |
| Repetitive sequences | 887.18 Mb/61.88% |
| Number of genes with GO annotation | 68 615 |
| Number of genes with KOG annotation | 82 632 |
| Number of genes with NR annotation | 95 647 |
| Number of genes with Swiss annotation | 70 412 |
| Number of genes with TrEMBL annotation | 93 331 |
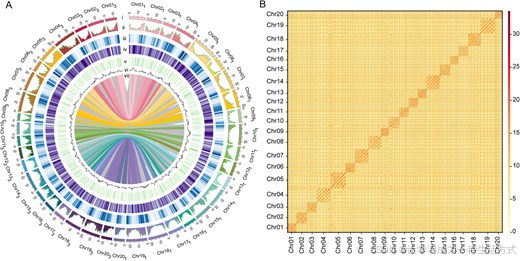
图 1 山药基因组各特征组分分布
(A) 山药基因组全景图谱。由外至内依次展示:(i) 染色体分布、(ii) 基因密度、(iii) 转座元件密度、(iv) 基因表达量、(v) 非编码 RNA 含量、(vi) GC 含量、(vii) 不同染色体间旁系同源基因分布;采用 500 kb 滑动窗口 分析。(B) 全基因组 Hi-C 互作热图,展示各染色体对应的 4 套单倍型(Hap1、Hap2、Hap3、Hap4)。
本研究利用通用单拷贝直系同源基因评估(BUSCO)检验基因组组装完整性。在 1614 条陆生植物核心 BUSCO 基因中,山药基因组完整单拷贝及重复基因占比达 96.4%(表 S5)。结合同源比对预测、从头预测与转录组证据 联合注释蛋白编码基因,共鉴定 98 699 个基因;基因平均长度 3440 bp,平均外显子长度 252 bp,单个基因平均含 5.25 个外显子(表 1)。通过公共数据库完成功能注释的基因共 95 668 个,占全部基因的 96.9%(表 1、图 S4)。四套单倍型基因组重复序列总长 887.18 Mb,占组装基因组总长的 61.9%(表 1)。
山药不同单倍型的差异表达解析
为解析山药每条染色体 4 套单倍型的进化关系,将山药基因组与圆薯蓣(Dioscorea rotundata )基因组比对,共鉴定获得 4 937 003 个单核苷酸变异(SNP),并利用 SNP 构建各组假染色体的系统发育树。结果显示:在 20 条假染色体中,16 条染色体的 Hap1 与 Hap2 进化关系更近,Hap3 与 Hap4 亲缘关系更近(图 S5),表明 4 套单倍型可划分为两大谱系:Hap1/Hap2 分支 与 Hap3/Hap4 分支 (图 2A)。
统计各组单倍型间的序列变异(SNP、插入缺失 InDel)以量化遗传分化:Hap1 与 Hap2、Hap3 与 Hap4 之间的变异数量,显著低于其他单倍型组合(图 2B、表 S6、表 S7)。系统发育与基因组变异特征高度一致,进一步证实本研究单倍型分型结果准确可靠 。
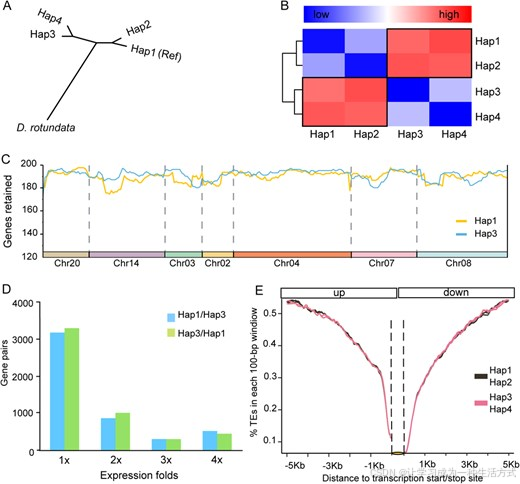
图 2 山药染色体单倍型分型与亚基因组优势分析
(A) 基于 4 937 003 条染色体特异性 SNP 聚类分析,将基因组稳定划分为两大分支。以圆叶山药(Dioscorea rotundata )为外类群,Hap1~Hap4 代表分型完成后的四套染色体。以 01 号染色体为代表性示例,其余多数染色体均呈现一致进化规律。(B) 亚基因组间序列变异热图。每个色块代表两个亚基因组之间的 SNP 密度与插入缺失(InDel)差异关系,颜色深浅反映变异程度高低。(C) 山药两个亚基因组代表性染色体的基因密度差异。展示两套亚基因组代表性染色体上连续区段的基因密度分布,无明显大片段断裂;基因密度采用 200 kb 滑动窗口计算。(D) 山药两个亚基因组旁系同源基因对的优势表达基因数量统计。蓝色:Hap1 基因表达量高于 Hap3 同源基因(表达倍数>1、2、3、4 倍);绿色:Hap3 基因表达量高于 Hap1 同源基因(表达倍数>1、2、3、4 倍)。(E) 不同基因集上下游侧翼区域的转座元件(TE)分布。以转录起始位点上下游各 5 kb 范围为研究区间,采用 100 bp 滑动窗口计算 TE 密度;黄色椭圆标注基因本体区域。
结合单倍型系统发育聚类结果(Hap1/Hap2、Hap3/Hap4 分别构成同源配对,图 2A、2B),本研究选取 Hap1、Hap3 作为四倍体山药基因组中两套二倍体假基因组的代表,评估二者的分化水平。Hap1 包含 25 679 个基因,Hap3 包含 24 056 个基因。为排除结构变异干扰,仅分析共线性区域,分别在 Hap1、Hap3 中鉴定到 17 258 与 17 356 个共线性基因,说明Hap1 并未比 Hap3 保留更多基因,基因含量无显著优势 (图 2C)。
进一步验证两套亚基因组的转录表达是否均衡:利用山药块茎转录组测序(RNA-seq)数据,分别检测到 Hap1 表达基因 20 681 个、Hap3 表达基因 20 056 个。关键结果:两套亚基因组共线性旁系同源基因对之间表达水平无显著偏向性 (TPM≥2),不存在明显的表达优势亚基因组(图 2D、表 S8)。同时统计共线性区域转座元件分布,基因上下游侧翼区域的 TE 密度在两套假基因组间也高度相近(图 2E)。
对 Hap1 与 Hap3 基因序列比对发现:二者序列保守性极高,超过 95% 的同源基因对序列相似度>95% (图 3A)。对茎、根、块茎外皮、块茎肉质等多组织进行单倍型特异表达分析,结果显示:茎、根、块茎外皮、块茎肉质中,单倍型特异表达基因占比分别仅为 2.2%、2.4%、1.7%、1.5%(图 3B、表 S9);仅 86 个表达基因在四种组织中呈现显著的单倍型特异性差异表达(图 3C)。
双等位均衡表达基因的 Ka/Ks 比值显著更低(图 3D),表明 Hap1 与 Hap3 之间表达均衡的基因,在进化上更为保守,显著区别于单倍型表达失衡的基因。综上证实:同源四倍体山药各单倍型之间不存在明显的亚基因组表达优势 。
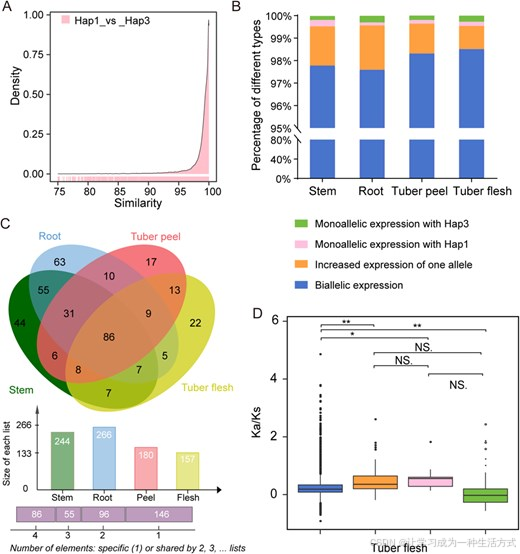
图 3 山药等位基因特异性表达特征
(A) 两个单倍型(Hap1 与 Hap3)等位基因编码序列差异比较。(B) 茎、根、块茎外皮与块茎肉质组织中的等位基因特异性表达(ASE)模式。Hap1 与 Hap3 等位基因 TPM 均>2、且表达差异小于 2 倍,定义为双等位均衡表达 ;双等位基因 TPM 均>2、但表达差异大于 2 倍,定义为单等位基因优势上调表达 ;仅其中一个单倍型等位基因 TPM>2、另一等位基因 TPM≤2,分别定义为 Hap1 优势表达 或 Hap3 优势表达 。(C) 四种组织中等位基因特异性表达基因的韦恩交集分析。(D) 块茎肉质组织中不同类型等位特异性表达基因的 Ka/Ks 比值分布;圆点代表离群值,箱体表示四分位距。*P ≤ 0.05;**P ≤ 0.001(t 检验)。
山药全基因组复制事件与系统发育关系分析
为解析山药物种进化历程,本研究通过计算共线性基因对的同义替换率(Ks )分布,识别全基因组复制(WGD)事件信号。基于 Ks 峰值特征,在山药基因组中共检测到三次全基因组复制事件:
- 近期山药物种特异性四倍化事件 (Ks =0.020),对应 Hap1/Hap2 与 Hap3/Hap4 两大单倍型类群的分化时间;
- 两次谱系共有古老复制事件:分别为薯蓣科保守的 δ 事件(Ks =0.82)、单子叶植物保守的 τ 事件(Ks =1.18)。
同时,估算得到山药与大薯的物种分化 Ks 为 0.063。综上,山药特有的近期全基因组复制事件直接导致其同源四倍化,证实瑞昌山药 为典型同源四倍体 物种。
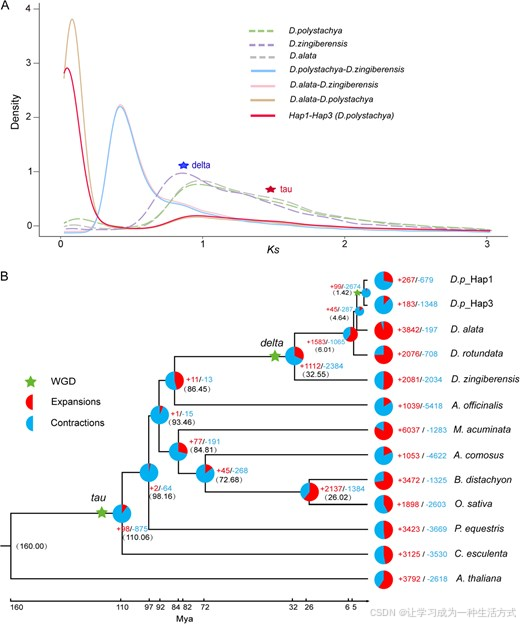
图 4 多花薯蓣的同源四倍体化事件
(A) 同义替换率(Ks)分析表明,多花薯蓣在演化过程中发生了一次近期、物种特异性的全基因组复制事件。(B) 多花薯蓣与其他 11 种植物的系统发育树。饼图展示了基因家族整体变化中扩张与收缩的基因家族占比;各分支节点标注了估算的分化时间(百万年前,Mya);五角星代表三次全基因组复制事件。
本研究选取 923 个共有单拷贝基因,构建了包含大薯、圆叶薯蓣、盾叶薯蓣在内的 12 种植物的时间校正系统发育树。系统基因组学分析结果显示,薯蓣科与其他单子叶植物类群的分化时间约为8645 万年前 ;盾叶薯蓣约在3255 万年前 从薯蓣属类群中分化出来;而多花薯蓣与其近缘物种大薯的分化时间仅约464 万年前 (图 4B)。分子定年结果显示,τ、δ 两次古老全基因组复制事件,以及多花薯蓣特有四倍体化全基因组复制事件,分别发生于 1.10 亿年前、3200 万年前与 142 万年前(图 4B)。
本研究利用大薯与多花薯蓣基因组的共线性基因对进行分析,以多花薯蓣共线性基因数 ÷(大薯共线性基因数 × 4) 计算背景基因保留率,结果为 91.3%。该高基因保留率,与多花薯蓣和大薯分化时间较短的演化背景相符。值得注意的是,参与薯蓣皂苷生物合成通路的基因保留率更高,达 98.4%,说明该类基因在多花薯蓣基因组中几乎完整保留 4 个拷贝(单倍型各 1 个)。此外,该合成通路中的 6 个基因家族还通过串联重复事件进一步发生拷贝数扩张,分别为 GGPP、24 - 甾醇甲基转移酶 1 型(SMT1)、C4 - 甾醇甲基氧化酶 1(SMO1)、CYP72A、CYP90B 及 CYP94 基因家族(附表 11)。基于块茎组织转录组测序数据发现,上述基因在 4 套单倍型中普遍存在单倍型表达分化现象(附表 11)。综上表明:相较于大薯,多花薯蓣的四倍体化进程,通过提升关键基因拷贝数、分化基因表达模式两种途径,强化了薯蓣皂苷的生物合成能力。
Dp7-DR 基因在多花薯蓣薯蓣皂苷积累中的作用
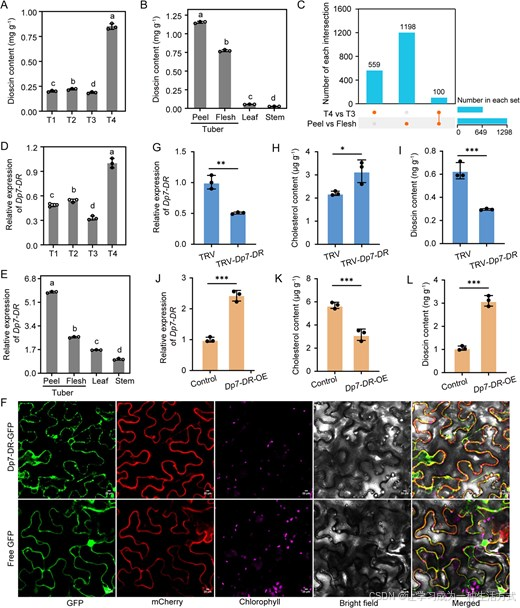
以多花薯蓣 1 号单倍型基因组为参考,对种植后 150 d(T1)、170 d(T2)、190 d(T3)、210 d(T4)四个块茎发育时期开展时序转录组测序分析(附图 6)。测序平均产出 8.65 Gb 高质量清洁读段,平均基因组比对率达 96.0%(附表 12)。通过四个发育时期的两两差异比较筛选差异表达基因,并经 K-means 聚类分析将差异基因划分为 9 个共表达模块(附图 6B、6C)。本团队前期研究证实,T2 至 T4 阶段为薯蓣块茎快速发育期 21。其中,4 号与 6 号模块的差异基因在 T4 时期高表达,且显著富集于类固醇生物合成 与植物激素信号转导 KEGG 通路(附图 6D)。薯蓣块茎主要活性甾体皂苷 ------ 薯蓣皂苷的含量在 T4 发育时期达到峰值(图 5A);组织分布结果显示,块茎表皮与肉质组织的皂苷含量显著高于叶片和茎段,且块茎表皮含量高于块茎肉质组织(图 5B)。
图 5 薯蓣皂苷生物合成关键基因的鉴定
(A、B) 多花薯蓣块茎不同发育时期 (A) 与不同组织 (B) 的薯蓣皂苷含量。T1~T4 代表四个快速生长阶段(种植后 150、170、190、210 天)。数据为三次生物学重复的平均值 ± 标准差(n=3)。单因素方差分析(ANOVA)结果显示,不同小写字母代表组间差异显著(P<0.05)。(C) 不同比较组合的差异表达基因数量。UpSet 图横坐标为各组鉴定到的差异表达基因总数,纵坐标为各特有基因集的差异基因数量。(D、E) 实时荧光定量 PCR(RT-qPCR)检测多花薯蓣块茎不同发育时期 (D) 及不同组织 (E) 中Dp7-DR 的相对表达量。特异性引物序列见附表 2;以ACTIN 作为内参基因。各样品设置三次生物学重复,采用2−ΔΔCt法定量基因转录水平。(F) Dp7-DR 在本氏烟草叶片中的亚细胞定位。利用德国蔡司 LSM 880 激光共聚焦显微镜,分别采集表达 Dp7-DR-GFP 融合蛋白(上图)与空载 GFP(下图)的叶片共聚焦图像,参数设置:绿色荧光蛋白 GFP 激发波长 488 nm、内质网标记蛋白 SPER-mCherry 激发波长 561 nm、叶绿素自发荧光激发波长 640 nm。GFP:绿色荧光蛋白;SPER-mCherry:内质网定位标记;Chlorophyll:叶绿素自发荧光;Merged:GFP 荧光、内质网荧光、叶绿素自发荧光与明场图像叠加。比例尺:20 μm。(G--L) 多花薯蓣珠芽中Dp7-DR 基因沉默(G--I)与过表达(J--L)处理下,Dp7-DR 相对表达量(G、J)、胆固醇含量(H、K)及薯蓣皂苷含量(I、L)。数据为三次重复平均值 ± 标准差(n=3)。TRV:pTRV1 载体与空载体 pTRV2 共侵染;TRV-Dp7-DR :pTRV1 与重组载体 pTRV2-Dp7-DR 共侵染。∗P<0.05;∗∗P<0.01;∗∗∗P<0.001(t 检验)。
为筛选调控薯蓣皂苷积累的核心基因,本研究对比分析了块茎 T3、T4 时期,以及块茎表皮与肉质组织的差异表达基因,分别鉴定到 659 个和 1298 个差异基因,其中两组共有差异基因 100 个(图 5C)。在上述基因中,编码 7 - 脱氢胆固醇还原酶(7-DR)的Dp7-DR (基因编号:DpolyH1c03G000046),被注释参与类固醇生物合成 KEGG 通路(ko00100)(附图 7A)。对多花薯蓣四个单倍型中薯蓣皂苷合成通路基因(附表 10)进行表达分析发现,Dp7-DR 的四个等位拷贝(DpolyH1c03G000046、DpolyH2c03G000045、DpolyH3c03G000049、DpolyH4c03G000003)均呈高表达模式,且表达量与薯蓣皂苷含量高度相关(附图 7B、7C;附表 13)。四个单倍型的Dp7-DR 序列完全一致(附图 8A)。本研究克隆获得长度为 1305 bp 的Dp7-DR 开放阅读框(附图 8B),编码 434 个氨基酸;系统进化分析显示,该蛋白与大薯Da7-DR 、圆叶薯蓣Dr7-DR 同源蛋白聚为一支(附图 8C;附表 14)。Dp7-DR 在块茎 T4 发育时期表达量达到峰值,且在块茎表皮与肉质组织中优势表达(图 5D、5E),与薯蓣皂苷的富集规律一致。通过在本氏烟草叶片瞬时表达 Dp7-DR-GFP 融合蛋白开展亚细胞定位实验,结果显示 GFP 荧光信号与内质网标记蛋白信号共定位(图 5F),证实 Dp7-DR 主要定位于内质网。该定位特征与其作为甾醇合成通路关键酶的生物学功能相符,进而调控薯蓣皂苷的合成积累。
为明确Dp7-DR 在薯蓣皂苷生物合成中的生物学功能,本研究采用病毒诱导基因沉默(VIGS)与瞬时过表达技术,在多花薯蓣珠芽中开展功能验证(图 5G--L、附图 9)。与对照组相比,Dp7-DR 基因沉默珠芽中,基因转录水平显著下调(图 5G),胆固醇含量升高、薯蓣皂苷含量显著降低(图 5H、5I);反之,珠芽中过表达Dp7-DR 后,胆固醇含量下降,薯蓣皂苷积累量显著提升(图 5J--L)。综上结果表明,Dp7-DR 正向调控多花薯蓣中薯蓣皂苷的积累。
DpbZIP12 结合 Dp7-DR 启动子并激活其转录
利用 PlantCARE 数据库预测分析显示,Dp7-DR 启动子区域含有 11 个脱落酸响应元件(ABRE)(图 6A;附表 15)。脱落酸响应元件可响应脱落酸(ABA)信号,并被碱性亮氨酸拉链(bZIP)A 亚家族转录因子特异性识别。外源脱落酸处理 12 h 后,多花薯蓣薯蓣皂苷含量上升,同时Dp7-DR 表达量显著上调(图 6B、6C)。转录组数据表明,编码 bZIP A 亚家族蛋白的DpbZIP12 在多花薯蓣块茎中高表达,且其表达量与薯蓣皂苷含量呈显著正相关(图 6D、附图 11A)。为探究DpbZIP12 对薯蓣皂苷积累的调控机制,进一步验证 DpbZIP12 是否直接结合Dp7-DR 启动子。酵母单杂交(Y1H)实验证实,DpbZIP12 蛋白可在酵母体内结合Dp7-DR 启动子(图 6E)。双荧光素酶报告实验用于验证 DpbZIP12 对Dp7-DR 启动子活性的调控作用(图 6F);将DpbZIP12 效应载体与Dp7-DR 启动子驱动萤火虫荧光素酶(LUC)的报告载体共转化本氏烟草叶片后,叶片荧光活性显著高于对照组(图 6G)。凝胶迁移阻滞实验(EMSA)选用含 bZIP 结合位点的Dp7-DR 启动子片段作为探针,结果显示,纯化的 MBP-DpbZIP12 重组蛋白可结合生物素标记探针;加入未标记竞争探针后,特异性结合条带强度明显减弱(图 6H)。以上实验共同证实,DpbZIP12 可直接结合Dp7-DR 启动子,进而激活该基因的转录表达。
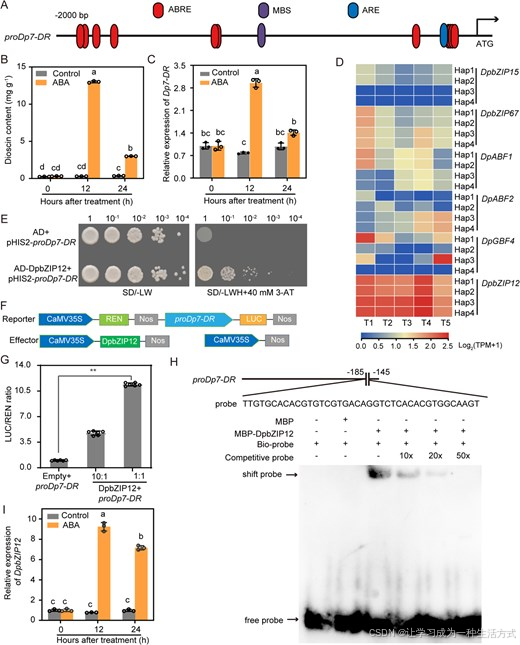
图 6 DpbZIP12 直接结合 Dp7-DR 启动子并激活其表达
(A) 利用 PlantCARE 数据库对Dp7-DR 基因启动子顺式作用元件进行预测。(B、C) 100 μmol/L 脱落酸(ABA)处理下的薯蓣皂苷含量 (B) 与Dp7-DR 相对表达量 (C)。数据为 3 组独立生物学重复的平均值 ± 标准差;不同小写字母表示经单因素方差分析(ANOVA)检验差异显著(P<0.05)。(D) A 亚家族 bZIP 转录因子编码基因在 4 个块茎发育时期(T1--T4)、4 套单倍型中的表达热图。(E) 酵母单杂交试验验证 DpbZIP12 与Dp7-DR 启动子的结合。将 pHIS2-proDp7-DR 与 AD-DpbZIP12 质粒共转化 Y1H Gold 酵母菌株。AD:GAL4 激活域;SD/−LW:缺失亮氨酸、色氨酸的合成缺陷培养基;SD/−LWH:缺失亮氨酸、色氨酸、组氨酸的合成缺陷培养基;3-AT:3 - 氨基 - 1,2,4 - 三唑。(F) 双荧光素酶报告实验载体构建示意图。将Dp7-DR 启动子克隆至 pGreenII-0800-LUC 载体的萤火虫荧光素酶(LUC)报告基因上游;DpbZIP12 克隆至 pGreenII-62-SK 载体,作为效应载体。(G) 双荧光素酶实验证明 DpbZIP12 可激活Dp7-DR 启动子的转录活性。以空载体 pGreenII-62-SK 为阴性对照;含 pGreenII-62-SK-DpbZIP12 与 pGreenII-0800-LUC-proDp7-DR 的农杆菌菌液分别按 10:1、1:1 体积比混合侵染。数据为平均值 ± 标准差(n=6);对照组与 1:1 混合组采用 t 检验进行差异分析,P<0.01 。(H) 凝胶迁移实验(EMSA)验证纯化重组蛋白 MBP-DpbZIP12 与 Dp7-DR 启动子的结合能力。生物素标记探针与 MBP-DpbZIP12 蛋白共孵育,非标记探针用作竞争探针。MBP:麦芽糖结合蛋白;pro Dp7-DR : Dp7-DR 启动子。(I) 100 μmol/L ABA 处理下 DpbZIP12 的相对表达量。数据为 3 组独立重复平均值 ± 标准差;* P<0.05 、 P<0.01、***P<0.001(t 检验)。
外源 ABA 处理 12 h 内可显著诱导DpbZIP12 表达上调(图 6I)。在珠芽中沉默DpbZIP12 后,Dp7-DR 转录水平显著降低(图 7A、B),造成胆固醇大量累积、薯蓣皂苷含量下降(图 7C、D)。反之,过表达DpbZIP12 能够降低胆固醇含量,同时上调Dp7-DR 表达并促进薯蓣皂苷积累(图 7E--H)。综上表明,DpbZIP12 可结合并激活Dp7-DR 启动子,上调该基因表达,进而正向促进薯蓣皂苷的生物合成。
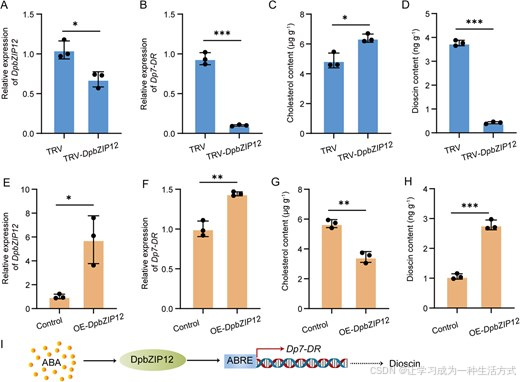
图 7 DpbZIP12 促进珠芽中薯蓣皂苷的积累
(A--H) DpbZIP12 (A、E)与Dp7-DR (B、F)的相对表达量、胆固醇含量(C、G)及薯蓣皂苷含量(D、H);其中 A--D 为DpbZIP12 基因沉默材料,E--H 为DpbZIP12 过表达材料。采用附表 2 所列引物进行实时荧光定量 PCR 检测,以ACTIN 为内参基因。所有样品设置三组生物学重复,通过2−ΔΔCt法定量基因转录水平。数据为三次重复的平均值 ± 标准差(n=3);∗P<0.05、∗∗P<0.01、∗∗∗P<0.001(t 检验)。TRV:pTRV1 与空载体 pTRV2 共侵染,作为阴性对照;TRVDpbZIP12 :pTRV1 与重组载体 pTRV2DpbZIP12 共侵染。(I) ABA 介导调控薯蓣皂苷生物合成的作用模型:DpbZIP12 通过激活Dp7-DR 的转录,正向调控薯蓣皂苷合成。
讨论
近期全基因组复制事件形成多花薯蓣同源四倍体,并促进薯蓣皂苷生物合成
多倍化与植物物种分化密切相关,在植物基因组进化中发挥关键作用 22。单子叶植物共有 τ 全基因组复制事件、薯蓣属物种特有 δ 全基因组复制事件;除此之外,多花薯蓣在与其近缘测序物种大薯分化后,于约 142 万年前发生了物种特异性全基因组复制事件(图 4),最终形成同源四倍体基因组 23。
多倍化可赋予植物诸多重要农艺优势,例如器官增大、缓冲有害突变、提升杂合度等。利用多倍化优良性状,有助于培育高产、优质、抗逆性更强的作物品种 24-26。例如,四倍体马铃薯与紫花苜蓿的产量显著高于二倍体植株 27-28;玉米多倍化可大幅促进类胡萝卜素积累,人工四倍体玉米籽粒中类胡萝卜素含量可达二倍体的 2.2 倍 29;天然四倍体拟南芥可通过调控叶片钾离子稳态,显著增强耐盐性 30。已有研究证实,二倍体近缘种大薯与多花薯蓣的薯蓣皂苷含量存在显著差异 18,本研究进一步证实:多倍化是多花薯蓣薯蓣皂苷大量积累的重要驱动力 。
全基因组复制后基因拷贝数增加与基因剂量效应,是多花薯蓣薯蓣皂苷富集的核心原因之一。相较于二倍体大薯,多花薯蓣中薯蓣皂苷合成通路关键基因的保留率更高、拷贝数量更多(附表 11)。六倍体亚麻荠中,3 个FAD2 同源基因经基因编辑产生序列变异,可形成油脂组分差异极大的株系,油酸含量跨度为 10%~62%,证明等位基因剂量可累加调控代谢性状 31。甘薯全基因组关联分析同样发现大量受剂量效应调控的农艺性状:扩张蛋白基因IbEXPA4 的表达与优异等位基因剂量负相关,进而调控块根重量;肉质颜色相关基因IbOr 的单倍型剂量则正向调控薯肉着色 32。此外,穿龙薯蓣与盾叶薯蓣中,CYP90 、CYP94 、UGT73 基因家族扩张,同样显著促进薯蓣皂苷合成与积累 5,18。
大薯起源于东南亚,主要分布于热带、亚热带区域;而多花薯蓣耐寒性更强,广泛种植于温带地区,是我国种植面积最大的薯蓣作物,生态适应性更广 33。研究表明,薯蓣属中仅不足 33% 的物种存在倍性分化,且同一物种内部也常出现倍性差异 14。长期无性繁殖会诱导多倍体产生,是植物适应极端环境、提升抗逆能力的重要进化策略 34。多倍化驱动基因家族扩张,再通过基因片段化分化,促使基因发生亚功能化与新功能化,最终提升植物的环境适应性与基因组可塑性。
脱落酸与 DpbZIP12 协同调控多花薯蓣薯蓣皂苷合成
植物激素可通过调控关键合成酶基因的表达,广泛参与植物皂苷等次生代谢物的合成调控。脱落酸(ABA)是植物次生代谢的核心调控激素 35,可促进番茄黄酮合成 36、柑橘果实类胡萝卜素积累 37-38、工业大麻萜类物质合成 39 以及青蒿中青蒿素代谢 40。目前关于薯蓣皂苷合成的分子调控机制研究仍较薄弱。本研究发现,外源 ABA 处理 12 h 可显著提升薯蓣皂苷含量,处理 24 h 后含量回落(图 6)。短期 ABA 可通过上调合成通路关键基因,快速诱导次生代谢物积累;但持续激素处理会激活负反馈通路,诱导 PP2C、SnRK2 等 ABA 信号负调控因子表达,加速代谢物降解,避免次生代谢物过度累积产生细胞毒性 41。同时,长期激素胁迫会促使植物将能量优先用于细胞膜修复、渗透平衡维持等基础生命活动,减少次生代谢底物供给,进而降低代谢物合成 42。因此推测:单次 ABA 诱导可显著促进薯蓣皂苷积累,而持续处理会触发反馈抑制,导致次生代谢水平下降 。
bZIP 转录因子是 ABA 信号通路的核心调控元件 43-44。柑橘中 CsbZIP44 可结合类胡萝卜素合成基因启动子,激活基因表达,介导 ABA 调控类胡萝卜素代谢 37-38;青蒿 AabZIP1 通过激活ADS 与CYP71AV1 ,促进青蒿素合成 45;丹参 SmbZIP7/SmbZIP20 调控丹参酮与青蒿素代谢 46;水稻 OsbZIP79 参与二萜类植保素合成调控 47;天门冬中两个 bZIP 蛋白可直接结合甾体皂苷合成关键基因ArSQE 的启动子 48。尽管 bZIP 家族广泛调控植物次生代谢,但其在薯蓣皂苷合成中的功能,尤其在薯蓣属物种中尚未被报道。本研究鉴定得到 ABA 响应型转录因子 DpbZIP12,该蛋白可直接结合Dp7-DR 启动子,精准调控薯蓣皂苷合成(图 6、图 7、附图 10)。对DpbZIP12 沉默与过表达珠芽的差异基因分析显示,18 个富集于 "植物激素信号转导" 通路的差异基因特异性参与 ABA 信号通路,包括 PYL 受体、PP2C 磷酸酶、SnRK2 激酶、ABF 转录因子及 ABI5 等核心元件(附图 11C)。后续仍需深入解析 ABA 信号蛋白与转录因子的互作网络,完善薯蓣皂苷的分子调控通路。
全球薯蓣属物种约 600 余种,但商业化栽培品种极少,蕴藏巨大育种与基因资源挖掘潜力。结合现有基因组数据与代谢关键基因鉴定结果,可进一步筛选薯蓣皂苷合成、转运与积累的核心靶点基因。例如,盾叶薯蓣中CYP94D144 启动子区 SNP 变异与薯蓣皂苷元含量显著关联,可作为分子育种标记基因 49;利用 CRISPR/Cas9 基因编辑技术上调该基因表达,可定向提升皂苷含量、加速分子育种进程。本研究明确了DpbZIP12--Dp7-DR 核心调控模块对薯蓣皂苷含量的调控作用,为解析薯蓣皂苷合成机制、培育高皂苷薯蓣新品种提供了关键靶点与理论依据。
总结
本研究完成了多花薯蓣同源四倍体的单倍型水平染色体级别基因组 组装。该物种除拥有单子叶植物保守 τ 全基因组复制事件、薯蓣属特有 δ 全基因组复制事件外,还在约 142 万年前发生物种特异性全基因组复制,最终形成同源四倍体基因组。相较于二倍体近缘种大薯,多花薯蓣薯蓣皂苷合成通路基因的整体保留率显著更高(98.4% vs 91.3%)。功能验证表明,Dp7-DR 是薯蓣皂苷合成的关键结构基因;同时鉴定出全新调控因子 DpbZIP12,该转录因子可激活Dp7-DR 转录,正向促进薯蓣块茎中薯蓣皂苷的合成与积累(图 7I)。
材料与方法
植物材料与处理
本试验所用山药材料为多花薯蓣栽培品种'瑞昌山药',种植于中国江西省南昌市江西农业大学试验基地(北纬 28°45′53″,东经 115°49′41″)。采集幼嫩叶片用于全基因组测序,同时收集根、幼茎及块茎样品开展转录组测序分析。采用 100 μmol/L 脱落酸(ABA)喷施山药叶片,分别于处理后 0 h、12 h、24 h 随机取样,样品经液氮快速冷冻后置于−80 ℃超低温冰箱保存备用。
基因组大小评估
利用SOAPnuke(v1.6.5) 对 Illumina 短读长测序数据进行质控预处理;再通过 GenomeScope 软件结合多组 k-mer 参数评估基因组大小。同时,分别采集多花薯蓣与大豆(内参对照)新鲜叶片,制备纯化细胞核,经碘化丙啶(PI)染色后,采用 FACSCalibur 流式细胞仪测定细胞核 DNA 含量,辅助验证基因组大小 50。
基因组组装、染色体挂载与亚基因组单倍型分型
利用 PacBio HiFi 长读长序列与 Hi-C 染色质互作数据,结合hifiasm(v0.19.3-r572) 软件完成多花薯蓣四倍体基因组组装;设置参数--n-hap 4,实现四条同源单倍型的分型组装,获得初步单倍型水平组装结果。
采用Purge_Dups(v1.2.5) 软件,按单倍型特异性去除杂合序列与冗余序列,优化组装质量。简要流程:通过minimap2(v2.28) 将 HiFi 长读长与二代短读长比对至初步组装基因组;依托 hifiasm 分型结果,运行split_paf.py脚本将比对结果划分为四组单倍型特异数据集;依据测序覆盖度信息,识别并剔除各单倍型的冗余片段。优化后四条单倍型基因组大小与流式细胞仪测定结果一致;同时与近缘物种大薯基因组比对验证,确保编码区序列未被错误删除。
染色体挂载环节:使用BWA-mem(v0.7.17) 将 Hi-C 测序读长比对至优化后的组装基因组;基于最优比对得分划分四组单倍型特异数据集,借助 HiC-Pro(v3.1.0)概率模型保留多重比对读长并完成单倍型分配。随后利用Allhic(v0.9.8) 流程分别对四个亚基因组进行染色体挂载:整合 Juicer(v1.5)、3D-DNA(180922)与 Juicebox(v1.11.08)工具,基于各单倍型特异 Hi-C 数据,为每条单倍型构建 20 条假染色体。
通过Nucmer(v3.23) 比对分析四条单倍型的同源关系,合并整合 Juicebox 组装文件并完成同源分组;结合全基因组 Hi-C 互作图谱开展人工校正。依据同单倍型染色质互作强度高于异单倍型 的原则,利用 Juicebox 修正 contig 跨单倍型错误分配问题;分析染色体间互作信号,重新排布各单倍型同源假染色体,保证同单倍型整体互作信号更强。最终获得包含 80 条假染色体的染色体水平基因组,每条单倍型各含 20 条染色体。
基因组注释
联合多种策略预测蛋白编码基因:整合Genemark(v4.61_lic) 、AUGUSTUS(v3.3.3) 的从头预测结果;结合多物种同源蛋白注释证据,包括非冗余蛋白库(Nr)、真核直系同源基因数据库(KOG)、基因本体数据库(GO)、瑞士蛋白库(Swiss-Prot)、TrEMBL 数据库;同时利用 Trinity(v2.11.0)对多花薯蓣转录组数据进行从头组装,作为转录本辅助注释证据。
采用RepeatModeler 软件从头预测多花薯蓣基因组重复序列,构建物种特异性重复序列库;再通过RepeatMasker 完成全基因组重复序列的注释与屏蔽。
薯蓣属物种全基因组共线性分析
以相邻共线性基因对为基础,解析亚基因组间大规模共线性区块。考虑局部结构变异与组装误差,若两个共线性片段间隔基因数<50 或物理距离<300 kb,则合并为一个完整共线性区块 65。
使用mSynOrths 默认参数,鉴定多花薯蓣与其他薯蓣科物种(盾叶薯蓣、大薯)的共线性直系同源基因。以大薯与多花薯蓣的共线性基因为背景,计算全局基因保留率(双物种共有共线性基因占总共线性基因对的比例);并采用相同分析体系,定量解析薯蓣皂苷合成通路基因的保留特征。
旁系同源基因表达量差异分析
利用多花薯蓣叶片与块茎转录组数据,比较单倍型间旁系同源基因的表达差异,重点分析 Hap1 与 Hap3 两组单倍型的旁系同源基因对。通过featureCounts 统计染色体基因 TPM 表达量,剔除 TPM<2 的低表达基因,仅分析功能表达基因。采用Salmon(v0.13.1) 默认参数完成转录本定量,系统评估各亚基因组的基因表达模式差异。
基因周围转座子的分布差异
采用100 bp 滑动窗口、10 bp 步长 分析多花薯蓣基因侧翼区域的转座子(TE)密度。具体方法:统计每个基因上游 5 kb 与下游 5 kb 范围内的转座子来源核苷酸数量,计算每 100 bp 窗口内转座子序列与非转座子序列的碱基占比。汇总所有基因的平均转座子占比并绘制分布图,以此评估基因上下游侧翼区的转座子密度特征。
同义替换率(Ks)分析
利用 Synorths 软件比对旁系同源与直系同源基因对的编码区序列,借助 KaKs_calculator 软件,采用 Nei-Gojobori 算法计算每个基因对的同义位点同义替换率(Ks)。分别开展种内比较(多花薯蓣、盾叶薯蓣、大薯)、种间比较(多花薯蓣--盾叶薯蓣、多花薯蓣--大薯、大薯--盾叶薯蓣),以及多花薯蓣内部 Hap1 与 Hap3 单倍型间的 Ks 分析。依据公式 Ks=2μT 估算分化时间,其中μ为年均替换速率,T为物种分化时间 16。
基因组进化分析
为解析多花薯蓣与近缘物种的系统发育关系,收集 12 个物种基因组数据(大薯、多花薯蓣、圆叶薯蓣、盾叶薯蓣、二穗短柄草、水稻、菠萝、小果野蕉、蝴蝶兰、芦笋、芋头、拟南芥)进行基因家族聚类分析。使用 OrthoFinder(v2.5.4)鉴定跨物种保守直系同源基因家族;通过 r8s(v1.81)构建超度量系统发育树;利用 PAML 软件包中的 MCMCtree 程序估算各进化分支节点的分化时间;采用 Cafe5 软件分析基因家族扩张与收缩动态,明确不同物种谱系的进化规律。
同源单倍型比较与转录组测序分析
借助 Nucmer 检测单倍型间 SNP 与 InDel 变异,设置 300 kb 滑动窗口量化全基因组变异密度,绘制变异分布热图,在染色体水平解析 6 组单倍型组合(H1--H2、H1--H3、H1--H4、H2--H3、H2--H4、H3--H4)的进化差异。结合多花薯蓣与近缘物种圆叶薯蓣的 SNP 位点,利用 IQ-TREE(v2.2.6)对 4 套同源染色体分别构建最大似然进化树,验证单倍型分型结果的准确性。
选取幼茎、根、块茎表皮与块茎肉质组织开展转录组测序分析。原始测序数据经质控修剪后,通过 HISAT2(v2.2.1)完成序列比对;采用 DESeq2 分析等位基因特异性表达,筛选阈值:错误发现率FDR<0.05、∣log2(倍数变化)∣>175。
将单倍型基因表达模式分为双等位均衡表达 与表达失衡 两大类;参考已有研究方法,将表达失衡进一步划分为:Hap1 单等位特异表达、Hap3 单等位特异表达、等位基因差异高表达 76。以根、茎、块茎表皮、块茎肉质四种组织的表达特征为判定标准:
- 双等位均衡表达:Hap1、Hap3 基因 TPM 均>2,且表达量差异小于 2 倍;
- 等位基因高差异表达:双单倍型 TPM 均>2,表达量差异≥2 倍;
- 单等位优势表达:仅其中一个单倍型 TPM>2,另一单倍型 TPM≤2,分别定义为 Hap1 优势表达或 Hap3 优势表达。使用 StringTie v2.1.4 计算外显子每千碱基转录本丰度与 TPM 表达量 77。
转录组数据集与基因表达模式聚类分析
采用 SOAPnuke(v1.6.5)对块茎 4 个发育时期(种植后 150 d T1、170 d T2、190 d T3、210 d T4)的转录组原始数据进行质控过滤;干净读长经 HISAT2 比对、Bowtie2(v2.4.5)组装与定量分析 78。基因表达量统一标准化为 TPM 79,利用 DESeq2 筛选差异表达基因,筛选条件:表达倍数>1.5、校正后P<0.05。通过 R 语言clusterProfiler程序包完成差异基因的 GO 功能、KEGG 通路富集分析及表达热图绘制 80。
基因克隆、亚细胞定位、实时荧光定量 PCR 与终点反转录 PCR
以多花薯蓣块茎 cDNA 为模板,使用 pClone007 通用克隆载体试剂盒克隆Dp7-DR 全长编码序列。通过 NCBI 数据库 BLASTP 检索其他物种 7 - 脱氢胆固醇还原酶同源蛋白序列(详见附表 14),利用 MEGA7 软件构建最大似然系统进化树 81。采用 PlantCARE 在线网站分析Dp7-DR 启动子序列及顺式作用元件。
亚细胞定位试验:扩增不含终止密码子的Dp7-DR 全长编码区,连接至 pBWA (V) HS-GLosgfp 载体(附表 16)。将重组载体与空载对照分别转化农杆菌 GV3101;阳性菌株于 LB 培养基培养后,重悬于侵染缓冲液(10 mM MES、120 μM 乙酰丁香酮、10 mM MgCl2,pH 5.6),调节OD600=0.6。农杆菌菌液与内质网标记载体 SPER-mCherry 按体积比 1:1 混合侵染本氏烟草叶片;侵染 3 d 后,采用蔡司 LSM 880 激光共聚焦显微镜观察绿色荧光信号。
采用宝生物植物总 RNA 提取试剂盒提取山药根、茎、叶、块茎总 RNA,经反转录获得第一链 cDNA。所有样品设置三组生物学重复,以ACTIN (DpolyH1c19G001005)为内参基因,采用2−ΔΔCt法进行荧光定量分析 4,基因特异性引物详见附表 16。
薯蓣珠芽病毒诱导基因沉默与瞬时过表达
利用植物基因组数据库 SGN 的 VIGS 在线工具预测基因沉默特异性片段 83,扩增目的片段并插入烟草脆裂病毒载体 pTRV2,重组载体转化农杆菌 GV3101。参考唐菖蒲侵染体系,在多花薯蓣珠芽中开展 VIGS 沉默试验 82:pTRV1 辅助载体与 pTRV2 载体菌液按 1:1 混合侵染;以 pTRV1 + 空 pTRV2 侵染组作为阴性对照。侵染后取样进行 RT-qPCR,检测基因沉默效率。
扩增候选基因全长编码序列,构建 pSuper1300 过表达载体(附表 16)。将含目的载体或空载对照的农杆菌重悬于侵染缓冲液,调节OD600=0.8,侵染多花薯蓣珠芽;取侵染部位组织,用于代谢物含量测定与基因表达检测。
薯蓣皂苷与胆固醇提取及含量测定
采用岛津 Nexera LC-30A 高效液相色谱串联 AB Sciex QTrap 4500 质谱仪(HPLC-MS/MS)定量检测薯蓣皂苷与胆固醇含量。简要步骤:取 200 mg 植物样品,加入 1.2 mL 异丙醇充分研磨,4 ℃超声提取 10 min,离心 10 min;上清经 0.22 μm 有机滤膜过滤,用于胆固醇检测。薯蓣皂苷检测样品需将上清低温旋蒸至干燥,70% 甲醇复溶后过滤。色谱分离条件:Waters Acquity UPLC BEH C18 色谱柱,柱温 45 ℃。采用动态多反应监测模式采集质谱数据,依据标准品保留时间设定靶向离子转换参数;结合外标标准曲线定量代谢物含量(附图 10)。
酵母单杂交、双荧光素酶报告实验与凝胶迁移实验
酵母单杂交(Y1H) :从多花薯蓣块茎 RNA 反转录 cDNA 中扩增DpbZIP12 全长编码序列,连接至 pGADT7 载体;从叶片基因组 DNA 扩增 475 bp 的Dp7-DR 启动子片段,插入 pHIS2 载体(附表 16)。将 pHIS2-proDp7-DR 报告载体与 pGADT7-DpbZIP12 效应载体共转化 Y187 酵母菌株 84;涂布于 SD/−Leu/−Trp 缺陷培养基培养 3 d。挑取阳性菌落稀释点板,分别接种于 SD/−Leu/−Trp 基础培养基与添加 40 mM 3 - 氨基 - 1,2,4 - 三唑的 SD/−Leu/−Trp/−His 筛选培养基。
双荧光素酶实验 :将DpbZIP12 全长序列克隆至 pGreenII 62-SK 效应载体,Dp7-DR 启动子片段连接至 pGreenII 0800-LUC 报告载体,分别转化农杆菌 GV3101;以空载体为阴性对照。将效应载体与报告载体农杆菌菌液混合后共侵染本氏烟草叶片。参照经典实验体系,采用 Promega 双荧光素酶检测试剂盒,通过 Synergy H1 多功能酶标仪测定萤火虫荧光素酶(LUC)与海肾荧光素酶(REN)活性,以LUC/REN 相对比值 评价启动子活性,每组实验独立重复 3 次以上 84。
凝胶迁移(EMSA) :通过 Gateway 克隆系统将DpbZIP12 全长序列重组至 pHMGWA 表达载体,获得 MBP-DpbZIP12 融合蛋白表达质粒;转化大肠杆菌 BL21,0.5 mM IPTG 诱导蛋白表达纯化。使用 Thermo 化学发光 EMSA 试剂盒,结合生物素标记的启动子探针开展结合试验;分别加入 10 倍、20 倍、50 倍浓度未标记竞争探针,验证结合特异性。反应产物经聚丙烯酰胺凝胶电泳分离,利用 Bio-Rad ChemiDoc XRS 成像系统采集发光信号。
统计学分析
采用 SPSS 19.0 软件进行配对双侧 t 检验,两组间差异显著性标注:∗P<0.05、∗∗P<0.01、∗∗∗P<0.001;绘图软件使用 Origin 8.0。所有试验数据均以平均值 ± 标准差 表示。