01
文献学习

今天分享的文献是由暨南大学附属第一医院张水兴教授团队于2026年4月24日在《Radiology: Imaging Cancer》(中科院2区,IF=6.3)上发表的研究"Deep Learning Model Based on Tumor and Visceral Adipose Tissue CT Features for Predicting Peritoneal Metastasis Risk after Radical Gastrectomy in Serosa-Invasive Gastric Cancer"即基于肿瘤和内脏脂肪组织CT特征的深度学习模型用于预测浆膜浸润性胃癌根治术后腹膜转移风险,该研究开发并验证了一种多模态深度学习模型(MDLR),该模型整合了术前CT图像中的肿瘤特征、内脏脂肪组织(VAT)特征及临床指标,用于预测浆膜浸润性胃癌患者根治术后腹膜转移(PM)的风险。模型在内部和外部测试集中均表现出良好的预测性能(AUC均为0.86),并能显著区分高、低风险患者的无复发生存期。
创新点:①融合肿瘤与内脏脂肪组织CT特征 :首次将两者深度特征结合,突破单一区域分析局限,更全面捕捉腹膜转移风险。②构建多模态深度学习模型(MDLR) :整合影像深度特征与临床指标,预测性能显著优于单一模型 ,AUC达0.86。③专注浆膜浸润胃癌术后风险 :针对T4a期同质高危人群实现有效风险再分层,弥补传统分期鉴别力不足。
临床价值:①术前无创预测,指导个体化治疗 :基于常规CT即可评估腹膜转移风险,辅助筛选腹腔内化疗(IPC)获益人群 ,避免过度治疗。②优化术后复发管理 :高风险组复发-free生存显著缩短,支持强化随访与辅助治疗决策 ,改善患者预后。③多中心验证,泛化能力可靠 :内外测试集AUC均达0.86,决策曲线显示明确临床净收益,具备推广潜力。
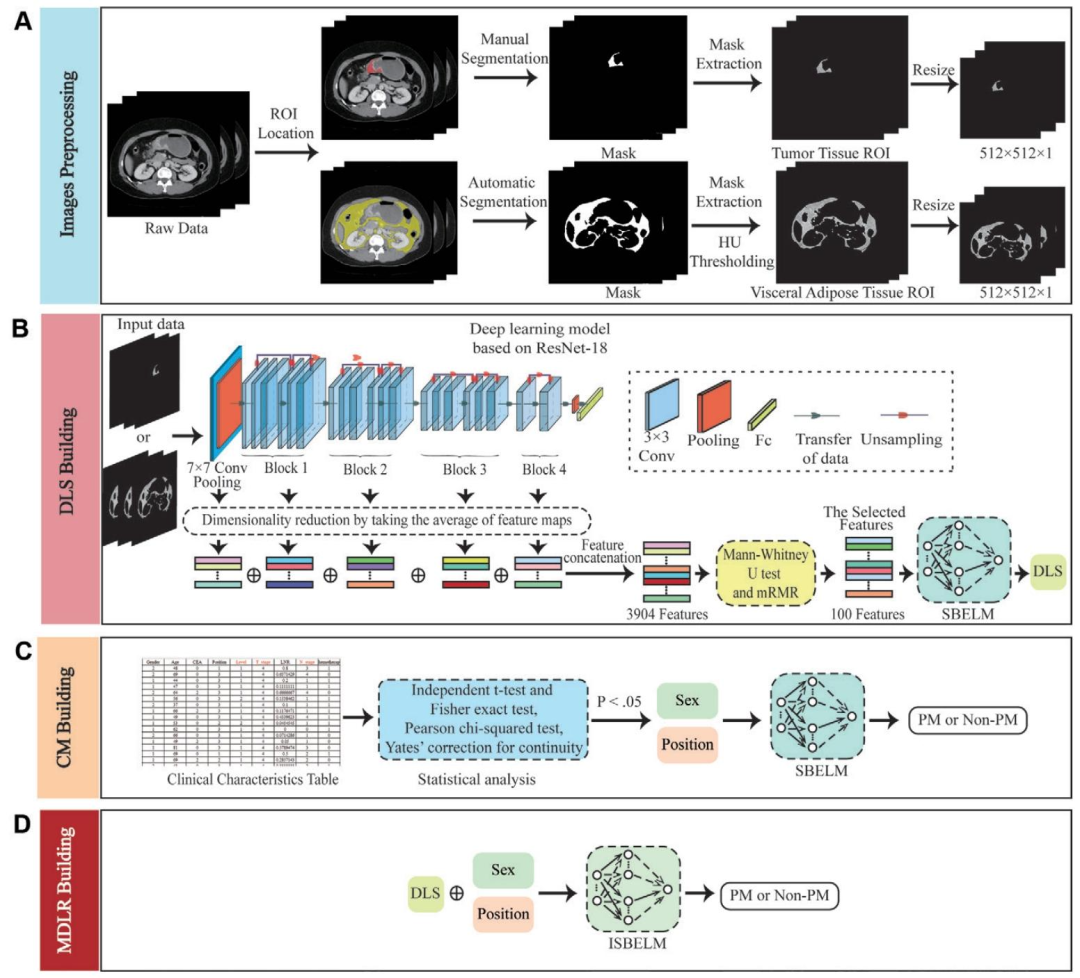
图 2:数据预处理、深度特征提取与模型构建工作流
A:数据处理流程
原始CT数据:获取静脉期CTHU值图像
肿瘤区域处理 :手动分割肿瘤ROI→提取掩码→resize为512×512
内脏脂肪组织(VAT)处理 :自动分割+人工修正→阈值处理→提取掩码→resize为512×512
B:基于ResNet18的深度学习特征(DLS)构建
输入:肿瘤/VAT的512×512 CT图像
网络:ResNet18(Block1-Block4卷积模块)
特征提取:卷积层输出3904维深度特征
特征筛选:Mann-Whitney U检验+mRMR算法→保留100个最优特征
分类器:SBELM(稀疏贝叶斯极限学习机)→输出PM/Non-PM预测
C:临床模型(CM)构建
输入:临床指标(性别、肿瘤位置,经单因素分析筛选)
统计检验:卡方检验、t检验、Fisher精确检验(P<0.05为有意义)
分类器:SBELM→构建临床预测模型
D:多模态深度学习放射组学模型(MDLR)构建
输入:融合深度学习特征(F-DLS)+临床指标
分类器:ISBELM(集成SBELM)
输出:最终腹膜转移风险预测结果
02
研究背景和目的
研究背景
胃癌是全球第五大常见恶性肿瘤,也是癌症相关死亡的第三大主要原因。腹膜转移是胃癌术后最常见的转移模式 ,尤其是在T3或T4期(浆膜浸润性)胃癌患者中,高达50%的患者在接受根治性手术后会出现腹膜转移 。一旦发生腹膜转移,患者预后极差,中位生存期仅3-6个月,5年总生存率低于2%。因此,早期、准确地识别高危患者对于改善治疗决策和预后至关重要。然而,目前临床常用的预测手段存在明显局限:TNM分期系统无法对同为局部晚期的浆膜浸润性胃癌患者进行进一步的风险分层 ;CT检查仅能发现具有大网膜饼征或腹膜增厚等典型特征的晚期腹膜转移,对早期或隐匿性转移敏感性低;腹腔灌洗细胞学检查灵敏度也不理想,许多阴性结果的患者术后仍会发生腹膜转移。近年来,越来越多的证据表明,内脏脂肪组织不仅是能量储存器官,更通过分泌脂肪因子、调控局部炎症和维持促肿瘤微环境等机制,主动参与肿瘤细胞的腹腔播散和种植过程。基于CT影像的内脏脂肪组织特征可能无创地捕获这些生物学信息。深度学习技术能够提取人眼难以识别的深层影像特征,为整合肿瘤与内脏脂肪组织特征、构建更精准的预测模型提供了新的技术途径。在此背景下,开发一种基于术前CT影像的无创预测工具,具有重要的临床意义。
研究目的
本研究旨在开发并验证一种融合肿瘤和内脏脂肪组织CT影像特征与临床指标的深度学习模型 ,用于预测浆膜浸润性胃癌患者接受根治性胃切除术后发生腹膜转移的风险 。具体而言,该研究利用多中心回顾性队列数据,首先采用ResNet18网络分别从术前CT的肿瘤区域和内脏脂肪组织区域提取深度学习特征,构建基于肿瘤、内脏脂肪组织以及两者融合的深度学习特征标签。进一步,将这些深度学习特征与术前可获得的临床变量(如性别、肿瘤位置等)相结合,通过稀疏贝叶斯极限学习机构建一个多模态深度学习影像组学模型 。研究通过受试者工作特征曲线下面积、综合判别改善指数、校准曲线、决策曲线分析以及无复发生存期等多种指标,在内部测试集和独立外部测试集中全面评估模型的预测性能、校准度和临床净收益。最终目标是实现术前无创评估腹膜转移风险,对患者进行有效的术后风险分层,从而指导个体化治疗决策------例如筛选适合接受术中或术后腹腔内化疗的高危患者,避免对低危患者进行不必要的过度治疗,并为更密切的术后随访或临床试验入组提供依据。
03
数据和方法
研究数据
样本来源:两家中心(暨南大学附属第一医院、江门市中心医院)
时间范围:2008年4月至2018年1月
总样本量:416例(训练集181例、内部测试集121例、外部测试集114例)
入组标准:
接受根治性胃切除术
病理 confirmed 浆膜浸润性胃癌
术前4周内行增强CT
完整临床和随访资料
排除标准:术前已有PM、接受过新辅助治疗
PM发生率:中心1为23.5%,中心2为22.8%
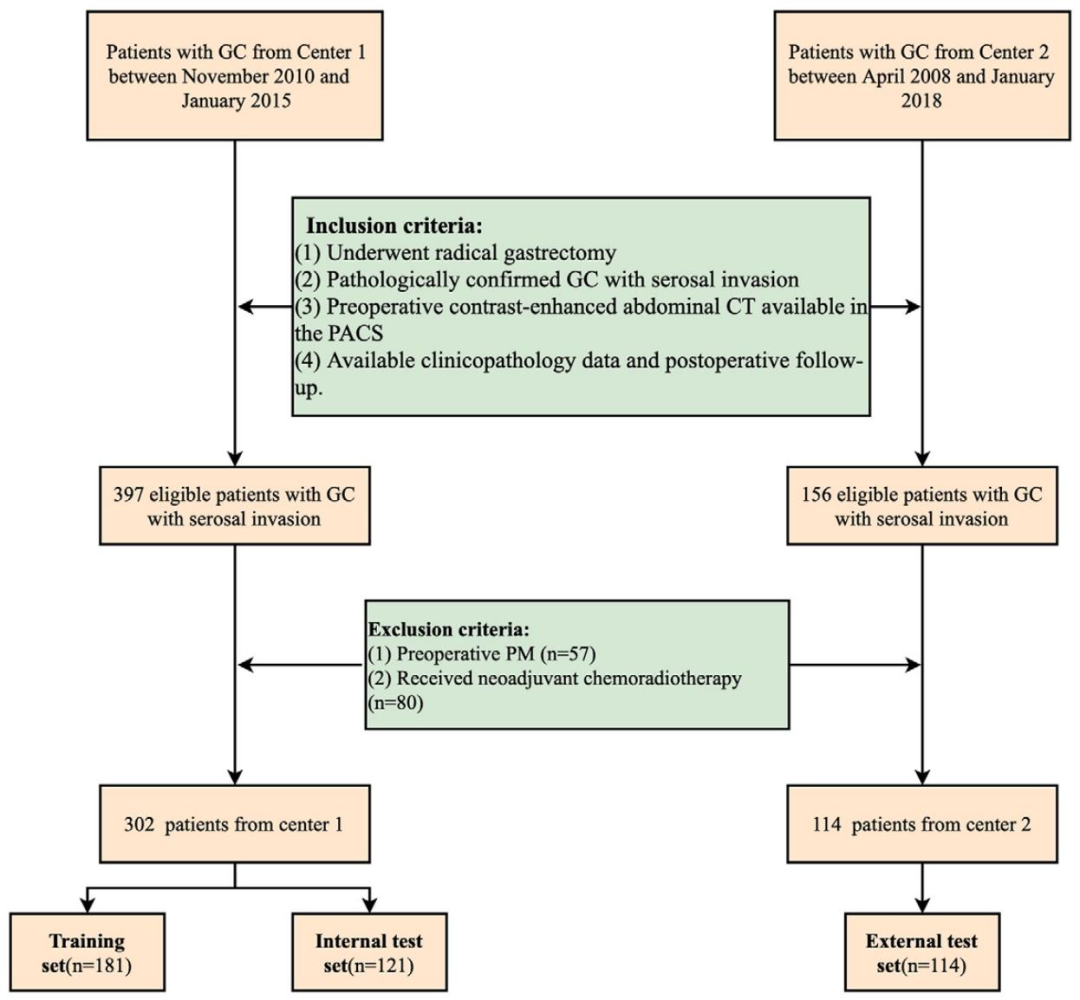
图 1:患者筛选流程图
技术方法
影像处理:
人工勾画肿瘤ROI
自动分割VAT(同一CT层面)
深度学习模型:
使用预训练ResNet18提取肿瘤和VAT特征
构建三种DLS:TT-DLS、VAT-DLS、F-DLS
模型构建:
使用稀疏贝叶斯极限学习机(SBELM)
融合临床变量构建多模态深度学习影像组学模型(MDLR)
评估指标:AUC、IDI、校准曲线、决策曲线分析、Kaplan-Meier生存分析
可视化:Grad-CAM用于解释模型关注区域
04
实验结果
****①F-DLS表现:内部测试集AUC=0.81,外部测试集AUC=0.79
****②MDLR表现:内部测试集AUC=0.86,外部测试集AUC=0.86,显著优于临床模型和单区域DL模型(IDI,P<0.001)
****③风险分层:高风险组RFS显著短于低风险组(30.0个月 vs 46.1个月,log-rank P<0.001)
****④可视化:Grad-CAM显示模型关注肿瘤-浆膜界面及VAT区域
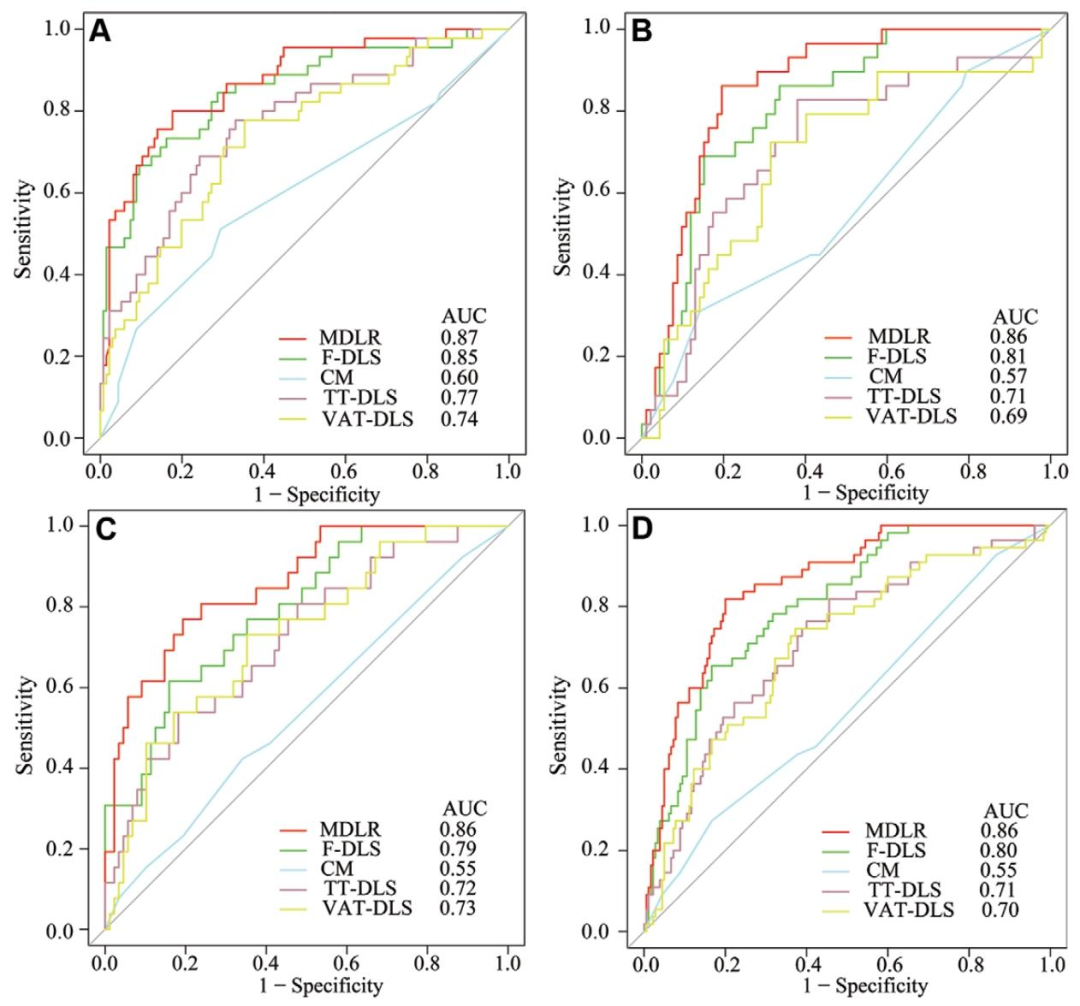
图 3-深度学习模型及多模态模型的ROC曲线: 包含A、B、C、D四个子图,分别对应训练集、内部测试集、外部测试集和总体测试集的ROC曲线。各子图中均展示TT-DLS、VAT-DLS、F-DLS、临床模型和MDLR五条曲线 。结果显示MDLR曲线下面积最大,在内部测试集中达0.86(95% CI: 0.79, 0.92) ,外部测试集同样为0.86,显著优于其他模型。F-DLS也表现出较好性能(AUC约0.80),而单独临床模型表现最差(AUC约0.55-0.60),凸显了深度学习特征融合的价值。
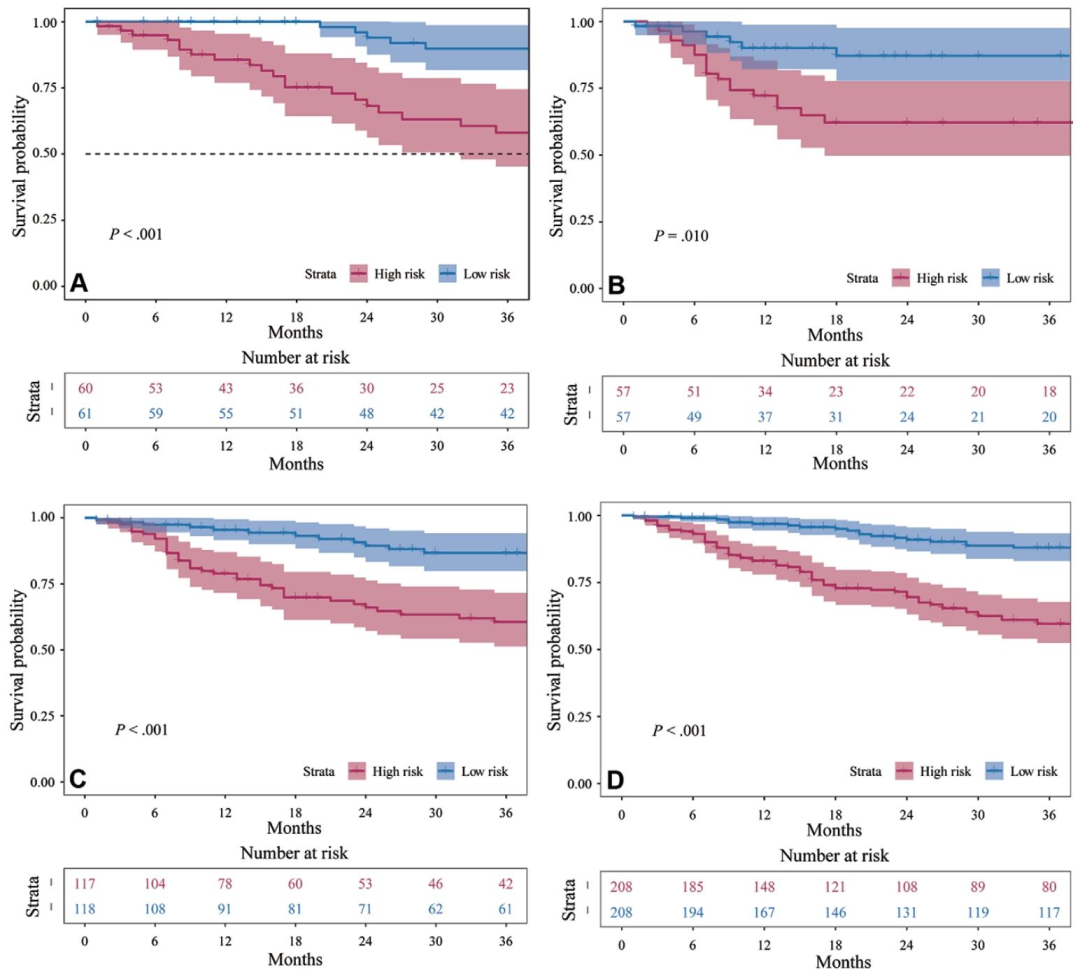
图 4-基于MDLR风险分层的Kaplan-Meier无复发生存曲线: 包含A、B、C、D四个子图,分别对应训练集、内部测试集、外部测试集和总体测试集。各子图均显示高、低风险两组患者的生存曲线 ,以MDLR预测概率结合约登指数确定阈值进行分层。在所有数据集中,高风险组的无复发生存期均显著短于低风险组(log-rank检验P ≤ 0.001) 。例如总体测试集中,高风险组平均无复发生存为30.0个月,低风险组为46.1个月。该图验证了MDLR不仅可预测腹膜转移风险,还能有效实现术后复发风险分层。
05
研究结论
针对浆膜浸润性胃癌患者,研究者构建的多模态深度学习放射组学模型(MDLR) ,通过整合术前CT图像中的肿瘤特征 、内脏脂肪组织(VAT)特征 以及临床指标,能够有效预测根治性胃切除术后腹膜转移风险 。模型在内部和外部独立测试集中均表现出稳健的预测性能(AUC均为0.86),显著优于仅使用临床指标或单一深度学习特征(如单纯肿瘤或VAT特征)的模型。融合肿瘤与VAT特征的深度学习特征(F-DLS) 相比单一区域特征具有更高的预测效能,提示肿瘤与周围脂肪微环境之间存在潜在的协同生物学机制。进一步分析显示,MDLR能够将患者区分为高、低风险组 ,高风险组的无复发生存期显著缩短 ,验证了其在预后分层中的价值。该模型基于术前常规CT影像,无需有创操作 ,有助于早期识别高危患者,从而为个体化治疗决策(如是否实施腹腔内化疗、加强术后监测)提供依据。尽管研究存在回顾性设计、样本量有限等不足,但MDLR为浆膜浸润性胃癌的无创腹膜转移风险分层提供了有前景的工具。
06
Q&A
Q1:本研究提出的MDLR模型相比传统临床模型或单一深度学习特征模型,预测腹膜转移的优势体现在哪些方面?
**A1:**本研究提出的多模态深度学习影像组学模型(MDLR)融合了肿瘤CT特征、内脏脂肪组织(VAT)CT特征以及术前临床指标(如性别、肿瘤位置等)。相比仅基于临床指标的模型(CM,AUC 0.55--0.57)或仅基于肿瘤(TT-DLS)或VAT(VAT-DLS)的单一深度学习模型,MDLR在所有测试集中均表现出更高的AUC(内部测试集AUC 0.86,外部测试集AUC 0.86),显著提升了预测能力。综合判别改善指数(IDI)分析也显示,MDLR显著优于单一特征模型(P < 0.001),且具有良好的校准性和临床净收益。
Q2:为什么本研究选择将内脏脂肪组织(VAT)作为预测腹膜转移的重要影像特征?
**A2:**VAT不仅是能量储存组织,还具有免疫调节和代谢活性,能通过分泌脂肪因子、诱导炎症、促进肿瘤微环境形成等方式影响肿瘤细胞在腹膜中的播散和种植。已有研究表明,VAT与胃癌的化疗反应、并发症和生存率相关。本研究进一步发现,VAT在肿瘤所在CT层面的影像特征具有独立预测价值,VAT-DLS在外部测试集中的AUC达到0.73,说明其在预测腹膜转移中具有重要作用。因此,将VAT纳入模型可更全面地反映腹膜转移的生物学机制。
Q3:本研究的MDLR模型在临床实践中有哪些潜在应用价值?
**A3:**MDLR模型基于术前常规CT影像和临床指标,可无创地预测术后腹膜转移风险,具有以下潜在临床应用价值:
****①筛选高风险患者:为可能从术中腹腔内化疗(IPC)或更激进的治疗策略中获益的患者提供依据;
②指导个体化治疗:辅助制定术后辅助治疗策略,如加强化疗、密切随访或纳入临床试验;
****③避免过度治疗:识别低风险患者,避免不必要的有创治疗或资源浪费;
****④预后分层:通过模型划分的高、低风险组在无复发生存期(RFS)上具有显著差异(log-rank P < 0.001),有助于预后判断和患者沟通。
07